| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点归纳《键参数――键能、键长与键角》考点强化练习(2017年押题版)(四)
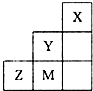 参考答案:由X、Y、Z、M在短周期的相对位置可知,X为氦元素、Y为氟元素、Z为硫元素、M为氯元素. 本题解析: 本题难度:简单 4、选择题 下列物质中,既有离子键又有共价键的离子晶体是( ? ) 参考答案:A 本题解析: 本题难度:一般 5、填空题 有A、B、C、D、E五种原子序数依次增大的元素(原子序数均小于30)。A的基态原子2p能级有3个单电子;C的基态原子2p能级有1个单电子;E的内部各能层均排满,且有成单电子;D与E同周期,价电子数为2。则: 参考答案:(1)3d104s1(2分) 本题解析:有A、B、C、D、E五种原子序数依次增大的元素(原子序数均小于30),A的基态原子2p能级有3个单电子,则A是N元素;C的基态原子2p能级有1个单电子,且C的原子序数大于A,所以C是F元素,则B是O元素;E原子核外有成单电子,其次外层有3个能级且均排满电子,且原子序数小于30,则E是Cu元素;D与E同周期,价电子数为2,则D是Ca元素, 本题难度:一般 |
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点总结《氧化还原反.. | |