微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法不正确的是(?)
A.氯气是黄绿色的有毒气体,氯离子是无色、无毒、比氯原子结构稳定的粒子
B.氯原子易得电子,所以在化学反应中,氯元素化合价只会降低
C.新制的饱和氯水中,除水分子外,较多存在的粒子是Cl2分子
D.铜在氯气中燃烧生成棕黄色烟
参考答案:B
本题解析:误解C,原因是新制饱和氯水的成分含糊不清,只是根据Cl2+H2O====HCl+HClO和2HClO====2HCl+O2↑,误认为Cl2在水中应含有Cl2、H2O、HClO、H+、Cl-、ClO-、OH-多种粒子。殊不知,在新制的饱和氯水中,Cl2很少与水反应,反应也只是少部分反应,故含较多Cl2是正确的。再者,没见过铜在氯气中燃烧的现象,无法判断D是否正确,也有可能出现误选。
对于氯原子,最外层有7个e-,在化学反应中易得e-,但是不是只得e-,它也能在化学反应中自身氧化还原形成正价化合物。例:Cl2+H2O====HCl+HClO、Cl2+2NaOH====NaCl+NaClO+H2O等反应中,HClO、NaClO中的氯元素均显+1价,可见B是不对的。
本题难度:简单
2、填空题 一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应)。生成物中共有三种含氯元素的离子,其中两种离子的物质的量(n)与反应时间(t)的曲线如图。生成C1O3-离子的反应为: 6Ca(OH)2 +6C12 ="=" 5CaC12+Ca(C1O3)2+ 6 H2O。
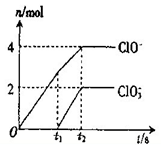
⑴t2时,Ca(C1O)2、Ca(C1O3)2的物质的量之和为??摩尔,该石灰乳中含有Ca(OH)2的质量是 克
(2)据分析,生成Ca(C1O3)2的反应是由温度升高引起的,通入氯气的速率不同,n(C1O-)和n(C1O3-)的比例也不同。若在原石灰乳中通入氯气的速率加快,则反应后n(ClO-)/n(ClO3-)??2.(填">"、"<"或"=");
(3)若n(ClO-)/n(ClO3-) = a,则n(Cl-)=________mol(用含a的代数式表示)
参考答案:(1) 3,(1分)? 740 (1分)?(2)< (2分)(3)n(Cl-)= 10(5+a)/(3+a)( 2分)
本题解析:(1)t2时,n(ClO-)=4mol,n(ClO3-)=2mol,则n[Ca(C1O)2]=2mol,n[Ca(C1O3)2]=1mol,则Ca(C1O)2、Ca(C1O3)2的物质的量之和为3mol;
溶液中还有Cl-,由化合价的升降守恒可知:n(Cl-)=1×4+5×2=14mol,n(CaCl2)=7mol,由钙元素守恒可知,n(Ca(OH)2)=10mol,m(Ca(OH)2)=740g
(2)通入氯气的速率加快,反应速率加快,单位时间内放出的热量就多,则有利于Ca(C1O3)2的生成,则n(ClO-)/n(ClO3-)<2
(3)设n(ClO3-)=x,则n(ClO-)=ax,由电子守恒可知n(Cl-)=5x+ax,由Ca~2Cl,知ax+x+5x+ax=20,得x=10/(3+a),n(Cl-)=10(5+a)/(3+a)
本题难度:简单
3、选择题 工业上制造金刚砂(SiC)的化学方程式如下:SiO2+3C SiC+2CO↑。在这个氧化还原反应中,氧化剂和还原剂的物质的量之比是(?)
SiC+2CO↑。在这个氧化还原反应中,氧化剂和还原剂的物质的量之比是(?)
A.1:2? B.2:1? C.1:1? D.3:5
参考答案:A
本题解析:氧化剂是C,还原产物是SiC;还原剂是C,氧化产物是CO。所以氧化剂和还原剂的比是1∶2。
本题难度:一般
4、选择题 下列气体中无色无味的是( )
A.SO2
B.Cl2
C.NO2
D.N2
参考答案:A、二氧化硫是无色有刺激性气味的气体,故A错误;
B、氯气是黄绿色有刺激性气味的气体,故B错误;
C、二氧化氮是红棕色有刺激性气味的气体,故C错误;
D、氮气是无色无味的气体,故D正确.
故选D.
本题解析:
本题难度:简单
5、填空题 三大强酸的性质均与浓度有关。回答下列问题:
(1)某学习小组用15 mol/L浓硝酸配制100 mL3 mol/L稀硝酸。
①他们需要用量筒量取15 mol/L浓硝酸_______mL;
②如下图所示仪器,在配制过程中不需用的是_________(填序号)。
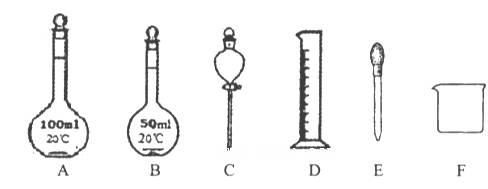
除图中已有的仪器外,配制上述溶液还需用到的玻璃仪器是___________;
③下列实验操作中,不正确的是_________(填写标号)。
A.使用容量瓶前,检查它是否漏水。
B.定容时液面超过刻度线,多出的液体应用胶头滴管吸出。
C.配制溶液时,用量筒量取浓硝酸直接倒入容量瓶中,然后加蒸馏水定容。
D.定容后盖好瓶塞,把容量瓶反复上下颠倒,摇匀。