微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在容积不变的密闭容器中存在如下反应:2SO2(g)+O2(g)
2SO3(g)△H<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是( )
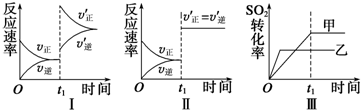
A.图Ⅰ表示的是t1时刻增大O2的浓度对反应速率的影响
B.图Ⅱ表示的是t1时刻加入催化剂后对反应速率的影响
C.图Ⅲ表示的是催化剂对化学平衡的影响,且甲的催化效率比乙高
D.图Ⅲ表示的是压强对化学平衡的影响,且乙的压强较高
参考答案:A.增大氧气的浓度,瞬间逆反应速率不变,图中不符,应为增大压强,故A错误;
B.图Ⅱ正正逆反应速率同等程度的增大,为催化剂对反应的影响,故B正确;
C.催化剂不改变平衡,应为压强对反应的影响,故C错误;
D.乙先达到平衡,压强大,且压强大,转化率增大,转化率与图象不符合,故D错误;
故选B.
本题解析:
本题难度:一般
2、填空题 (14分) 在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K与温度t的关系如下:
CO(g)+H2O(g),其化学平衡常数K与温度t的关系如下:
t℃
| 700
| 800
| 830
| 1000
| 1200
|
K
| 0.6
| 0.9
| 1.0
| 1.7
| 2.6
|
请回答下列问题:(1)该反应的化学平衡常数K =  。
。
(2)该反应为 反应。(填“吸热”或“放热”)
(3)800℃,固定容积的密闭容器中,放入混合物,起始浓度为c(CO)="0.01" mol/L, c(H2O)="0.03" mol/L, c(CO2)="0.01" mol/L, c(H2)="0.05" mol/L ,则反应开始时,H2O的消耗速率比生成速率 (填“大”、“小”或“不能确定”)
(4)830℃,在1 L的固定容器的密闭容器中放入2 mol CO2和1 mol H2,平衡后CO2的转化率为 , H2的转化率为 。
参考答案:
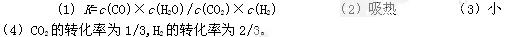
本题解析:略
本题难度:困难
3、选择题 一定条件下存在下列平衡:2A(g)?B(g);△H<O在测定A的相对分子质量时,下列条件中测定结果误差最小的是( )
A.温度150℃、压强5.05×104Pa
B.温度150℃、压强4.04×105Pa
C.温度25℃、压强1.01×105Pa
D.温度0℃、压强5.05×104Pa
参考答案:由于存在平衡2A(g)?B(g),B的存在会影响A的相对分子质量测定,故应采取措施使平衡向左移动,减小B的含量,该反应正反应是体积减小的放热反应,减小压强平衡向逆反应移动,升高温度平衡向逆反应移动,故应采取高温低压,平衡逆向进行,测定结果误差最小,
故选A.
本题解析:
本题难度:一般
4、选择题 下列事实不能用勒沙特列原理解释的是( )
A.由H2、I2蒸气、HI组成的平衡体系加压后颜色变深
B.增大压强,有利于SO2和O2反应生成SO3
C.用排饱和食盐水法收集Cl2
D.工业制取金属钾Na(l)+ KCl(l)  NaCl(l)+ K(g)选适宜的温度,使K成蒸气从反应混合物中分离出来
NaCl(l)+ K(g)选适宜的温度,使K成蒸气从反应混合物中分离出来