微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列表示对应化学反应的离子方程式正确的是
A.用氨水吸收废气中氮的氧化物:NO+NO2+2OH-═2N+H2O
B.用FeCl3溶液刻蚀铜电路板:Cu+Fe3+═Cu2++Fe2+
C.漂白粉溶液在空气中失效:ClO-+CO2+H2O═HClO+HC
D.0.01?mol?L -1 NH4Al(SO4)2溶液与0.02?mol?L-1? Ba(OH)2溶液等体积混合:N+Al3++2S+2Ba2++4OH-═2BaSO4↓+Al(OH)3↓+NH3?H2O
参考答案:D
本题解析:分析:A.一水合氨为弱电解质,在离子反应中应保留化学式;
B.电荷不守恒;
C.反应生成碳酸钙和HClO;
D.NH4Al(SO4)2、Ba(OH)2以1:2反应,生成硫酸钡、氢氧化铝、水.
解答:A.用氨水吸收废气中氮的氧化物的离子反应为NO+NO2+2NH3.H2O═2NH4++2NO2-+2H2O,故A错误;
B.用FeCl3溶液刻蚀铜电路板的离子反应为Cu+2Fe3+═Cu2++2Fe2+,故B错误;
C.漂白粉溶液在空气中失效的离子反应为Ca2++2ClO-+CO2+H2O═2HClO+CaCO3↓,故C错误;
D.0.01?mol?L -1NH4Al(SO4)2溶液与0.02?mol?L-1Ba(OH)2溶液等体积混合的离子反应为NH4++Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+Al(OH)3↓+NH3?H2O,故D正确;
故选D.
点评:本题考查离子反应方程式的书写,明确发生的化学反应是解答本题的关键,选项D为解答的难点,注意氢氧化铝不能溶于弱碱,题目难度不大.
本题难度:困难
2、填空题 (8分)现有三种物质A、B、C,它们均溶于水。其中有一种是酸,一种是碱,一种是盐,溶于水后电离,可以产生下表中的离子:
阳离子
| Na+?H+?Ba2+
|
阴离子
| OH-? CO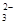 ? SO ? SO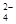 ? ?
|
为鉴别它们,分别完成以下实验,其结果如下:
① A溶液与B溶液反应生成无色气体X,气体X可以和C溶液反应生成沉淀E,沉淀E可与B溶液反应;
② B溶液与C溶液反应生成白色沉淀D,沉淀D不溶于稀硝 酸。
酸。
请根据上述实验结果,填空:
(1)写出下列物质的化学式:X?
(2)B溶于水后的电离方程式为?
(3)鉴别B中阴离子的实验操作方法是?
(4)B与C反应的离子方程式:?
参考答案:

本题解析:略
本题难度:一般
3、选择题 同学们在讨论往碳酸氢铵溶液中滴加石灰水的离子反应时,提出了如下四种结论(用离子方程式形式表达),其中一定不合理的是
A.Ca2++2OH-+NH4++HCO3-→CaCO3↓+NH3?H2O+H2O
B.NH4++CO32-+Ca2++OH-→CaCO3↓+NH3?H2O
C.HCO3-+Ca2++OH-→CaCO3↓+H2O
D.2?HCO3-+Ca2++2OH-→CaCO3↓+2H2O+CO32-
参考答案:BC
本题解析:分析:A、碳酸氢铵过量,氢氧化钙离子方程式中符合化学式组成比;
B、碳酸氢铵反应碳酸氢根离子是弱酸阴离子;
C、依据离子组成分析,氢氧根离子和碳酸氢根离子等物质的量反应,氢氧根离子会和铵根离子反应;
D、碳酸氢铵和氢氧化钙2:1反应时,氢氧根离子全部和碳酸氢根离子反应,铵根离子不反应.
解答:A、碳酸氢铵过量,氢氧化钙离子方程式中符合化学式组成比;Ca2++2OH-+NH4++HCO3-→CaCO3↓+NH3?H2O+H2O符合用量,故A正确;
B、碳酸氢铵反应碳酸氢根离子是弱酸阴离子不能茶城碳酸根离子,故B错误;
C、氢氧根离子和碳酸氢根离子等物质的量反应,氢氧根离子会和铵根离子反应,NH4++HCO3-+Ca2++2OH-→CaCO3↓+H2O+NH3?H2O,故C错误;
D、碳酸氢铵和氢氧化钙2:1反应时,氢氧根离子全部和碳酸氢根离子反应,反应离子方程式为:2 HCO3-+Ca2++2OH-→CaCO3↓+2H2O+CO32-,故D正确;
故选BC.
点评:本题考查了离子方程式的书写方法和产物判断,离子反应顺序分析,题目难度较大.
本题难度:简单
4、填空题 某待测溶液中可能含有Ag+、Fe3+、Na+、Mg2+、Ba2+、Al3+等离子,进行如下实验:①加入过量的稀盐酸,有白色沉淀生成。②过滤,在滤液中加入过量的稀硫酸,又有白色沉淀。③过滤,取少量滤液,滴入KSCN溶液,没有明显的现象出现。④另取少量步骤③中的滤液,加入NaOH溶液至溶液呈碱性,无明显现象。⑤另取少量步骤④反应后的溶液,焰色反应呈黄色。根据实验现象回答:
(1)待测液中一定含有的离子是?。
(2)待测液中一定不含有的离子是?。
(3)待测液中不能确定是否存在的离子是?,要检测这种离子的实验方法是(填写实验名称和观察到的现象,不要求写实验操作过程)?。
参考答案:(每空2分)?(1)Ag+、Ba2+?(2)Fe3+、Mg2+ 、Al3+?
(3)Na+?取原待测液做焰火反应实验,焰色反应呈黄色,证明待测液中含有Na+
本题解析:加入过量的稀盐酸,有白色沉淀生成,说明溶液中含有Ag+。过滤,在滤液中加入过量的稀硫酸,又有白色沉淀,这说明溶液中还含有Ba2+。过滤,取少量滤液,滴入KSCN溶液,没有明显的现象出现,说明溶液中不存在Fe3+。另取少量步骤③中的滤液,加入NaOH溶液至溶液呈碱性,无明显现象,这说明溶液中没有Mg2+ 、Al3+。另取少量步骤④反应后的溶液,焰色反应呈黄色,说明含有钠离子。但由于在实验过程中加入了氢氧化钠溶液,所以不能确定是否含有钠离子。要检测是否含有钠离子,正确的实验操作是取原待测液做焰火反应实验,焰色反应呈黄色,证明待测液中含有Na+。
点评:该题是中等难度的试题,也是高考中的常见题型,试题综合性强,侧重对学生灵活运用基础知识解决实际问题的能力,有利于培养学生的逻辑推理能力和规范严谨的实验设计能力。该题还需要注意的是在进行物质的检验时,要依据物质的特殊性质和特征反应,选择适当的试剂和方法,准确观察反应中的明显现象,如颜色的变化、沉淀的生成和溶解、气体的产生和气味、火焰的颜色等,进行判断、推理、验证即可。
本题难度:一般
5、选择题 下列示意图与对应的反应情况正确的是
[? ]
A.含0.01mol KOH和0.01mol Ca(OH)2的混合溶液中缓慢通入CO2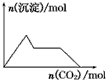
B.NaHSO4溶液中逐滴加入Ba(OH)2溶液 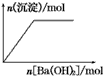 ?
?
C.KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液 
D.NaAlO2溶液中逐滴加入盐酸 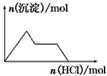
参考答案:B
本题解析:
本题难度:一般