微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 工业制备氯化铜时,将浓盐酸用蒸气加热至80℃左右,慢慢加入粗CuO粉末(含杂质Fe2O3、FeO),充分搅拌,使之溶解,得一强酸性的混合溶液,现欲从该混合溶液中制备纯净的CuCl2溶液,采用以下步骤[参考数据:pH≥9.6时,Fe2+完全水解成Fe(OH)2;pH≥6.4时,Cu2+完全水解成Cu(OH)2;pH≥3.7时,Fe3+完全水解成Fe(OH)3].请回答以下问题:
(1)第一步除去Fe2+,能否直接调整溶液pH=9.6,将Fe2+沉淀除去?______,(填“能”或“不能”)理由是______,
(2)有人用强氧化剂NaClO先将Fe2+氧化为Fe3+,再调整溶液的PH将Fe3+沉淀除去:
①加入NaClO后,溶液的pH变化是______(填代号).
A.一定增大B.一定减小C.可能增大D.可能减小
②你认为用NaClO作氧化剂是否妥当?______,(填“是”或“否”)现有下列几种常用的氧化剂,可用于除去混合溶液中Fe2+的有______(有几个选几个,填代号).
A.浓HNO3B.Cl2 C.KMnO4D.H2O2
(3)加入适当物质调整溶液pH,使Fe3+转化为Fe(OH)3沉淀,可以达到除去Fe3+而不损失CuCl2的目的,则调整溶液pH可选用下列物质中的______.
A.NaOHB.NH3?H2OC.CuOD.Cu(OH)2.
参考答案:(1)由题给信息可知,除去Fe2+时,应避免Cu2+生成沉淀,如直接调整溶液pH=9.6,则生成氢氧化亚铁的同时,氢氧化铜、氢氧化铁也同时生成,
故答案为:不能;因Fe2+沉淀的pH最大,Fe2+沉淀完全时,Cu2+、Fe3+也会沉淀完全;
(2)①NaClO为强碱弱酸盐,水解呈碱性,则加入NaClO,溶液的pH一定增大,另外NaClO可以酸反应生成HClO而导致溶液pH增大,故答案为:A;
②加入氧化剂时,不能引入新的杂质,如用NaClO,则可引入NaCl杂质,应加入氯水或过氧化氢,
故答案为:否;BD;
(3)使Fe3+转化为Fe(OH)3沉淀,应调节溶液的pH,所加物质能与酸反应,注意不能引入新杂质,则可用CuO 或Cu(OH)2或CuCO3;
故答案为:CD.
本题解析:
本题难度:一般
2、选择题 下列叙述中不正确的是
[? ]
A.过滤时,漏斗下端要紧贴接液烧杯内壁
B.蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口
C.分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出
D.测氯水的pH,可用玻璃棒蘸取氯水点在pH试纸上,待其变色后和标准比色卡比较
参考答案:D
本题解析:
本题难度:简单
3、选择题 下列说法正确的是
A.氧的摩尔质量是32 g/mol
B.硝酸的摩尔质量是63 g
C.CO2的相对分子质量是44 g
D.CO32-的摩尔质量是60 g/mol
参考答案:D
本题解析:描述物质的摩尔质量时,必须指明具体微粒.A选项中的“氧”,未指明是氧原子还是氧分子,叙述有误,应该为O2的摩尔质量是32 g/mol;摩尔质量的常用单位是g/mol,B选项中的单位表示有误;相对分子质量是个比值,单位为1,C选项也是单位表示有误;复杂离子的摩尔质量在数值上等于组成离子的各原子相对原子质量总和.
本题难度:简单
4、实验题 某化学小组同学为了验证日常生活所用火柴头中的化学成分(含KClO3、MnO2、S等),设计了以下实验流程(见图-1):?

试回答以下问题:
(1)燃着的火柴按图-2进行实验,若试管中能观察到?的现象,则可证明火柴头中含有硫元素。图中针筒的作用是?。
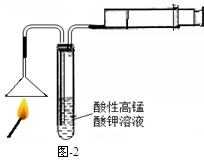
(2)为了证明火柴头中含有氯元素,后续的实验步骤是?。
(3)有同学提出检验火柴头中KClO3的另一实验方案:
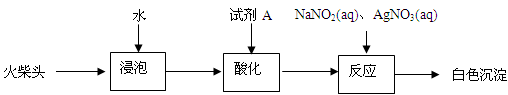
试剂A为?,加入NaNO2的目的是?。
(4)设计实验:简述验证滤渣D中含有MnO2的一个实验方案,并写出有关反应的化学方程式。?。
参考答案:(1)KMnO4溶液褪色或颜色变浅或其他正确描述(2分)、
(意思正确即可)(1分)
(2)取少量滤液C置于试管中,先后加入HNO3、AgNO3溶液,若观察到白色沉淀产生,,即可证明火柴头中含有氯元素。(1分×3)
(3)硝酸或HNO3(1分);还原KClO3(1分)
(4)取少量滤渣D加入装有少量H2O2的试管中,有大量气泡放出说明含有MnO2(2分);
2H2O2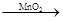 2H2O+O2↑(2分)或其他正确答案。
2H2O+O2↑(2分)或其他正确答案。
本题解析:(1)若有硫元素燃烧中生成了二氧化硫气体会使KMnO4溶液褪色或颜色变浅。用针筒主是使燃烧产生的气体顺利进入试管。
(2)氯元素燃烧中主要生成了氯化氢气体,只要取少量滤液C置于试管中,先后加入HNO3、AgNO3溶液,若观察到白色沉淀产生,,即可证明火柴头中含有氯元素。相当于是氯离子的检验。
(3)KClO3有强的氧化性,在酸性环境下,如加硝酸或HNO3主要是酸化,而亚硝酸钠有较强的还原性,可以还原KClO3为氯离子。
(4)验证是否有MnO2,可以用实验室制取氯气的方法,也可以做为催剂如取少量滤渣D加入装有少量H2O2的试管中,有大量气泡放出说明含有MnO2,相关反应? 2H2O2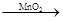 2H2O+O2↑
2H2O+O2↑
本题难度:一般
5、选择题 下列除去杂质的方法正确的是( )
A.除去Al中的少量Fe:加入足量的盐酸,过滤
B.除去CO2中的少量HCl:通入Na2SO3溶液,收集气体
C.除去FeCl2溶液中的少量FeCl3:加入足量铜粉,充分反应后,过滤
D.除去KCl溶液中的少量MgCl2:加入适量的KOH溶液,过滤后加入少量稀盐酸,加热
参考答案:A.铝和铁都能与盐酸反应,将原物质除掉,故A错误;
B.盐酸与Na2SO3溶液反应生成二氧化硫,引入新的杂质,故B错误;
C.氯化铁与铜反应生成氯化亚铁和氯化铜,引入了新的杂质,故C错误;
D.氯化镁与氢氧化钾生成氯化钾和氢氧化镁,过滤后加入少量稀盐酸除掉过量的KOH溶液,故D正确.
故选D.
本题解析:
本题难度:简单