微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
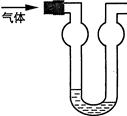
1、选择题 双球洗气管是一种多用途仪器,常用于去除杂质、气体干燥、气体吸收(能防止倒吸)等实验操作。右图是用水吸收下列某气体时的情形,根据下面附表判断由左方进入的被吸收气体是?
A.Cl2
B.HCl
C.H2S
D.CO2
参考答案:B
本题解析:四种气体的溶解度表(室温下)
附:
气体
Cl2
HCl
H2S
CO2
l体积水约能吸收气体体积数
2
500
2.6
1
?
由四种气体的溶解度表可以看出,HCl溶解度最大,溶解的速率大于气体进入洗气管的速率,导致左侧洗气管气压降低,出现如图所示情形。
本题难度:一般
2、选择题 提纯含杂质的固体碘单质最常用的方法是
A.萃取
B.重结晶
C.升华
D.蒸馏
参考答案:C
本题解析:试题分析:根据碘易升华的物理性质可判断提纯含杂质的固体碘单质最常用的简单方法是升华,C正确。萃取适合于溶质在不同溶剂中的溶解性不同而分离的一种方法,结晶法适用于不同溶质的溶解度受温度影响不同而分离的一种方法,蒸馏是依据混合物中个组分沸点不同而分离的一种法,适用于除去易挥发、难挥发或不挥发杂质,所以答案选C。
考点:考查物质的分离和提纯
点评:该题是高考中的常见题型,属于基础性试题的考查,主要是考查学生对常见物质分离和提纯方法的熟悉了解程度,旨在考查学生灵活运用基础知识解决实际问题的能力,有利于培养学生的逻辑推理能力和发散思维能力。
本题难度:一般
3、选择题 下列实验设计方案中,可行的是(?)
A.用加入适量铜粉的方法除去Mg(NO3)2溶液中混有的AgNO3
B.用洗气瓶中的NaOH溶液除去CO2中混有的HCl气体
C.向某无色未知溶液中仅加入BaCl2溶液,以检验未知溶液中的SO42-
D.先滴加石蕊试液,后滴加BaCl2溶液,将盐酸、硫酸、硫酸钠、氢氧化钠和硝酸钾五种无色溶液鉴别开
参考答案:D
本题解析:A不正确,因为又引入了铜离子,应该用镁粉;CO2也能被氢氧化钠溶液吸收,应该用饱和碳酸钠溶液,B不正确;C不正确,应该首先加入盐酸,没有现象后,在加入氯化钡溶液检验SO42-;D正确,石蕊试液可以先鉴别开氢氧化钠。而盐酸与硫酸、硫酸钠与硝酸钾可以分为2组。然后利用氯化钡鉴别硫酸和硫酸钠,答案选D。
点评:该题是高考中的常见题型和重要的考点之一,试题综合性强,注重解题的灵活性和逻辑性,有助于培养学生的逻辑思维能力,提高学生分析问题、解决问题的能力。该类试题学生要明确的是进行物质的检验时,要依据物质的特殊性质和特征反应,选择适当的试剂和方法,准确观察反应中的明显现象,如颜色的变化、沉淀的生成和溶解、气体的产生和气味、火焰的颜色等,进行判断、推理、验证即可。
本题难度:一般
4、填空题 某科研小组以难溶性钾长石(K2O?Al2O3?6SiO2)为原料,提取A12O3、 K2CO3等物质,工艺流程如下:
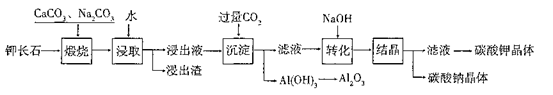
(1)“煅烧”过程中有如下反应发生:
①钾长石中的硅元素在CaCO3作用下转化为CaSiO3,写出SiO2转化为CaSiO3的化学方程式_____________________。
②钾长石中的钾元素和铝元素在Na2CO3作用下转化为可溶性的NaAlO2和 KAlO2,写出Al2O3转化为NaAlO2的化学方程式____________________________。
(2)已知NaAlO2和KAlO2易发生如下反应:AlO2-+2H2O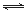 Al(OH)3+OH-。
Al(OH)3+OH-。
“浸取”时,应保持溶液呈______性(填“酸”或“碱”)。“浸取”时不断搅拌的目的是______________。
(3)“转化”时加入NaOH的主要作用是_______ (用离子方程式表示)。
(4)上述工艺中可以循环利用的主要物质是_______、_______和水。
参考答案:(1)①CaCO3+SiO2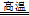 CaSiO3+CO2↑?(3分)
CaSiO3+CO2↑?(3分)
②Na2CO3+Al2O3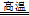 2NaAlO2+CO2↑?(3分)
2NaAlO2+CO2↑?(3分)
3? CuCl? FeCl2(3分)?
② Cl-+ CuCl = [CuCl2]-(2分)
③ 4FeCO3 + O2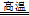 4CO2 + 2Fe2O3(3分)
4CO2 + 2Fe2O3(3分)
④ CuCl2、 NaCl (4分)
(2)(共4分)不会产生SO2污染大气(2分),不用煅烧黄铜矿从而节约热能 [或可得副产品铁红和硫,合理答案都行。2分]
本题解析:(1)①读图可知,缺少的生成物为FeCl2、CuCl,硫元素由―2升为0,设CuFeS2的系数为1,则2个硫原子升高总数为4,铜元素由+2降为+1,1个铜原子降低数为1,由于升降总数相等,则铁元素由+3降为+2,需要3个铁原子降低总数3,则CuFeS2+3FeCl3=CuCl+4FeCl2+2S;②依题意,难溶的CuCl与可溶的NaCl在水中发生反应,其原理为Cl-+ CuCl = [CuCl2]-;③依题意,该反应的反应物是FeCO3和O2,生成物是Fe2O3和CO2,铁元素由+2升为+3价,氧元素由0降为―2价,根据最小公倍数法配平可得:4FeCO3 + O2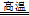 4CO2 + 2Fe2O3;依题意,Na[CuCl2]在水中发生反应V,铜元素由+1部分升高为+2,部分降低为0,则溶液A中含有Cl-、Cu2+和Na+,所以推断A的溶质主要是CuCl2和NaCl;(2)传统方法需要高温煅烧,不仅消耗大量的能量,而且还产生大量的SO2等有毒气体,污染空气,新方法的优点是不会产生SO2污染大气,不用煅烧黄铜矿从而节约热能,可得副产品铁红和硫。
4CO2 + 2Fe2O3;依题意,Na[CuCl2]在水中发生反应V,铜元素由+1部分升高为+2,部分降低为0,则溶液A中含有Cl-、Cu2+和Na+,所以推断A的溶质主要是CuCl2和NaCl;(2)传统方法需要高温煅烧,不仅消耗大量的能量,而且还产生大量的SO2等有毒气体,污染空气,新方法的优点是不会产生SO2污染大气,不用煅烧黄铜矿从而节约热能,可得副产品铁红和硫。
本题难度:一般
5、选择题 下列分离或提纯物质的方法错误的是
A.用渗析的方法精制氢氧化铁胶体
B.用加热的方法提纯含有少量碳酸氢钠的碳酸钠
C.用溶解、过滤的方法提纯含有少量硫酸钡的碳酸钡
D.用盐析的方法分离、提纯蛋白质
参考答案:C
本题解析:
考查物质分离和提纯
硫酸钡和碳酸钡都是难溶性物质,C不正确,其余都是正确的,答案选C。
本题难度:一般