��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ������ڻ�ѧ��Ӧ���ȵ������У���ȷ����
A����ѧ��Ӧ���ȶ���ͬ
B������ͨ���ı��¶ȿ��ƻ�ѧ��Ӧ����
C������ͨ���ӳ���ѧ��Ӧ��ʱ��ı仯ѧ��Ӧ����
D����һ����ѧ��Ӧ��һ�������´ﵽ��ʱ����Ӧ��ֹͣ
�ο��𰸣�B
���������A����Ӧ�����ܷ�Ӧ����Ӧ������Ӱ�죬��Ӧ����Ӧ������ͬ����Ҳ��ͬ������B����Ӧ�����¶�Ӱ�죬����ͨ���ı��¶ȿ��ƻ�ѧ��Ӧ���ȣ���ȷ��C����Ӧ�ﵽһ�����Ⱥ��������䣬��Ӧ�Ȳ��䣬�����淴Ӧʱ��ĸı���ı䣬����D����ѧ��Ӧ����һ�ֶ�̬ƽ�⣬��Ӧ���ڽ��У�����ֹͣ������ѡB��
�����Ѷȣ�һ��
2��ѡ���� ���ݻ�һ�����ܱ������У���ӦA(?)+B(g) C(g)+2D(g)�ﵽƽ��������¶�������������ܶ���������������һ����ȷ����
C(g)+2D(g)�ﵽƽ��������¶�������������ܶ���������������һ����ȷ����
A������Ӧ�����ȷ�Ӧ����A������̬
B������Ӧ�Ƿ��ȷ�Ӧ����A����̬
C����������C������A��ת��������
D���ı�ѹǿ�Ը�ƽ����ƶ���Ӱ��
�ο��𰸣�A
�����������
�����Ѷȣ���
3��ѡ���� ������ɱ���ܱ������У���ӦmA(g)��nB(s)  pC(g)�ﵽƽ���ѹ�����������������A��ת������֮���ͣ�����˵���У���ȷ����
pC(g)�ﵽƽ���ѹ�����������������A��ת������֮���ͣ�����˵���У���ȷ����
A��(m��n)�ض�С��p
B��(m��n)�ض�����p
C��m�ض�С��p
D��m�ض�����p
�ο��𰸣�C
����������������֪ѹǿ���ƽ�����ƣ�m<p
�����Ѷȣ�һ��
4������� ���п���֤��H2(g)+I2(g) 2HI(g)�Ѵ�ƽ��״̬��������������?
2HI(g)�Ѵ�ƽ��״̬��������������?
�ٵ�λʱ��������n mol H2��ͬʱ,����n mol HI
��һ��H��H�����ѵ�ͬʱ������H��I������
�۰ٷֺ���w(HI)=w(I2)
�ܷ�Ӧ����v(H2)=v(I2)=v(HI)
��c(HI)��c(H2)��c(I2)=2��1��1
���¶Ⱥ����һ��ʱ,������Ũ�Ȳ��ٱ仯
���¶Ⱥ����һ��ʱ,������ѹǿ���ٱ仯
������һ��,��������ƽ����Է����������ٱ仯
�ο��𰸣��ڢ�
����������÷�Ӧ��һ����Ӧǰ���������ʵ������ֲ���ķ�Ӧ,���ѹǿ��ƽ����Է����������䲻����Ϊƽ���оݡ�
�����Ѷȣ�һ��
5������� ��18�֣���֪���淴ӦCO2(g) + H2(g) CO(g) + H2O(g)��
CO(g) + H2O(g)��
��д���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽ��K=?��
��830Kʱ������ʼʱ��c (CO2)=2mol/L��c (H2)=3mol/L��ƽ��ʱCO2��ת����Ϊ60%��������ת����Ϊ?��KֵΪ?��
��830Kʱ����ֻ����ʼʱc (H2)��Ϊ6mol/L����������ת����Ϊ?��
����830Kʱ����ʼŨ��c (CO2) =" a" mol/L��c (H2) =" b" mol/L��H2O��ƽ��Ũ��Ϊc (H2O) =" c" mol/L����a��b��c֮��Ĺ�ϵʽ�� ?���ڵ�a = bʱ��a =?c��
�ο��𰸣���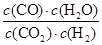 ?��3�֣� ��40%��3�֣��� 1��3�֣� ?��25%��3�֣�
?��3�֣� ��40%��3�֣��� 1��3�֣� ?��25%��3�֣�
��c2��(a-c) (b-c) ��3�֣�?��?a��2c��3�֣�
�����������1����ѧƽ�ⳣ������һ�������£������淴Ӧ�ﵽƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ��Ũ�ȵ���֮���ı�ֵ�������CO2(g) + H2(g) CO(g) + H2O(g)��֪���÷�Ӧ��ƽ�ⳣ������ʽΪ��K�T
CO(g) + H2O(g)��֪���÷�Ӧ��ƽ�ⳣ������ʽΪ��K�T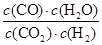 ��
��
��2��ƽ��ʱCO2��ת����Ϊ60%��������CO2��Ũ����2mol/L��0.6��1.2mol/L�����Ը��ݷ�ӦʽCO2(g) + H2(g) CO(g) + H2O(g)��֪����������Ũ����1.2mol/L������������ת����Ϊ
CO(g) + H2O(g)��֪����������Ũ����1.2mol/L������������ת����Ϊ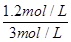 ��100%��40%��ƽ��ʱʣ��CO2��������Ũ�ȷֱ���0.8mol/L��1.8mol/L������CO��ˮ������Ũ�Ⱦ���1.2mol/L�����Ը��¶��·�Ӧ��ƽ�ⳣ��K��
��100%��40%��ƽ��ʱʣ��CO2��������Ũ�ȷֱ���0.8mol/L��1.8mol/L������CO��ˮ������Ũ�Ⱦ���1.2mol/L�����Ը��¶��·�Ӧ��ƽ�ⳣ��K��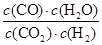 ��
��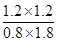 ��1��
��1��
��3��830Kʱ����ֻ����ʼʱc (H2)��Ϊ6mol/L��������������Ũ��Ϊx����
CO2(g) + H2(g) CO(g) + H2O(g)
CO(g) + H2O(g)
��ʼŨ�ȣ�mol/L��? 2? 6? 0? 0
ת��Ũ�ȣ�mol/L��? x? x? x? x
ƽ��Ũ�ȣ�mol/L�� 2��x? 6��x? x? x
���Ը���ƽ�ⳣ��K��֪ ��1
��1
���x��1.5
����������ת����Ϊ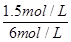 ��100%��25%
��100%��25%
��4������830Kʱ����ʼŨ��c (CO2) =" a" mol/L��c (H2) =" b" mol/L��H2O��ƽ��Ũ��Ϊc (H2O) =" c" mol/L����
CO2(g) + H2(g) CO(g) + H2O(g)
CO(g) + H2O(g)
��ʼŨ�ȣ�mol/L��? a? b? 0? 0
ת��Ũ�ȣ�mol/L��? c? c? c? c
ƽ��Ũ�ȣ�mol/L�� a��c? b��c? c? c
���Ը���ƽ�ⳣ��K��֪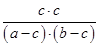 ��1
��1
���c2��(a-c) (b-c)
�ڵ���a��bʱ�������c2��(a-c) (b-c)��֪a��2c��
�����Ѷȣ�һ��