��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��Ӧ��A = 2B�У�A��B��Ũ�ȱ仯��ͼ��ʾ����2min���ڵ�ƽ����Ӧ������Ϊ�� ? ��

A��VA= 9 mol/��L��min��
B��VA= 4.5 mol/��L��min��
C��VB= 18 mol/��L��min��
D��VB= 9mol/��L��min��
�ο��𰸣�D
���������
�����Ѷȣ���
2��ѡ���� ���ܱ������г���4 mol X����һ���¶���4X(g)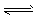 3Y(g)+Z(g)���ﵽƽ��ʱ����30%��X�����ֽ⣬��ƽ��ʱ��������ܵ����ʵ�����
3Y(g)+Z(g)���ﵽƽ��ʱ����30%��X�����ֽ⣬��ƽ��ʱ��������ܵ����ʵ�����
[? ]
A��4 mol
B��3.4 mol
C��2.8 mol
D��1.2 mol
�ο��𰸣�A
���������
�����Ѷȣ�һ��
3��ѡ���� ��10�֣���1����֪���淴Ӧ��M(g)��N(g) P(g)��Q(g)?��H��0��
P(g)��Q(g)?��H��0��
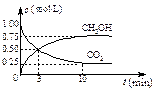
��Ҫ����Q��Ũ�ȣ��������������������¿��Բ�ȡ�Ĵ�ʩΪ?������ţ���
A������һ����M? B�����ͷ�Ӧ�¶�? C�����߷�Ӧ�¶�?
D����С�������? E���������? F�������һ����P
��2����˹�����������Ϳ�ѧ�о����к���Ҫ�����塣��Щ��Ӧ�ķ�Ӧ����Ȼ��ֱ�Ӳ�ã�����ͨ����ӵķ����ⶨ���ָ�������3���Ȼ�ѧ��Ӧ����ʽ��
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)?��H����24.8 kJ��mol��1
3Fe2O3(s)+ CO(g)==2Fe3O4(s)+ CO2(g)?��H����47.2 kJ��mol��1
Fe3O4(s)+CO(g)==3FeO(s)+CO2(g)?��H����640.5 kJ��mol��1
д��CO���廹ԭFeO����õ�Fe �����CO2������Ȼ�ѧ��Ӧ����ʽ��
_________________?��
��3�������Ϊ1 L���ܱ������У�����1 mol CO2��3 mol H2��һ�������·�����Ӧ�� CO2(g)+3H2(g) CH3OH(g)+H2O(g)? ��H=��49.0 kJ/mol�� ��
CH3OH(g)+H2O(g)? ��H=��49.0 kJ/mol�� ��
��CO2��CH3OH(g)��Ũ����ʱ��仯����ͼ��ʾ��
�ٴ�3 min��10 min��v(H2)=?mol/(L��min)��
����˵��������Ӧ�ﵽƽ��״̬����?��ѡ���ţ���
A����Ӧ��CO2��CH3OH�����ʵ���Ũ��֮��Ϊ1�U1����ͼ�н���㣩
B�����������ܶȲ���ʱ��ı仯���仯
C����λʱ����ÿ����3 mol H2��ͬʱ����1 mol H2O
D��CO2����������ڻ�������б��ֲ���
�����д�ʩ����ʹn (CH3OH)/n (CO2)�������?��ѡ���ţ���
A�������¶�? B�����º��ݳ���He(g)
C����H2O(g)����ϵ�з���? D�����º����ٳ���1 mol CO2��3 mol H2
�ο��𰸣���1��A C D F��2�֣�
��2��CO(g)+FeO(s)= Fe(s) + CO2(g)?��H=?��218.00kJ��mol��1��2�֣�
��3��? ��0.11��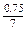 ����D? ��CD?��ÿ��2�֣�
����D? ��CD?��ÿ��2�֣�
�����������
�����Ѷȣ���
4������� �����ܡ�����δ�������������Դ��
��ʵ���ã�1 g����ȼ������Һ̬ˮʱ�ų�142.9kJ������������ȼ�յ��Ȼ�ѧ����ʽΪ_______��
A. 2H2(g)+O2(g)=2H2O(l) ��H=-142.9kJ/mol
B. H2(g)+1/2O2(g)=H2O(l) ��H=-285.8kJ/mol
C. 2H2+O2=2H2O(l) ��H=-571.6 kJ/mol
D. H2(g)+1/2O2(g)=H2O(g) ��H=-285.8 kJ/mol
��ij��ѧ�Ҹ��ݡ�ԭ�Ӿ��á���˼�룬����������Ʊ�H2�ķ�Ӧ���裺
��CaBr2+H2O CaO+2HBr
CaO+2HBr
��2HBr+Hg HgBr2+H2
HgBr2+H2
��HgBr2+_____ ______
______
��2HgO2 Hg+O2��
Hg+O2��
������ݡ�ԭ�Ӿ��á���˼�������������۵Ļ�ѧ����ʽ��__________________�����ݡ���ɫ��ѧ����˼�������÷�����H2����Ҫȱ�㣺_______��
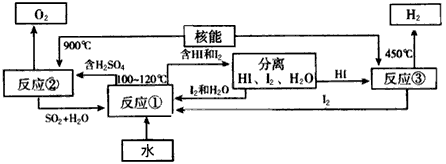
�����ú��ܰ�ˮ�ֽ�����������Ŀǰ�����о��Ŀ��⡣��ͼ�����е�һ�����̣��������˹����ĵ⡣(��ʾ����Ӧ�ڵIJ�����O2��SO2��H2O) ������з�Ӧ�Ļ�ѧ����ʽ��
��Ӧ��_______________����Ӧ��_____________���˷���ȡ����������ŵ���__________________
��������ͨ��������ˮú���ķ����Ƶá�����CO(g)+ H2O(g)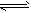 CO2(g)+H2(g) ��H<0 ��850��ʱ��
CO2(g)+H2(g) ��H<0 ��850��ʱ��
K=1��
(1)�������¶ȵ�950��ʱ���ﵽƽ��ʱK_____������ڡ���С�ڡ��� �ڡ���1��
(2)850��ʱ������һ�ݻ��ɱ���ܱ�������ͬʱ����1.0 molCO��3.0mol H2O�� 1.0 molCO2��xmol H2���� �ٵ�x=5.0ʱ������ƽ����_____�������Ӧ�����淴Ӧ����������С�
����Ҫʹ������Ӧ��ʼʱ������Ӧ������У���xӦ�����������________��
(3)��850��ʱ������x=5.0 mol��x=6.0 mol���������ʵ�Ͷ�ϲ��䣬��������Ӧ�ﵽƽ����H2����������ֱ�Ϊa%��b%����a_____������ڡ���С �ڡ����ڡ���b��
V��������ԭ����ͭ���õĺ�ɫ���������ͭ��������ͭ�Ļ�����֪Cu2O ��������Һ�пɷ�������������ԭ��Ӧ������Cu2+�͵���ͭ��
(1)����8g����ͭ��������ԭ�õ���ɫ����6.8 g�����к�����ͭ��������ͭ�����ʵ���֮����_____��
(2)����6.8 g�����������������ϡ�����ַ�Ӧ����ˣ��ɵõ�����_______g��
(3)����6 8 g�����������һ������Ũ�����ַ�Ӧ��
�����ɱ�״����1. 568 L�����壨������NO2���ܽ⣬Ҳ������NO2��N2O4��ת��)���������ijɷ�
��_______�������ʵ���֮����_______��
�ڰѵõ�����ҺС������Ũ�����������ľ�����˳������þ���23. 68 g����������ԭ��Һ�е�Cu2+��
20%������ĸҺ�С������þ���Ļ�ѧʽ��_______��
�ο��𰸣���B
��HgBr2+CaO HgO+CaBr2��ѭ��������Ҫ�ܸߵ���������ʹ���ؽ��������������Ⱦ
HgO+CaBr2��ѭ��������Ҫ�ܸߵ���������ʹ���ؽ��������������Ⱦ
��SO2+I2+2H2O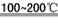 2HI+H2SO4��2H2SO4
2HI+H2SO4��2H2SO4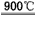 2SO2��+O2��+2H2O��SO2�� I2��ѭ��ʹ�ã�����Ⱦ
2SO2��+O2��+2H2O��SO2�� I2��ѭ��ʹ�ã�����Ⱦ
����(1)С�ڣ�(2)���淴Ӧ����0��x<3��(3)С��
V��(1)2��1��(2)4.8��(3)��NO��NO2��4:3����Cu(NO3)2��6H2O
���������
�����Ѷȣ�����
5��ѡ���� ��ҵ���Ʊ����跴Ӧ���Ȼ�ѧ����ʽ���£�SiCl4(g)��2H2(g)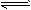 Si(s)��4HCl(g)����H��+QkJ��mol-1 (Q��0)��ij�¶ȡ�ѹǿ�£���һ�����ķ�Ӧ��ͨ���ܱ������������Ϸ�Ӧ������������ȷ����
Si(s)��4HCl(g)����H��+QkJ��mol-1 (Q��0)��ij�¶ȡ�ѹǿ�£���һ�����ķ�Ӧ��ͨ���ܱ������������Ϸ�Ӧ������������ȷ����
[? ]
A����Ӧ�����У�������ѹǿ�����SiCl4��ת����
B������Ӧ��ʼʱSiCl4Ϊ1mol����ﵽƽ��ʱ����������ΪQkJ
C����Ӧ��4minʱ����HCl��Ũ��Ϊ0.12mol��L-1����H2�ķ�Ӧ����Ϊ0.03mol/(L��min)
D������Ӧ��������Ϊ0.025QkJʱ�����ɵ�HClͨ��100mL1mol��L-1��NaOHǡ�÷�Ӧ
�ο��𰸣�D
���������
�����Ѷȣ�һ��