微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知反应?P+Q=M+N是放热反应,下列关于反应能量的变化的说法中不正确的是( )
A.断裂P和Q中化学键吸收的总能量小于形成M和N中化学键释放的总能量
B.P和Q的总能量大于M和N的总能量
C.P和Q的总能量小于M和N的总能量
D.任何化学反应都伴随着能量变化
参考答案:A.生成物化学键生成释放的能量高于反应物化学键断裂放出的能量,故A正确;
B.在放热反应中,反应物的能量高于生成物的能量,故B正确;
C.在放热反应中,反应物的能量高于生成物的能量,故C错误;
D.化学反应在生成新物质的同时,还伴随着能量的变化,故D正确.
故选C.
本题解析:
本题难度:一般
2、选择题 已知25 ℃、101 k Pa下,石墨、金刚石燃烧的化学方程式分别为:C(石墨) + O2(g) = CO2(g),1 moL C(石墨) 完全燃烧放热393.51 kJ;C(金刚石) + O2(g) = CO2(g),1 moL C(金刚石) 完全燃烧放热 395.41 kJ。据此推理所得到的下列结论中,正确的是(?)。
Pa下,石墨、金刚石燃烧的化学方程式分别为:C(石墨) + O2(g) = CO2(g),1 moL C(石墨) 完全燃烧放热393.51 kJ;C(金刚石) + O2(g) = CO2(g),1 moL C(金刚石) 完全燃烧放热 395.41 kJ。据此推理所得到的下列结论中,正确的是(?)。
A.金刚石比石墨稳定
B.由石墨制备金刚石一定是吸热反应
C.石墨的能量比金刚石的能量高
D.石墨转化为金刚石是物理变化
参考答案:B
本题解析:略
本题难度:简单
3、填空题 将煤转化为水煤气是通过化学方法将煤转化为洁净燃料的方法之一。煤转化为水煤气的主要化学反应为:C(s)+H2O(g) ?CO(g)+H2(g)。
?CO(g)+H2(g)。
而C(g)、CO(g)和H2(g)完全燃烧的热化学方程式分别为:
①C(s)+O2(g)=CO2(g) ΔH1=-393.5 kJ・mol-1
②H2(g)+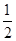 ?O2(g)=H2O(g) ΔH2=-242.0 kJ・mol-1
?O2(g)=H2O(g) ΔH2=-242.0 kJ・mol-1
③CO(g)+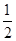 ?O2(g)=CO2(g) ΔH3=-283.0 kJ・mol-1
?O2(g)=CO2(g) ΔH3=-283.0 kJ・mol-1
请你根据上述信息回答下列问题:
(1)煤是一种成分复杂的混合物,其中除含碳、氢元素外,还含有氧、硫、氮、砷、硒等元素。所以固体煤燃烧会导致大气污染,写出煤燃烧产生的两种污染: ,将石灰石粉与煤粉混合,可以有效地减少煤燃烧过程中的二氧化硫污染,写出该反应的化学方程式:____________________
(2)根据已知热化学方程式写出由煤制备水煤气的热化学方程式:____________________________。
(3)下面是甲、乙两位同学对上述热化学方程式及煤燃烧的理解。
甲同学:1 mol CO与1 mol H2燃烧放出的热量之和大于1 mol固体炭燃烧放出的热量,所以煤燃烧时加入少量水,可以使煤燃烧放出更多的热量。
乙同学:根据下面的物质与能量循环,将煤炭转化为水煤气,再燃烧放出的热量与直接燃烧煤炭放出的热量相同,而将煤炭转化为水煤气将会增加消耗,故煤炭转化为水煤气得不偿失。
C(s)+H2O(g)+O2(g) CO2(g)+H2O(g)
CO2(g)+H2O(g)
 ?
?
CO(g)+O2(g)+H2(g) CO(g)+H2O(g)+
CO(g)+H2O(g)+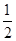 ?O2(g)
?O2(g)
请你评价两位同学的理解:
①甲同学的说法 (答“正确”或“不正确”),原因是______________________________________。
②乙同学的说法 (答“正确”或“不正确”),原因是_____________________________________。
参考答案:(1)酸雨(或答“二氧化硫污染大气”)、含砷粉尘污染、氮氧化物污染(答出两种即可)
2SO2+2CaCO3+O2=2CaSO4+2CO2
(2)C(s)+H2O(g)=CO(g)+H2(g)ΔH=+131.5 kJ・mol-1
(3)①不正确 加入水,水汽化需要吸收能量
②不正确 尽管将煤炭转化为水煤气再燃烧放出的热量与直接燃烧煤炭放出的热量相同,但水煤气与氧气接触面积大,反应速率快,燃烧充分,能量利用率高,污染小
本题解析:煤在燃烧时产生的SO2、NyOx及含砷的化合物等均会污染大气。工业上用CaCO3固硫,发生的反应为:2CaCO3+2SO2+O2=2CaSO4+2CO2。
本题难度:一般
4、选择题 根据热化学方程S ( s ) + O2 ( g ) = SO2 ( g )?△H = -297.23 kJ/mol (反应在298K,101kPa下发生)分析下列说法不正确的是(?)
A.标况下,燃烧1mol S放出的热量为297.23 kJ
B.S ( g ) + O2 ( g ) = SO2 ( g ) 放出的热量大于297.23 kJ
C.S ( g ) + O2 ( g ) = SO2 ( g )放出的热量小于297.23 kJ
D.形成1 mol SO2的化学键所释放的总能量大于断裂 1 molS ( s )和 1mol O2 ( g )的化学键所吸收的总能量
参考答案:AD
本题解析:略
本题难度:简单
5、选择题 相同条件下,如果1mol氢原子所具有的能量为E1,1mol氢分子的能量为E2。下列关系中正确的是
A.2E1=E2
B.2E1>E2
C.2E1<E2
D.E1=E2
参考答案:B
本题解析:形成化学键,放出能量,氢原子生成氢分子是放热的,所以选项B正确,答案选B。
本题难度:一般