微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 某学习兴趣小组探究氨气的制取实验:
(1)甲同学拟用下列实验方法制备氨气,其中合理的是_________。
A.将氯化铵固体加热分解
B.将浓氨水滴入氢氧化钠固体中
C.将氢氧化钠固体加入浓氨水中
D.将氯化铵稀溶液滴入氢氧化钠固体中
(2)根据上述正确的原理,该同学欲用下列常见的实验室制气装置制取氨气,适宜的装置是__________。?

(3)气体的性质是气体收集方法选择的主要依据,下列性质与收集方法无关的是___________。
①密度②颜色③溶解性④热稳定性⑤与氧气反应
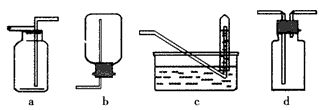
(4)下图是甲同学设计收集氨气的几种装置,其中可行的是_________,集气的原理是:__________。
参考答案:(1)B
(2)C
(3)②④
(4)d ;利用氨气密度小于空气,采用短管进氨气, 长管出空气,即可收集氨气
本题解析:
本题难度:一般
2、简答题 A:某同学用下列装置制取氯气并进行氯气的性质实验,请根据描述的实验现象回答下面的几个问题.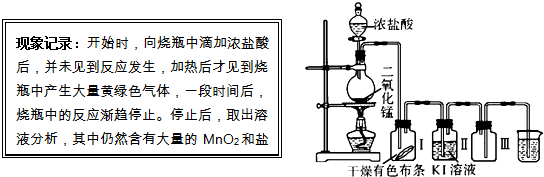
(1)据此现象,你认为在书写MnO2和盐酸反应的化学方程式时,一定要注意______符号的书写和盐酸______的标注.
(2)查阅资料,干燥的氯气没有漂白作用,但实验时发现广口瓶Ⅰ中干燥的有色布条褪色,其原因是______;实验结束后,要从广口瓶Ⅱ中分离得到固态I2,应先进行的操作是______,然后再作进一步的后续处理.
(3)烧杯中物质为氢氧化钠溶液,其作用是______.
(4)在探究氯水漂白原因时,为了确证是HClO起了漂白作用,你认为还应增加的实验是:检验______(填物质名称)能否使红色布条褪色.
参考答案:(1)MnO2和盐酸反应需在加热的条件下反应,且稀盐酸与MnO2不反应,所以书写MnO2和盐酸反应的化学方程式时,一定要注意加热符号的书写和盐酸浓度的标注,反应方程式为:MnO2+4HCl(浓) △.MnCl2+Cl2↑+2H2O,
故答案为:加热;浓度;
(2)浓盐酸中的水在加热条件下变成水蒸气,所以氯气中混有水蒸气;氯气有氧化性,能置换出碘化钾中的碘,广口瓶Ⅱ中Cl2+2KI=2KCl+I2,从氯化钾溶液中获取碘需用萃取的方法,
故答案为:产生的氯气中混有水蒸气;萃取;
(3)氯气有毒,污染环境,所以不能直接排空;氯气能和氢氧化钠反应2NaOH+Cl2 =NaCl+NaClO+H2O,所以可用氢氧化钠溶液吸收多余的氯气,
故答案为:尾气处理,防止环境污染;
(4)氯气和水反应的产物是盐酸和次氯酸,要证明谁有漂白性,得做两个实验:证明盐酸是否有漂白性和证明次氯酸是否有漂白性的实验,
故答案为:盐酸;
本题解析:
本题难度:简单
3、填空题 合成氨工业对化学和国防工业具有重要意义。
(1)实验室欲用下图所示装置(夹持固定装置略去)制备并收集氨气。
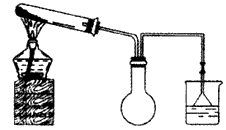
①请在图中烧瓶内绘出导管所缺部分。
②试管中反应的化学方程式是____
③为吸收多余的氨气,烧杯中的试剂是______
(2)氨有很多重要性质。
①将酚酞溶液滴加到氨水中溶液呈红色,其原因是____。
②管道工人曾经用浓氨水检验氯气管道是否漏气,如出现白烟,说明有氯气泄露,同时还有一种相对分子质量为28的气体生成,该反应的化学方程式是____。
(3)写出氨的两种用途____。
参考答案:(1)① 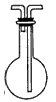
②2NH4Cl+2Ca(OH)2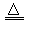 CaCl2+2NH3↑+2H2O
CaCl2+2NH3↑+2H2O
③水(或稀盐酸、硫酸等)
(2)①氨水显碱性(NH3・H2O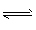 NH4++OH-)
NH4++OH-)
②8NH3+3Cl2=N2 +6NH4Cl
(3)作制冷剂、制硝酸、制化肥、铵盐、纯碱等
本题解析:
本题难度:一般
4、选择题 下列实验装置图正确的是
[? ]
A. 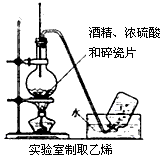
B. 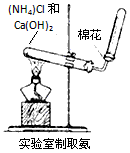
C. 
D. 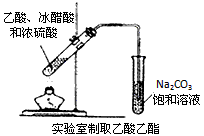
参考答案:B
本题解析:
本题难度:一般
5、实验题 氯气和氨气在常温下混合即可发生反应。某兴趣小组同学为探究纯净、干燥的氯气与氨气的反应,设计了如下装置

请回答:
(1)装置F中发生反应的离子方程式是___,
(2)装置D中盛放的试剂是____,其作用是____,
(3)装置C中有白烟产生,试写出反应的化学方程式__,
(4)若从装置C的G处逸出的尾气中含有少量Cl2,为防止其污染环境,可将尾气通过盛有 ____的洗气瓶。
参考答案:(1) MnO2+4H++2Cl- Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
(2)浓硫酸 ;干燥氯气
(3)8NH3+3Cl2 ==N2+6NH4Cl (或2NH3+3Cl2==N2+6HCl?,?NH3+HCl=NH4Cl)
(4)氢氧化钠溶液
本题解析:
本题难度:一般