| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点总结《离子共存》高频试题强化练习(2017年最新版)(十)
参考答案:C 本题解析:离子间如果发生化学反应,则不能大量共存,反之是可以的。再酸性溶液中,NO3-能氧化Fe2+、I-、S2-,①不能大量共存;②中溶液显碱性,可以大量共存;加入Al能放出H2的溶液既可能是强酸,也可能是强碱。显碱性Mg2+、NH4+不能大量共存,显酸性是可以大量共存的;使石蕊变红的溶液是显酸性的,可以大量共存;水电离的H+浓度c(H+)=10-12mol/L的溶液中,水的电离平衡是被破坏的,溶液既可能显酸性,也可能显碱性。显酸性,HCO3-、S2O32-不能大量共存。显碱性HCO3-、NH4+不能大量共存,所以正确的答案选C。 本题难度:困难 3、选择题 常温下,下列各组离子在指定溶液中一定能大量共存的是( ) 参考答案:A.c(OH-)/c(H+)=1010的溶液,c(OH-)=0.01mol/L,溶液显碱性,Fe3+、OH-结合生成沉淀,则不能共存,故A错误; 本题解析: 本题难度:一般 4、选择题 某无色透明的酸性溶液中能大量共存的一组离子是 |
参考答案:D
本题解析:因为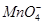 显示紫红色,而溶液是无色透明的,所以可以排除C选项;弱酸的酸根离子在酸性溶液中可以和H+反应生成相应的弱酸,所以
显示紫红色,而溶液是无色透明的,所以可以排除C选项;弱酸的酸根离子在酸性溶液中可以和H+反应生成相应的弱酸,所以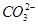 和H
和H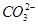 不能在此溶液中大量共存,其反应的离子方程式分别为
不能在此溶液中大量共存,其反应的离子方程式分别为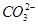 +2H+====H2O+CO2↑、
+2H+====H2O+CO2↑、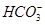 +H+====H2O+CO2↑,排除A和B选项。
+H+====H2O+CO2↑,排除A和B选项。
考点:离子反应
本题难度:一般
5、选择题 下列各离子组中,可以在某种澄清透明溶液中大量共存的是( )
A.I-、Na+、Fe3+、Cl-
B.Na+、Ba2+、Cl-、CO
参考答案:A.因I-、Fe3+发生氧化还原反应,则不能共存,故A错误;
B.因Ba2+、CO32-能结合生成沉淀,则不能共存,故B错误;
C.因该组离子之间不反应,则能共存,故C正确;
D.因H+、Fe2+、NO3-发生氧化还原反应,则不能共存,故D错误;
故选C.
本题解析:
本题难度:简单
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学试题《键参数――键能、.. | |