��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��10�֣������������ƶ�����Ҫ�Ĺ�ҵ��Ʒ����ش�
(1)��ҵұ�����Ļ�ѧ����ʽ��? ________________?��
(2)���������ӽ���Ĥ����ⱥ��ʳ��ˮ��NaOH���乤��ԭ��������ͼ��ʾ��
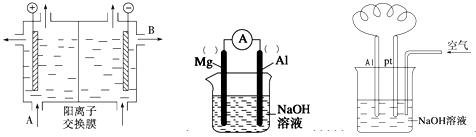
����д��A��B�������ʵ����ƣ�A___________________�� B____________________
B____________________
����д�����ʳ��ˮ�����ӷ���ʽ__________________________________________
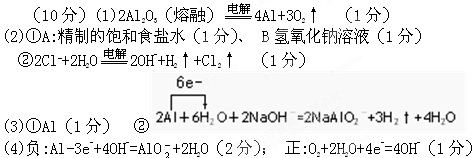
(3)��þ������ƬΪ�缫����NaOH��ҺΪ�������Һ��Ƶ�ԭ���������ͼ��?
�ٸ�������Ϊ________(��Mg��Al)��
�ڸ�ԭ��ص��ܷ�ӦʽΪ____________________________________________
(Ҫ���õ����ű������ת�Ƶķ������Ŀ)
(4)��������ȼ�ϵ�ؿ����ڵ綯������ͨ����NaOH��ҺΪ���Һ�����Ͻ�Ϊ������ͨ������ļ�Ϊ����(������ͼ)����
�����ĵ缫��ӦʽΪ? ______________________?��
�����ĵ缫��ӦʽΪ_______________ ____________________��
____________________��
�ο��𰸣�
�����������
�����Ѷȣ�һ��
2������� ������ҵ�ǹ��ҹ�ҵ�Ļ�����������������ȴ�洦�ɼ���Ϊ��ÿ�������ʧ�� ��?�ʽ���ش������ʴ����������е��й����⣮

��1�������ĵ绯ѧ��ʴԭ���������Ի����з������ⸯʴ�������Ի���Ի����з���������ʴ��
�ٷֱ�д��ͼ1�����缫��ʯī�缫�ĵ缫��Ӧʽ��
??��?��
�ڽ���װ�������ļ��ɳ�Ϊ�����绯ѧ������װ�ã�����ͼ1���߿�����ʾ
λ�������ģ����ü�ͷ��������е�����������
��д���ĺ�ʯī�缫�ĵ缫��Ӧʽ??��
��2����ҵ�ϳ��������ȥ���⣮�ֽ�һ�������Ƭ���������У���Һ�п��ܷ����Ļ�ѧ��Ӧ�Ļ�ѧ����ʽ�� ?��
��3����ʵ�������У���������Ʒ�ı����ͭ��ֹ������ʴ��װ��ʾ����ͼ2��
��A�缫��Ӧ�Ľ����ǣ�дԪ�����ƣ�?��B�缫�ĵ缫��Ӧʽ��?��
�������ǰ����ͭ��Ƭ����������ͬ�������ɺ�����ȡ��ϴ������ɡ�����������������Ϊ5.12g������ʱ��·��ͨ���ĵ���Ϊ?mol ��
�۶Ʋ������ͭ���ȶ�п�������ױ���ʴ�����Ҫ˵��ԭ��?��
�ο��𰸣���1����Fe-2e- =Fe2+? O2+4e-+2H2O=4OH-?��2�֣�
?�� ?��2�֣���2Cl--2e-=Cl2����1�֣�
?��2�֣���2Cl--2e-=Cl2����1�֣�
��2��Fe2O3+6HCl=2FeCl3+3H2O Fe+2HCl=FeCl2+H2�� 2FeCl3+Fe=3FeCl2��3�֣�
��3����ͭ?Cu2++2e-�TCu ��2�֣��� 0.08mol��2�֣�
������ͭ���ã��Ʋ��ƻ����ڳ�ʪ�������γ�ԭ��أ���Ϊ�������������ĸ�ʴ��2�֣�
�����������1����ͼ1Ϊԭ��أ�Fe������������Fe-2e- =Fe2+ʯī������������O2+4e-+2H2O=4OH�������������������������߿����������Դ��ʹ����������������������������෴�� 
���ĺ�ʯīΪ�����������ӷŵ磬2Cl--2e-=Cl2��
��2������ɷ�ΪFe2O3���������ᷴӦ��Fe2O3+6HCl=2FeCl3+3H2O���������ᷴӦ��Fe+2HCl=FeCl2+H2����FeCl3��Fe��Ӧ��2FeCl3+Fe=3FeCl2
��3��������Ʒ�����ͭ������������ͭ��������A�缫��������ӦΪͭ��B�缫��ͭ���ӵĵ��ӻ�ԭΪͭ����ӦʽΪCu2++2e-�TCu��
�ڶ���������Ϊ5.12g��˵����2.56gͭ��������ת�Ƶ������ʵ���2.56g/64g/mol��2=0.08mol�۶�ͭ��������ͭ���ã��Ʋ��ƻ����ڳ�ʪ�������γ�ԭ��أ���Ϊ�������������ĸ�ʴ
�����Ѷȣ�һ��
3��ѡ���� �����йؽ�����ʴ�������˵����ȷ����(����)
A�������������ڿ�������ѧ��ʴ�����䰵
B������������Ʒ�ĶƲ�����ʱ���Ʋ����ܶ�����Ʒ�𱣻�����
C���ں�������������鱣����Dz��ܸ�ʴ�Dz�������������������������
D���ɽ��������ֹ������ֱ����Դ�����������Ա��������ܸ�ʴ
�ο��𰸣�A
��������������������ڿ������ױ�������ʹ���������ڣ��ǻ�ѧ��ʴ��A��ȷ������������ԭ��أ������������ӿ������ĸ�ʴ��B����������еĸ��������ӵ����鹹��ԭ��أ���������ʴ�������Ա������֣�C�������ֱ����Դ��������ʱ�����������ڵ�Դ�����ϣ�D����
�����Ѷȣ�һ��
4��ѡ���� ��ͼ�����Ͻ��������������ں��з�̪��NaCl��Һ�У����Կ����ڽ������������Һ���ַۺ�ɫ���ý�����������? (����)��
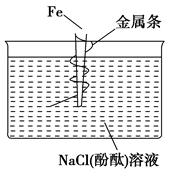
A��ͭ
B��þ
C����
D��п
�ο��𰸣�A
������������ַۺ�ɫ˵������������������OH����������������ʴ����������������������Ա���Ҫ�
�����Ѷȣ���
5��ѡ���� �����ڳ�ʪ�Ŀ����лᷢ��������ʴ������˵���У���ȷ����
[? ]
A�����������ķ�ӦΪ��Fe-2e-��Fe2+
B�����������ķ�ӦΪ��O2+4e-+4H+��2H2O
C����ʴ�����У����Ӵ���������
D��������ˮ�²��ֱ��ڿ�����ˮ���紦��������������ʴ
�ο��𰸣�A
���������
�����Ѷȣ�һ��