��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����˵����ȷ����
A��ÿһ����Ԫ�ض��ǴӼ������ʼ����ϡ���������
B��f�����Ǹ���Ԫ�أ�s����p���Ķ�������Ԫ��
C����֪��200C 1mol Naʧȥ1 mol����������650kJ�����������һ������Ϊ650KJ/mol��
D��Ge�ĵ縺��Ϊ1.8�������ǵ��͵ķǽ���
�ο��𰸣�B
���������A���һ���ھͲ��ǣ��ʴ���C������Ƶ��۵���370�ȡ�����һ������Ҫ������̬���� �γ���һ�۽���������ʱ�����������е��¶Ȳ��ܴﵽҪ�ʴ���D��縺��Ҳ������Ϊ�ж�Ԫ�صĽ����Ժͷǽ�����ǿ���ij߶ȡ�һ����˵���縺�Դ���1.8���Ƿǽ���Ԫ�أ�С��1.8���ǽ���Ԫ�أ���λ�ڷǽ����������߽�ġ�������������ࡢ��ȣ��ĵ縺������1.8���ң����Ǽ��н��������зǽ����ԣ��ʴ�����ѡB��
���������⿼�����Ԫ�������ɺ�Ԫ�����ڱ������֪ʶ����Ŀ�ѶȲ���ּ�ڿ���ѧ���Ի���֪ʶ�����������
�����Ѷȣ�һ��
2������� ��ͼ��������ԭ�ӵ����ʺ�ԭ������(1��20)���Ĺ�ϵͼ����ͼ��������ܴ������е�ijһ���ʣ�����������������������ۡ�ԭ�Ӱ뾶��Դ�С���õ������������ͼ2��ԭ������8��9��ͼ3��ԭ������2��10��18��������û�ж�Ӧ����ֵ��
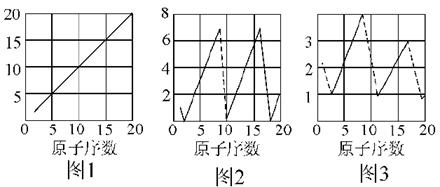
(1)ͼ1��ͼ3������ֱ����__________��__________��__________��
(2)��֪aA��bB��cC��dD��eE��gG����Ԫ��ԭ��������������ԭ�Ӱ뾶��A��E��D��C��B��G��˳���������Ƿ�ɢ�������������С�B��������Ĺ���Ԫ�أ�E��ͬ�����а뾶��С��Ԫ�أ�G�������������ȴ�����������2�������ǵ�ԭ�������������¹�ϵ����a��b��c����(b��d)/2��c����(c��e)/2��d��������ṩ����Ϣ���ش��������⣺
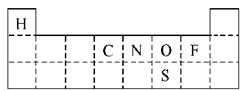
��?��ͼ��Ԫ�����ڱ�ǰ�����ڵı߽磬�뽫A��G���־���Ԫ�ط������ڱ�����Ӧ��λ�ã�
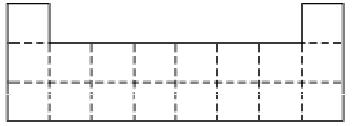
��д��ͭ��CԪ������������Ӧˮ�����Ũ��Һ��Ӧ�Ļ�ѧ ����_______________��
��X��Y��Z��W�ǽ�������Ԫ����ɵ��������ʣ���������ת����ϵ��
X��Y�D��Z��W����XΪ���ʣ�Y��Z��W��Ϊ������Ҹ÷�Ӧ����Ҫ�Ĺ�ҵ������Ӧ������Ӧ�Ļ�ѧ����ʽΪ__________________________��
�ο��𰸣�(1)����������������ۡ��õ����������?��ÿ��1�֣�
 ����3�֣���һ����1�֣�
����3�֣���һ����1�֣�
 ��2����Cu��4HNO3(Ũ)===Cu(NO3)2��2NO2����2H2O?��2�֣�
��2����Cu��4HNO3(Ũ)===Cu(NO3)2��2NO2����2H2O?��2�֣�
��3��4NH3��5O2?4NO��6H2O�� ��2�֣�
�����������
�����Ѷȣ�һ��
3��ѡ���� 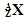 ��
��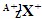 ��������������������ȷ����(����)
��������������������ȷ����(����)
A��һ�����������ӡ����ӡ�������ɵ�
B����ѧ���ʼ�����ȫ��ͬ
C���˵�����ͺ��������һ�����
D��������һ����ͬ����������������һ������ͬ
�ο��𰸣�D
�������������ԭ�ӵ���ɼ���ʾ�������ڱ�ʾԭ�����ʱԪ�ط��ŵ����½DZ�ʾ�����������ϽDZ�ʾ����������Ϊ��������������֮����������������ѡ��D����ȷ�ġ�A����ȷ�������ԭ��ľ���ӡ����ߺ����������ͬ�����Ի�ѧ���ʲ�ͬ��B��C������ȷ����ѡD��
�����Ѷȣ���
4������� V��W��X��Y��Z��ԭ���������εݼ������ֳ���Ԫ�ء�XԪ���ǵؿ��к�������Ԫ�أ�Y��Z��ɵ���̬������M��ˮ��Һ�ʼ��ԣ�W�ĵ�����X2��ȼ�ղ����ʹƷ����Һ��ɫ��V��һ����ʷ�ƾá�Ӧ�ù㷺�Ľ���Ԫ�ء���ش�
��1��YԪ�������ڱ��е�λ����?��д��X��Z����Ԫ����ɵĻ�����Z2X2��һ����;��?��
��2������������Ԫ������������γɵĻ������У���һ����������ˮ��Ӧ���������ҷ�Ӧ����������ԭ��Ӧ����д���÷�Ӧ�Ļ�ѧ����ʽ?��
��3��X��Y��Z����Ԫ�ؿ����һ��ǿ��U��M���ʵ������±�U��������һ���Ρ����ε�ˮ��Һ��pH?7������ڡ�����С�ڡ����ڡ�����ԭ���ǣ������ӷ���ʽ��ʾ��?
��4������V����Ͷ�뵽�����У�������dz��ɫ��ҺN��N��������Һ��˫��ˮ��Ӧ�����ӷ���ʽ��?
��5����������Ѱ����ʵĴ����͵缫���ϣ���Y2��Z2Ϊ�缫��Ӧ���HCl��NH4Cl��ҺΪ�������Һ��������ȼ�ϵ�أ���д���õ�ص������缫��Ӧʽ?���ŵ�ʱ��Һ��H+����?�����������������
�ο��𰸣���1���ڶ�����VA��?��ɫ������
��2��3NO2+H2O=2HNO3+NO
��3����? NH4++ H2O?NH3��H2O+H+
��4��2Fe2++2H++H2O2=2Fe3++ 2H2O
��5��N2+6e-+8H+= 2NH4+ ?��
������������������Ϣ֪��V��W��X��Y��Z��ԭ���������εݼ������ֳ���Ԫ�ء�XԪ���ǵؿ��к�������Ԫ�أ���XΪ��Ԫ�أ�Y��Z��ɵ���̬������M��ˮ��Һ�ʼ��ԣ���MΪ������YΪ��Ԫ�أ�ZΪ��Ԫ�أ�W�ĵ�����X2��ȼ�ղ����ʹƷ����Һ��ɫ����WΪ��Ԫ�أ�V��һ����ʷ�ƾá�Ӧ�ù㷺�Ľ���Ԫ�أ���VΪ��Ԫ�ء���1��YΪ��Ԫ�أ������ڱ��е�λ���ǵڶ�����VA�壻XΪ��Ԫ�أ�ZΪ��Ԫ�أ�������ɵĻ�����H2O2����;����ɫ����������2������������Ԫ������������γɵĻ������У���һ����������ˮ��Ӧ���������ҷ�Ӧ����������ԭ��Ӧ���÷�ӦΪ����������ˮ��Ӧ����ѧ����ʽ3NO2+H2O=2HNO3+NO����3��O��N��H����Ԫ�ؿ����һ��ǿ��HNO3��NH3���ʵ������±�HNO3��������һ����NH4NO3�����ε�ˮ��Һ��pHС��7��ԭ����NH4++ H2O?NH3��H2O+H+����4��VΪ��Ԫ�أ�������Ͷ�뵽�����У�������dz��ɫ��Һ������������������������Һ��˫��ˮ��Ӧ�����ӷ���ʽ��2Fe2++2H++H2O2=2Fe3++ 2H2O����5����������Ѱ����ʵĴ����͵缫���ϣ���N2��H2Ϊ�缫��Ӧ���HCl��NH4Cl��ҺΪ�������Һ��������ȼ�ϵ�أ��õ�ص������缫��ӦʽN2+6e-+8H+= 2NH4+���ŵ�ʱ��Һ��H+����������
�����Ѷȣ�һ��
5������� ��12�֣�������Ԫ�����ڱ���ǰ�������еIJ���Ԫ�أ�
������
| ��A
| ��A
| ��A
| ��A
| ��A
| ��A
| ��A
| 0
|
һ
| H
| ?
| He
|
��
| Li
| ?
| ?
| C
| N
| O
| F
| ?
|
��
| Na
| Mg
| ?
| ?
| ?
| S
| Cl
| ?
|
��1����ЩԪ���У�����õ�Ԫ����?,����õ�Ԫ����??��
��2��ԭ�ӽṹʾ��ͼ ����ʾ��ԭ����?���䵥����Ӳ��Ԫ��Ϊ?��
����ʾ��ԭ����?���䵥����Ӳ��Ԫ��Ϊ?��
��3��Na��Mg����Ԫ�ص�����������Ӧ��ˮ���ﶼ�Ǽ�������ּ�ļ���ǿ��ΪNaOH?Mg(OH)2 (����ڡ���С�ڡ�)��
��4����д�����ϱ���������Ԫ���γɵ�һ�����ӻ�����Ļ�ѧʽ?��
�ο��𰸣���1����4�֣�F? He?��2����4�֣�Cl? C
��3����2�֣�����?��4����2�֣�NaCl/MgCl2
�����������
�����Ѷȣ���