微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 铝在人体中积累可使人慢性中毒,世界卫生组织将铝确定为食品污染源之一而加以控制.铝在下列使用场合中,必须加以控制的是( )
A.制造炊具
B.制防锈油漆
C.制铝箔
D.制电线
参考答案:A.用铝制作炊具时,会使铝进入人体,需要加以控制,故A正确;
B.用铝制防锈油漆,正常情况下铝与人的消化系统不直接接触,铝不会因使用电缆进入人体,与人体健康无关,无需控制,故B错误;
C.制铝箔,铝与人的消化系统不直接接触,铝不会因使用铝箔进入人体,与人体健康无关,无需控制,故C错误;
D.铝作电线电缆与人的消化系统不直接接触,铝不会因使用电缆进入人体,无需控制,故D错误;
故选A.
本题解析:
本题难度:简单
2、选择题 向明矾溶液中滴入Ba(OH)2溶液,当SO42-恰好完全沉淀时,铝元素的存在形式是
A.一部分为Al(OH)3,一部分为Al3+
B.一部分为Al(OH)3,一部分为AlO2-
C.全部是Al(OH)3
D.全部是AlO2-
参考答案:D
本题解析:明矾的组成为KAl(SO4)2・12H2O,溶于水后:
KAl(SO4)2・12H2O=K++Al3+ + 2SO42-+12H2O
1mol? 1mol? 2mol
当使SO42-完全沉淀时,应加2mol Ba2+,即2mol Ba(OH)2,而2mol Ba(OH)2可产生4mol OH-。
2SO42-+2Ba2+=2BaSO4↓
Al3++4OH-=AlO2-+2H2O
可见当SO42-恰好沉淀完全时,Al(OH)3恰好完全消去,变成AlO2-。
本题难度:简单
3、选择题 0.1molMg分别在足量的O2、CO2、N2中燃烧,生成的固体质量依次为W1、W2、W3,则下列关系式中正确的是( )
A.W2>W1>W3
B.W1=W2>W3
C.W1=W2=W3
D.W3>W2>W1
参考答案:A
本题解析:
本题难度:一般
4、推断题 由中学化学常见元素组成的单质A、B、C和甲、乙、丙、丁、戊五种化合物有下图所示转化关系,A是由地壳中含量最多的金属元素组成的。请回答:
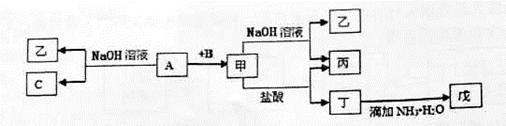
(1)写出下列物质的化学式:乙_______、丁_______、戊_______
(2)写出甲物质在工业上的一种主要用途:_______
(3)写出甲→乙+丙反应的离子方程式:____________
A→乙+C反应的化学方程式______________
参考答案:
(1)乙? NaAlO2;丁 AlCl3?; 戊? Al(OH)3 ?;
(2) 耐火材料 ;
(3) Al2O3+2OH-=2AlO2-+H2O ;? 2Al+2NaOH+2H2O=2NaAlO2+3H2↑ 。
本题解析:地壳中含量最多的金属元素是Al,故A为Al。A与NaOH反应生成NaAlO2和H2,故C为H2,乙为NaAlO2。A与B反应生成的甲可以和NaOH、盐酸反应,则B为O2,甲为Al2O3,则丙为H2O,丁为AlCl3,戊为Al(OH)3。Al2O3可用作耐火材料。
本题难度:一般
5、填空题 (13分)工业上用铝土矿(主要成分是Al2O3,还有少量的Fe2O3、SiO2)提取冶炼铝的原料氧化铝。工艺流程如下图:

(1) 原料A的名称是___▲___,步骤①反应的离子方程式是________▲_________。
(2) 滤液1中要加入稍过量原料B,原料B的化学式是_▲_,步骤②反应的离子方程式是?▲_。
(3) 步骤③的化学方程式是:______________▲_______________。
(4) 如果省去步骤①,即溶解铝土矿是从加入原料B开始,后续操作不变,则会对氧化铝的提取有什么影响______________▲______________。
参考答案:(13分)(1)盐酸(硫酸、硝酸)(2分)?
Al2O3+6H+=2Al3++3H2O(1分)Fe2O3+6H+=2Fe3++3H2O(1分)
(2)NaOH(2分)? H++OH-=H2O(1分)? Fe3++3OH-=Fe(OH)3 ↓(1分)? Al3++4OH-=AlO2-+2H2O(1分)?(3)NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3(2分)
(4)若用NaOH溶液溶解铝土矿,则有部分SiO2溶解在NaOH溶液中生成硅酸钠,最后使 加热制得的Al2O3混有SiO2杂质(2分)
加热制得的Al2O3混有SiO2杂质(2分)
本题解析:略
本题难度:一般