微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 用化学式简要表示下面的反应,并在括号里指出基本反应类型(化合反应或分解反应):
(1)磷在空气中燃烧:
(2)铁丝在氧气中燃烧:
(3)电解水: .
参考答案:(1)4P+5O2 2P2O5;化合反应;(2)3Fe+2O2 Fe3O4;化合反应;
(3)2H2O 2H2↑+O2↑;分解反应.
本题解析:首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写;再根据反应特征确定反应类型.
解:(1)磷在空气中燃烧生成五氧化二磷,反应的化学方程式为:4P+5O2 2P2O5;该反应符合“多变一”的特征,属于化合反应.
(2)铁在氧气中燃烧生成四氧化三铁,反应的化学方程式为3Fe+2O2 Fe3O4;该反应符合“多变一”的特征,属于化合反应.
(3)水通电分解生成氢气和氧气,反应的化学方程式为:2H2O 2H2↑+O2↑;该反应符合“一变多”的特征,属于分解反应.
本题难度:一般
2、填空题 某课外活动小组同学用下图装置进行实验,一段时间后在C电极表面有铜析出,试回答下列问题。
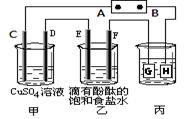
(1)A为电源的?极;
(2)E的电极反应式为:?;
(3)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为?;
(4)在常温下,现用丙装置给铁镀铜,则H电极材料应该是?,
当丙中铁表面析出铜的3.2g时,乙中溶液的PH值为?(假设溶液体积为1L);
(5)在电解一段时间后在甲中加入适量?可以使溶液恢复到原来的浓度。
参考答案:(1)负极?(2)? 2H+2e-=H2↑?(3)? 2:1:2:2?(4)?铜? 13?
(5)CuO(若考虑到水开始电解Cu(OH)2也可以)
本题解析:考查电化学的应用。
(1)C电极表面有铜析出,说明C是阴极,所以A是电源的负极,B是正极H、F、D都是阳极,G和E是阴极。
(2)E是阴极,根据离子的放电顺序可知,溶液中的氢离子放电,反应式为2H+2e-=H2↑。
(3)根据离子的放电能量可判断,C、D、E、F电极产生的单质铜、氧气、氢气和氯气。根据电子的得失守恒可知,四种单质的物质的量之比是2:1:2:2。
(4)电镀时镀层金属作阳极,待镀金属作阴极,含有镀层金属离子的溶液作电镀液,H是阳极,所以电极材料是铜。3.2g铜转移电子是 ,所以乙中生成的氢氧化钠是0.1mol,浓度是0.1mol/L,则pH=13。
,所以乙中生成的氢氧化钠是0.1mol,浓度是0.1mol/L,则pH=13。
(5)甲中的电解产物是铜、氧气和硫酸,所以要使溶液恢复到原来的浓度,应该加入氧化铜。
本题难度:一般
3、填空题 按下图所示装置进行实验,并回答下列问题:

(1)判断装置的名称:A池为____,B池为____。
(2)锌极为____极,电极反应式为____;铜极为_____极,电极反应式为__________ 、____________ ;石墨棒C1为____极,电极反应式为____;石墨棒C2附近发生的实验现象为________。
(3)当C2极析出224 mL气体(标准状况下),锌的质量变化为(增加或减少)__________g。CuSO4溶液的质量变化为(增加或减少)__________g。
参考答案:(1)原电池 ;电解池
(2)负; Zn-2e-==Zn2+ ;正 ;Cu2+ + 2e-==Cu ;阳 ;2Cl- - 2e- == Cl2↑ ;有无色气体产生;附近溶液出现红色
(3)减少0.65 ;增加0.01
本题解析:
本题难度:一般
4、选择题 有三个烧杯,分别盛有氯化铜,氯化钾和硝酸银三种溶液;均以Pt作电极,将它们串联在一起电解一定时间,测得电极增重总和2.8克,这时产生的有色气体与无色气体的物质的量之比为
A.4:1
B.1:1
C.4:3
D.3:4
参考答案:C?
本题解析:串联电路中,相同时间内各电极得或失的电子的物质的量相同,各电极上放出气体的物质的量之比为定值。不必注意电极增重是多少。只要判断出生成何种气体及生成该气体一定物质的量所得失电子的物质的量,就可以通过电子守恒,判断气体体积之比,第一个烧杯中放出Cl2,第二烧杯中放出Cl2和H2,第三烧杯中放出O2。在有1mol电子转移下,分别是0.5 mol,0.5mol,0.5mol和0.25mol。所以共放出有色气体0.5+0.5=1(mol)(Cl2),无色气体0.5+0.25=0.75(mol)(O2和H2)
本题难度:一般
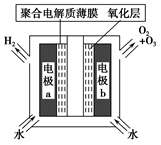
5、选择题 臭氧是常见的强氧化剂,广泛用于水处理系统。制取臭氧的方法很多,其中高压放电法和电解纯水 法原理如下图所示,下列有关说法不正确的是
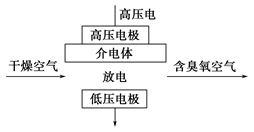 ?
?
A.高压放电法,反应的原理为3O2 2O3
2O3
B.高压放电出来的空气中,除含臭氧外还含有氮的氧化物
C.电解时,电极b周围发生的电极反应有3H2O-6e-=O3↑+6H+和2H2O-4e-=O2↑+4H+
D.电解时,H+由电极a经聚合固体电解质膜流向电极b
参考答案:D
本题解析:A、空气中含有氧气,在高压放电的条件下发生反应3O2 2O3,A正确;B、由于在放电的条件下氧气也与氮气化合生成NO,而NO可以被氧化生成NO2,所以高压放电出来的空气中,除含臭氧外还含有氮的氧化物,B正确;C、根据装置图可知,b电极生成氧气和臭氧,这说明b电极是阳极,水电离出的OH-放电,电极反应式为3H2O-6e-=O3↑+6H+和2H2O-4e-=O2↑+4H+,C正确;D、a电极是阴极,水电离出的氢离子放电生成氢气,所以电解时,H+由电极b经聚合固体电解质膜流向电极a,D不正确,答案选D。
2O3,A正确;B、由于在放电的条件下氧气也与氮气化合生成NO,而NO可以被氧化生成NO2,所以高压放电出来的空气中,除含臭氧外还含有氮的氧化物,B正确;C、根据装置图可知,b电极生成氧气和臭氧,这说明b电极是阳极,水电离出的OH-放电,电极反应式为3H2O-6e-=O3↑+6H+和2H2O-4e-=O2↑+4H+,C正确;D、a电极是阴极,水电离出的氢离子放电生成氢气,所以电解时,H+由电极b经聚合固体电解质膜流向电极a,D不正确,答案选D。
本题难度:一般