微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、计算题 (4分)(1)密度为1.17g/cm3,浓度为36.5%的浓盐 酸中HCl的物质的量的浓度为?。
酸中HCl的物质的量的浓度为?。
(2)Na2O和Na2O2的混合物14g和足量的水反应,得到300mL溶液,其中含溶质16g。原混合物中Na2O和Na2O2的质量分别多少?。
参考答案:(1)11.7mol/L? (2分,单位漏写扣1分)(2)? Na2O 6.2g,Na2O2 7.8g。(各1分)
本题解析:略
本题难度:一般
2、选择题 (1)5.4克H2O含有 molH。
(2)3.01×1024个OH―与 molNH3的质量相同。
(3)15.6 g Na2X中含Na+ 0.4mol,则X的相对原子质量是 。
(4)3.6g重水2H2O含电子物质的量为 。
(5)在一定温度和压强下,3L气体A2跟9L体积的气体B2完全化合生成6L体积某气体C,则该气体C的化学式为(用A、B表示) 。
参考答案:(1)0.6mol (2)5mol (3) 32 (4)1.8mol (5)AB3或B3A
本题解析:(1)5.4/18*2="0.6" (2)3.01×1024/6.02×1023=5mol,因二者摩尔质量相同,答案为5mol。(3)15.6/0.2-46=32 (4) 3.6/20*10=1.8mol (5) 同温同压下,气体的体积之比等于物质的量之比。利用原子守恒即可推出。
考点:物质的量的基本计算。
本题难度:一般
3、填空题 合成氨工业生产中所用的α?Fe催化剂的主要成分是FeO、Fe2O3。
(1)某FeO、Fe2O3混合物中,铁、氧的物质的量之比为4∶5,其中Fe2+与Fe3+物质的量之比为________。
(2)当催化剂中Fe2+与Fe3+的物质的量之比为1∶2时,其催化活性最高,此时铁的氧化物混合物中铁的质量分数为________(用小数表示,保留2位小数)。
(3)以Fe2O3为原料制备上述催化剂,可向其中加入适量碳粉,发生如下反应:2Fe2O3+C 4FeO+CO2↑。
4FeO+CO2↑。
参考答案:(1)1∶1 (2)0.72 (3)6
本题解析:(1)设Fe2+的物质的量为x,根据化合价代数和为0的原则:2x+(4-x)×3=5×2,x=2? mol,故Fe3+的物质的量也为2? mol。Fe2+与Fe3+的物质的量之比为1∶1。
(2)设催化剂中含1? mol Fe2+、2? mol Fe3+,根据化合价代数和为0,可知催化剂中氧原子的物质的量为1 mol+3 mol=4? mol。催化剂中铁的质量分数为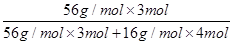 ≈0.72。
≈0.72。
(3)由题意知,被还原的Fe2O3与未被还原的Fe2O3的物质的量之比为1∶2,被还原的Fe2O3的物质的量为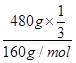 =1? mol,则:
=1? mol,则:
2Fe2O3 + C=4FeO+CO2↑
2? mol? 12 g
1? mol? m(C)
m(C)=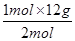 =6 g。
=6 g。
本题难度:一般
4、选择题 下列叙述中正确的是
A.硝酸的摩尔质量63g
B.1mol CO的体积约为22.4L
C.2g氢气所含原子数目为1mol
D.铁的摩尔质量在数值上等于铁原子的相对原子质量