| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点大全《物质的量》在线测试(2017年最新版)(十)
参考答案:D 本题解析:A. 标准状况下,1.12L氦气的物质的量为0.05moL,氦气是单原子分子,所含原子数为0.05NA,A错误;B. NH2―是10电子、9质子微粒,所含质子数为(1.6/16)x9NA=0.9NA,B错误;C.没有注明条件,无法计算物质的量,C错误;D.9g D2O所含的中子数为(9/20)x10NA=4.5NA,D正确;选D。 本题难度:一般 2、选择题 用NA表示阿伏加德罗常数,下列叙述中不正确的是 ( ) |
参考答案:D
本题解析:A正确,在标准状况下,NA个甲基(―CH3)和NA个羟基(―OH)所含电子数相等均有9NA个电子;B正确,铁与氯气反应生成氯化铁,+3价铁;C正确,NaHSO4和KHSO3的相对分子质量相同为120,且分子中均含有一个S原子,所以,120g由NaHSO4和KHSO3组成的混合物中含硫原子数目为NA;D错,1molCH3+中含有电子数为8NA
本题难度:一般
3、填空题 (1)1L?Na2SO4?溶液中,如果含钠元素的质量是2.3g,溶液中?SO42-物质的量浓度为______?mol/L.
(2)如果实验室没有?Na2SO4,可用?NaOH?和?H2SO4?反应配制?Na2SO4?溶液,从理论上计算,配制符合(1)的要求的?Na2SO4?溶液,需要NaOH的质量为______g?和?1.0mol/L硫酸溶液的体积为______?mL.(说明:按计算用量混合后,用蒸馏水稀释至1L?即可)
参考答案:(1)钠离子的物质的量=2.3g23g/mol=0.1mol,则钠离子的物质的量浓度=0.1mol1L=0.1mol/L,硫酸钠溶液中钠离子浓度与氯酸根离子浓度之比是2:1,所以SO42-物质的量浓度=0.1mol/L×0.5=0.05mol/L,
故答案为:0.05;
(2)根据钠离子守恒知,氢氧化钠的质量=2.3g23g/mol×40g/mol=4g,
根据硫酸根离子守恒得,硫酸的物质的量=0.1mol/L×0.5×1L1.0mol/L=0.05L=50mL,
故答案为:4,50.
本题解析:
本题难度:一般
4、选择题 下列示意图中,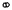 代表氢原子,
代表氢原子,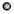 代表氦原子,方框代表容器,容器中间有一个可以上下滑动的隔板(其质量忽略不记)。其中能表示等质量的氢气与氦气的是
代表氦原子,方框代表容器,容器中间有一个可以上下滑动的隔板(其质量忽略不记)。其中能表示等质量的氢气与氦气的是
[? ]
A.
B.
C.
D.
参考答案:A
本题解析:
本题难度:一般
5、选择题 若NA表示阿伏加德罗常数,下列说法正确的是(? )
A.pH=1的硫酸溶液所含的H+数为NA个
B.20 g重水(D2O)中含有的电子数为10NA个
C.粗铜电解精炼时,阳极减少6.4 g,则转移电子数一定是0.2 NA个
D.在密闭容器中加入1molN2和3molH2充分反应可得到NH3分子数为2NA个
参考答案:B
本题解析:A不正确,因为溶液体积无法确定。C不正确,又因为粗铜中含有锌等活泼金属。D不正确,因为是可逆反应。答案选B。
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学必考知识点《配制一定物.. | |