| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学必考知识点《化学平衡状态的判断》考点预测(2017年强化版)(十)
(2)一定的条件下,合成氨反应为:N2(g)+3H2(g)  ?2NH3(g)。图1表示在此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。 ?2NH3(g)。图1表示在此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。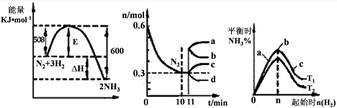 图1 ?图2?图3 ①该反应的平衡常数表达式为?,升高温度,平衡常数?(填“增大”或“减小”或“不变”)。 ②由图2信息,计算0~10min内该反应的平均速率v(H2)=?,从11min起其它条件不变,压缩容器的体积为1L,则n(N2)的变化曲线为?(填“a”或“b”或“c”或“d”) ③图3 a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是 ?点,温度T1?T2(填“>”或“=”或“<”) (3)若将等物质的量的SO2与NH3溶于水充分反应,所得溶液呈?性,所得溶液中c(H+)- c(OH-)=?(填写表达式)(已知:H2SO3:Ka1=1.7×10-2,Ka2=6.0×10-8,NH3・H2O:Kb=1.8×10-5) 参考答案:(1)①<?②B E? 本题解析:(1)①由图像可知:温度越高,平衡混合体系中SO3的百分含量越低。说明升高温度,化学平衡向逆反应方向移动。根据平衡移动原理:升高温度,化学平衡向吸热反应方向移动。逆反应方向为吸热反应,所以该反应的正反应为放热反应。因此△H<0.② A. 密闭容器的体积不变,所以任何时刻物质的密度都不会发生改变。错误。B. SO2与SO3的体积比保持不变,说明单位时间内SO2与SO3的物质的量不变,其浓度也不会发生改变,反应达到平衡状态。正确。C. 因为总质量不变,化学反应无论是否发生,也无论反应进行到什么时刻,都存在着体系中硫元素的质量百分含量不再变化。因此不能由此判断反应是否达到平衡状态。错误。D. 若转移4 mol 电子必然消耗2 mol SO3,但产生SO3的物质的量不能确定,所以不能判断反应是否达到平衡状态。错误。E. 由于该反应是个反应前后气体体积不等的可逆反应。若未达到平衡,则气体的分子数必然发生改变。现在容器内的气体分子总数不再变化。说明任何物质的消耗个数与生成个数相等。反应达到平衡状态。正确。因此正确选项为B、E。(2)①化学平衡常数是可逆反应达到平衡状态时各生成物的浓度幂指数的乘积与各反应物浓度浓度幂指数的乘积的比。该反应的平衡常数表达式为 本题难度:困难 2、选择题 对于反应2A(g)+B(g) 参考答案:AD 本题解析:此题考查含量(或浓度、转化率等)―温度―压强图象,解析此类题目时,关键是先固定一个量,再结合平衡移动原理讨论另外两个量的关系。首先要知道该反应是气体体积缩小的放热反应.此反应的平衡体系受压强的影响是:增大压强平衡向正反应方向移动,A的转化率增大,B的含量减小,C的含量增大.升高温度,平衡向逆反应方向移动,A的转化率减小,B的含量增大,C的含量减小。A图象表示B的含量随温度升高而增加,则符合此反应。另外,从反应开始到建立平衡,温度越高,到达平衡的时间越短.由于该反应是放热反应,建立平衡后,温度越高,B的含量就应越多。同理推知A、D图象正确,符合上述平衡体系,B、C图象不符合题意。 本题难度:一般 3、选择题 下列关于化学反应的熵变的叙述正确的是 参考答案:C 本题解析:熵变与反应的方向有关,但不能独立地作为自发性的判据,所以A项、B项、D项均错误。熵值增大的反应都是混乱度增大的反应,C项正确。 本题难度:简单 4、选择题 将4mol?A?气体和2mol?B?气体在2L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g)?2C(g)若经2s?后测得C的浓度为0.6mol/L,现有下列几种说法,其中正确的是( ) 参考答案:①用C表示的反应的平均速率为V=△C△t=0.6mol/L2s?=0.3mol/(L?s),因化学反应速率之比等化学计量数之比,所以用物质A表示的反应的平均速率为0.3mol/(L?s),故①正确; 本题解析: 本题难度:一般 5、选择题 在一恒温体积可变的密闭容器中发生如下反应:A(g)+B(g) 参考答案:C 本题解析: A、0~t1时,v正>v逆,t1~t2时,v正=v逆?;B、t2时刻改变的条件不可能是加催化剂,催化剂只改变速率,不改变平衡;D、化学平衡常数只跟温度有关,温度不变,化学平衡常数不变。 本题难度:一般 |
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学试题《有机化学反应类型.. | |