| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学必考知识点《化学平衡》试题巩固(2017年最新版)(十)
参考答案: 本题解析:略 本题难度:一般 3、选择题 恒温下在密闭容器中进行的反应2SO2 + O2 |
参考答案:D
本题解析:化学反应达到平衡状态的两个标志:各物质的浓度不再变化、同种物质的生成速率和消耗速率相等。A.容器中SO2、O2、SO3共存,这是可逆反应的基本特征,不能说明各物质的浓度不变,错;B.容器中SO2和SO3 浓度相同不能说明它们的浓度不再变化,错;C.容器中n(SO2)∶n(O2)∶n(SO3)=2∶1∶2 ,也不能说明物质的浓度不再变化,错;该反应是气体体积变化的反应,如果反应没有达到平衡,气体的物质的量会发生变化,压强也会发生变化,压强不变说明气体的生成和消耗相等,则反应达到了平衡,D对,选D。
考点:化学平衡状态的判断。
本题难度:一般
4、填空题 (1)CuCl2溶液有时呈黄色,有时呈黄绿色或蓝色,这是因为有CuCl2的水溶液中存在如下平衡: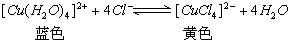 现欲使溶液由黄色变成黄绿色或蓝色,请写出两种可采用的方法:①___________,②________________。
现欲使溶液由黄色变成黄绿色或蓝色,请写出两种可采用的方法:①___________,②________________。
(2)在 的平衡体系中,加入18O构成氧气,当平衡发生移动后,SO2中18O的含量_________(填增加、减少或不变),其原因是__________。
的平衡体系中,加入18O构成氧气,当平衡发生移动后,SO2中18O的含量_________(填增加、减少或不变),其原因是__________。
参考答案:(1)加水 ;加入AgNO3溶液
(2)增加 ;在SO2与18O2反应生成S18O3的同时,又分解成S18O2。
本题解析:
本题难度:一般
5、填空题 (8分)化学学科中的平衡理论主要内容包括:化学平衡、电离平衡、水解平衡和溶解平衡等四种。且均符合勒夏特列原理。请回答下列问题。
(1)一定温度下,在一个固定容积的密闭容器中,可逆反应
A(g)+2B(g) 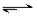 4C(g)
4C(g) 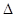 H >0 达到平衡时,c(A)="2mol/L," c(B)="7mol/L," c(C)=4mol/L。试确定B的起始浓度c(B)的取值范围是 ;若改变条件重新达到平衡后体系中C的体积分数增大,下列措施可行的是
H >0 达到平衡时,c(A)="2mol/L," c(B)="7mol/L," c(C)=4mol/L。试确定B的起始浓度c(B)的取值范围是 ;若改变条件重新达到平衡后体系中C的体积分数增大,下列措施可行的是
①增加C的物质的量 ②加 压 ③升温 ④使用催化剂
(2)常温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图所示。则图中表示醋酸溶液中pH变化曲线的是 (填“A”或“B”)。设盐酸中加入的Zn质量为m1,醋酸溶液中加入的Zn质量为m2。则m1 m2(选填“<”、“=”、“>”)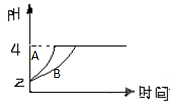
参考答案:(1)3mol/L<c(B)<9mol/L ③ (2)B;<
本题解析:(1)对于可逆反应来说,化学平衡的建立可以从反应物开始,可以从生成物开始,也可以从反应物、生成物同时开始;
①若平衡的建立是从反应物开始的,则根据“三段法”可求得B的起始浓度为9mol/L;
②若平衡的建立是从生成物开始的,则根据“三段法”可求得B的起始浓度为3mol/L;
若改变条件①增加C的物质的量,体系压强增大,则平衡向逆反应方向移动,C的体积分数减小;②加 压,则平衡向逆反应方向移动,C的体积分数减小;③升温,平衡向吸热反应方向移动,由于该反应的正反应为吸热反应,所以达到新的平衡后,C的体积分数增大;④使用催化剂,不影响平衡的移动,C的体积分数不变;
(2)醋酸为弱酸,加入Zn粒反应的过程中,醋酸要不断电离出氢离子,则盐酸是强酸,加入Zn粒反应的过程中不能再电离出氢离子,即醋酸溶液的PH变化更慢,所以,当溶液的PH均达到4时,消耗时间醋酸更长,所以图中表示醋酸溶液中pH变化曲线的是B,反应过程中消耗的Zn粒质量更多。
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点归纳《物质结构与.. | |