��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ijУ��չ�����о���ѧϰ���ӷϾɸɵ���л���̼����MnO2��NH4Cl��ZnCl2�����ʣ������������£��ش��й����⣺

��1����ͼ�Ǹɵ�صĻ�������ͼ���ɵ�ع���ʱ�����ϵķ�Ӧ��N
+e-=NH3��+H2�����ϵĵ缫��Ӧʽ��______��MnO2�������dz�ȥ�����ϵ�ij�����������Mn2O3���÷�Ӧ�Ļ�ѧ����ʽ��______��
��2��пƤ��̼���Ļ��գ���ǯ�Ӻͼ��Ӽ������յĸɵ�ص�пͲ����пƤ��̼��ȡ����ˢϴ�ɾ���������ڵĺ�ɫ��ĩ����С�ձ��У�
��3���Ȼ�李��Ȼ�п����ȡ������ͼ��飮����δӺ�ɫ��ĩ����ȡNH4Cl��ZnCl2�ľ������д����Ҫ��ʵ�鲽�裺______��
����ʲô�����ɽ�NH4Cl��ZnCl2�ľ���������뿪��______��
��д��֤��ZnCl2�����к�Zn2+�IJ������輰ʵ������______����֪Zn��OH��2�������������������ܽ��ڰ�ˮ��
�����ʣ��ĺ�ɫ��������Ҫ�ɷ���MnO2������̿�ں��л���ȣ��������յķ�����ȥ���ʣ���ʵ������Ҫ�õ�����Ҫ�������ƾ����⣬����______��
�ο��𰸣���1����п�̸ɵ���У����ý���пΪ��ظ�������ӦʽΪZn--2e-=Zn2+��MnO2����Mn2O3���ù����е�Mn���ϼ۽��ͣ�����ԭ����ԭ����������������������ӦʽΪ
2MnO2+H2=Mn2O3+H2O���ʴ�Ϊ��Zn--2e-=Zn2+��2MnO2+H2=Mn2O3+H2O��
��3���ٺ�ɫ��ĩ���п����Ե�NH4Cl��ZnCl2�����в�������Կ��Բ����ܽ⡢���ˡ��ᾧ�İ취�õ�ZnCl2��NH4Cl�Ļ���
�ʴ�Ϊ�����ɫ��ĩ�м���һ����������ˮ��ֽ����ܽ⣬���ˣ�����Һ����Ũ������ȴ�ᾧ���ٹ��ˣ����þ��弴ΪZnCl2��NH4Cl�Ļ���
��NH4Cl�����Ȳ��ȶ��ԣ������ȶ��Խ���ʱ�������ϻ��������Ȼ�泥���˿��Բ��ü��ȷ������ʴ�Ϊ���ӷ���
��Zn2+�в������ȵμ�ǿ���Ի���������Һ�����ȳ��ְ�ɫ������������ܽ⣬
�ʴ�Ϊ��ȡ����ZnCl2���Թ����ܽ⣬����Һƽ����Ϊ���ȷݣ��ֱ�μ�����NaOH��Һ�Ͱ�ˮ����֧�Թ��о�Ϊ�Ⱥ��ɫ�������ɣ���������ܽ⣻
�����ղ�����Ҫ������ת��������Ҫ����ǯ��������Ҫ���������żܻ�����̨����Ȧ�ϵ��������У����չ�����Ҫ�ò��������裬
�ʴ�Ϊ������������ǯ�����żܡ������ǡ���������
���������
�����Ѷȣ�һ��
2������� ���Ȼ��غ���������ԭ����������غ������������ϣ�����Ҫ�������£�
��֪�� ��Һ�ʼ��ԣ�30��������Һ��
��Һ�ʼ��ԣ�30��������Һ�� �����ֽ⡣
�����ֽ⡣

��1��д�� ��Һ�е������غ�___________________________________
��Һ�е������غ�___________________________________
��2��д��������I�з�Ӧ�Ļ�ѧ����ʽ_______________________���÷�Ӧ������Ƶķ�Ӧ������___________________________��
��3���������I��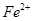 �����Ƿ���ȫ�ķ�����__________________________________��
�����Ƿ���ȫ�ķ�����__________________________________��
��4���ữ��Ŀ����___________________________��
��5���ڳ�����II�У�Ϊʹ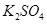 �����������õ����˲���������ʱ�õ�����Ҫ����������__________________________��
�����������õ����˲���������ʱ�õ�����Ҫ����������__________________________��
��6��N��P��K��S����ֲ�������������ҪԪ�ء���ҺA�������Ϸ��ϣ���Ϊ���к���___________��Ԫ�ء�
��7���й������ѧӦ�û�ѧ�о������Ҵ�ȼ�ϵ�ؼ���������ͻ�ƣ���װ�����Ժ�����ؼ�����ʽ��ѡ��Ҵ�ȼ�ϵ�صĹ���ԭ����ͼ��ʾ��
�ٸõ�ع���ʱ��c��ͨ�������Ϊ___________��
�ڸõ�ظ����ĵ缫��ӦʽΪ_____________________________________��

�ο��𰸣���1��[NH4+]+[NH3?H2O]=[CO32?]+[H2CO3]+[HCO3?] ��2�֣�
��2��2NH4HCO3 + FeSO4 = FeCO3��+ (NH4)2SO4 + CO2��+ H2O ��2�֣�����Ӧ�¶ȵ���30�� ��1�֣�
��3��ȡ�����آ����Һ���μ�KSCN��Һ��μ���ˮ������ɫ���֣�˵��������ȫ�����������ɣ���2�֣�
��4����ȥ��Һ�е�HCO3? ��2�֣�
��5����ͨ©�����ձ�����������2�� ��ȫ��1�֣���ͬ��
��6��K��S ��K?��2�֣�
��7��O2��1�֣���C2H6O �C 12e? + 3H2O = 2CO2 +12H+��2�֣�
�����������1�������غ��ʵ����Ԫ���غ㣬NH4HCO3��Һ��NԪ����CԪ�����ʵ�����ȣ�����[NH4+]+[NH3?H2O]=[CO32?]+[H2CO3]+[HCO3?]
��2��̼��������Ӻ���������֮�䷢��˫ˮ�ⷴӦ����̼���������������ų�������̼����Ӧ��ԭ������ʽΪ��2NH4HCO3+FeSO4=FeCO3��+��NH4?��2SO4+CO2��+H2O��Ϊ��ֹ�ϸ��¶���̼����淋ķֽ⣬Ҫע���¶ȵ�ѡ��Ӧ�¶ȵ���30�档
��3���������ӿ��Ա���������Ϊ���������ӣ�������������������ز���ɫ�������������������������ʾ��ɫ�����������I��Fe2+�����Ƿ���ȫ�ķ����ǣ�ȡ������I����Һ���μ�KSCN��Һ��μ���ˮ������ɫ���֣�˵��������ȫ��
��4�������آ��У��������ɵ�̼������֮�⣬��Һ���ܻẬ�й�����̼����泥������ᣬ�ữ��Ŀ���dz�ȥ��Һ�е�HCO3-��?
��5������Ŀ�����ڢ�Ӧ�����ɵ�K2SO4Ϊ���壬��K2SO4�����ܼ����ܽ���DZȽϴ�ģ�Ҫ��ʹK2SO4����ֻ�ܽ������ܽ�����Լ��봼���ܼ�Ŀ�Ľ���K2SO4���ܽ�ȡ�
��6����ҺA�ijɷ��к��У�NH4?��2SO4�Լ�KCl��������N��S��KԪ�أ����ڸ��Ϸ��ϡ�
��7������ͼ��H+�ƶ�����֪�Ҳ�缫Ϊȼ�ϵ�ص�����������c��ͨ�������ΪO2����ͼ��֪�������Һ�к�H+�������Ҵ���ˮ��Ӧ�����ݻ��ϼ۵ı仯��C2H5OHʧȥ12e?���ɵõ缫����ʽ��C2H6O �C 12e? + 3H2O = 2CO2 +12H+
�����Ѷȣ�һ��
3��ѡ���� ����˵������ȷ���ǣ�?����
A��ԭ����еĵ缫һ��Ҫ�����ֲ�ͬ�Ľ������
B��ԭ����е���������һ��������������������Ӧ
C��ԭ�������������������ԭ��Ӧ
D��ԭ������������������ƶ�
�ο��𰸣�D
�����������
�����Ѷȣ���
4��ѡ���� ������Ӧ��Zn+H2SO4=ZnSO4+H2����Ƴ�ԭ��أ�װ����ͼ����������˵����ȷ���ǣ�������
A��d��Һ��ϡ����
B��c��Һ��ɫ����
C��b������������Ӧ
D��a����ͭ��