| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点归纳《物质的量》高频试题强化练习(2017年最新版)(十)
参考答案:(1)②⑥⑦?(2)2.24?(3)加热或升华? 本题解析:(1)溶于水或在熔融状态下能够电离出离子的化合物是电解质,溶于水和在熔融状态下都不能够电离出离子的化合物是非电解质,据此可知,氨气、酒精是非电解质,碳酸钙、氢氧化钾和氯化氢是电解质,饱和食盐水是混合物,铜是单质,不是电解质也不是非电解质,答案选②⑥⑦。 本题难度:一般 2、选择题 下列关于阿佛加德罗常数的说法正确的是 |
参考答案:D
本题解析:A.0.1NA的NO与氧气反应后生成的NO2会自动化合成N2O4,导致得到的NO2小于0.1 mol,A项错误; B.SO2和氧气的反应是可逆反应,SO2不能完全转化成SO3,B项错误;C.铝在浓硫酸中发生钝化,因生成氧化膜阻止反应的继续进行,C项错误;D.水解反应是可逆的、微弱的过程,所以1 L 0.1 mol/L FeCl3溶液完全水解得到的Fe(OH)3胶体微粒数小于0.1 NA,D项正确;选D。
考点:考查阿伏伽德罗常数及计算。
本题难度:一般
3、选择题 现有铁粉与Fe2O3组成的混合物m g投入到足量的稀H2SO4中,在标准状况下收集到V L H2,所得溶液遇KSCN溶液不显红色,则混合物中Fe2O3的质量为
A.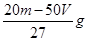
B.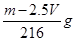
C.
D.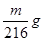
参考答案:A
本题解析:由题意知有关反应为:①Fe2O3+ 3H2SO4= Fe2(SO4)3+ 3H2O ②Fe + Fe2(SO4)3= 3FeSO4;③Fe + H2SO4?= FeSO4?+ H2?↑,?所得溶液遇KSCN溶液不显红色,则溶液中没有Fe3+,所得溶液为FeSO4溶液。?在标准状况下收集到VL H2,其物质的量是V/22.4mol,由反应③知与稀硫酸反应的铁为V/22.4mol质量为2.5Vg。由反应①、②知其余的铁与Fe2O3的物质的量之比是1:1。设Fe2O3、Fe的物质的量为x 160x+56x=m―2.5V解得x=(m―2.5V)/216(mol),Fe2O3的质量为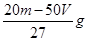
本题难度:一般
4、填空题 现有3.58gNa2CO3和NaHCO3的固体混合物,将其制成溶液后,边搅拌边逐滴滴加80.0ml 1.0mol/L 盐酸,反应完全后生成的CO2气体折算成标准状况下的体积为896ml(设气体全部逸出,下同)。回答下列问题:
(1)其中 过量。
(2)固体混合物中Na2CO3和NaHCO3的物质的量之比为 。
(3)取xg上述Na2CO3和NaHCO3的固体混合物,将其制成溶液后,边搅拌边逐滴滴加40.0ml 1.0mol/L 盐酸,反应完全后生成的CO2气体折算成标准状况下的体积为448ml,则x的值可能为 。
(4)取xg上述Na2CO3和NaHCO3的固体混合物,将其制成溶液后,边搅拌边逐滴滴加40.0ml 1.0mol/L 盐酸,反应完全后生成的CO2气体折算成标准状况下的体积为yml,当2.864≤x<14.32时,y与x的函数关系式是y= 。
参考答案:(1)盐酸(2)1:3 (3)1.79或7.16 (4)896-62.57x(或896-11200x/179)
本题解析:(1)相同质量的Na2CO3和NaHCO3,Na2CO3消耗的盐酸的量比较多,所以假设3.58g都为Na2CO3,则完全与盐酸反应,需要盐酸的物质的量n=3.58/106×2=0.0675mol,而80.0ml 1.0mol/L 盐酸中HCl的物质的量为0.08×1.0=0.08,所以盐酸过量;(2)设Na2CO3和NaHCO3的物质的量分别为a和b,则106a+84b=3.58,a+b=0.896/22.4,联立可以解得a=0.01mol,b=0.03mol,故固体混合物中Na2CO3和NaHCO3的物质的量之比为:1:3;(3)反应完全后生成的CO2气体折算成标准状况下的体积为448ml,即二氧化碳物质的量为0.448/22.4=0.02mol,所以有两种可能,一种是xg该混合物全部反应,即设xg中,Na2CO3和NaHCO3的物质的量分别为a和3a,则4a=0.02,所以a=0.005mol,即x=106×0.005+84×0.015=1.79g,第二种可能是盐酸不足量,则溶液中的溶质为氯化钠和碳酸氢钠,设该固体中Na2CO3和NaHCO3的物质的量分别为a和3a,根据钠元素和碳元素的守恒可以知道2a+3a=0.04×1+a+3a-0.02,即a=0.02,3a=0.06,所以x=106×0.02+84×0.06=7.16g;(4)取xg上述Na2CO3和NaHCO3的固体混合物,将其制成溶液后,边搅拌边逐滴滴加40.0ml 1.0mol/L 盐酸,盐酸的物质的量为0.04mol,设Na2CO3和NaHCO3的物质的量分别为a和3a,则x=106×a+84×3a=358a,所以a=x/358,当反应完全后生成的CO2气体折算成标准状况下的体积为yml,当2.864=x时,则盐酸刚好完全被消耗,生成的气体最多,随着x的量的不断增加,盐酸不足,即部分碳酸氢钠没有反应,生成的气体越来越少,知道x=14.32,不再生成气体,根据:
Na2CO3+HCl=NaHCO3+NaCl,可以知道该步反应消耗的盐酸为amol,生成了amol NaHCO3,所以NaHCO3的物质的量为4amol,而盐酸的物质的量剩下(0.04-a)mol,根据:
NaHCO3+HCl=CO2↑+H2O+NaCl可以知道生成CO2的物质的量为(0.04-a)mol,即y与x的函数关系式是y=(0.04-a)×22.4×1000=(0.04- x/358)×22.4×1000=896-11200x/179。
考点:碳酸盐与酸的反应
点评:本题考查了碳酸盐与酸的反应,本题题需要学生具有较强的分析能力,该题难度比较大。
本题难度:一般
5、选择题 同质量的下列气体中,所含原子数最少的是 (? )
A.CH4
B.CO2
C.H2S
D.N2
参考答案:B
本题解析:考查物质的量的有关计算。设物质的质量都是m,则根据n=m/M和物质的化学式可知,选项A、B、C、D中所含有的原子的物质的量分别是(mol) 。又因为
。又因为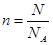 ,所以分子中含有的原子数最少的是CO2,答案选B。
,所以分子中含有的原子数最少的是CO2,答案选B。
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点归纳《原子的结构.. | |