| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
���л�ѧ֪ʶ����ɡ����ʵ�������Ƶ����ǿ����ϰ��2017�����°棩(��)
�ο��𰸣�C ���������A��5.6 gFe�����ʵ�����0.1mol�������������ᷴӦ�����Ȼ�����������������ת�Ƶ��ӵ���Ŀ��0.2NA������B��1������������2�������Ӻ�1�����������ӹ��ɣ�����1mol���������к�������������3NA������C�����ݰ���٤�����ɣ���״����22.4L���������������ʵ�����1mol�����Ժ��еķ�������NA����ȷ��D���Ȼ�þ��Һ�����δ֪�����������ӵ���Ŀ�����㣬����ѡC�� �����Ѷȣ�һ�� 2������� ��.������Ԫ��R����Ϊ������Ԫ�ء���RԪ�ص���۸��������Ӧ��ˮ������������̬�⻯�ﻯ��������A��д������A�Ļ�ѧ����ʽ?�� �ο��𰸣���10�֣� �����������.?RΪNԪ�أ�����۸��������Ӧ��ˮ����ΪHNO3���⻯��ΪNH3����Ӧ����A�Ļ�ѧ����ʽΪNH3+HNO3==NH4NO3�� �����Ѷȣ�һ�� 3��ѡ���� ij�������Һ�к���0.2 mol Na+��0.25 mol Mg2+��0.4 mol Cl����x mol SO42������xΪ �ο��𰸣�D ���������������Һ�ǵ����Եģ���0.2mol��0.25mol��2��0.4mol��2x�����x��0.15mol����ѡD�� �����Ѷȣ�һ�� 4��ѡ���� ʵ������2mol/L��Na2CO3��Һ950mL������ʱӦѡ�õ�����ƿ�Ĺ��ͳ�ȡ������Na2CO3�ֱ�Ϊ�������� �ο��𰸣�A ��������� �����Ѷȣ��� 5��ѡ���� 300 mL Al2(SO4)3��Һ�У���Al3��Ϊ1.62 g���ڸ���Һ�м���0.1 mol/L Ba(OH)2��Һ300 mL����Ӧ����Һ��SO�����ʵ���Ũ��Ϊ(����) |
�ο��𰸣�D
��������������ӵ����ʵ�����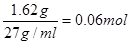 ������SO42�������ʵ�����0.09mol���������������ʵ�����0.03mol����˷�Ӧ��ʣ��SO42�������ʵ�����0.06mol����Ũ����
������SO42�������ʵ�����0.09mol���������������ʵ�����0.03mol����˷�Ӧ��ʣ��SO42�������ʵ�����0.06mol����Ũ����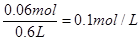 ����ѡD��
����ѡD��
�����Ѷȣ�һ��
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ���߿���ѧ֪ʶ����ɡ�ԭ�ӵĽṹ.. | |
| �����Ŀ |