��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��ͼ��ʾ����ѧ��ѧ�ﳣ��������A��L��ķ�Ӧ��ϵ������A��H��E��FΪ������E��FΪ���壬B�ڳ���������ɫҺ�壬C�ǵ���ɫ���壬L�Ǻ��ɫ���塣
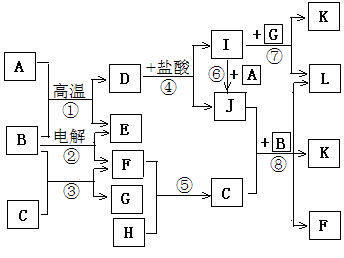
�����ͼʾ�жϲ��ش��������⣺
��1������A������Ԫ�������ڱ��е�λ����?��
��2����Ӧ�۵Ļ�ѧ����ʽΪ?��
��3����Ӧ�ܵ����ӷ���ʽΪ?��
��4����Ӧ������ӷ���ʽΪ?��
��5����Ӧ�ڷ��������У�����3��01��1024�����ӷ���ת��ʱ�������������B������Ϊ?g��ͬʱ�������ɵ���������Ϊ?L������Ϊ��״���µ��������
�ο��𰸣���1���������ڢ��壨2�֣�
��2��2Na2O2+2H2O=4NaOH+O2����3�֣�
��3��Fe3O4+8H+=Fe2++2Fe3++4H2O��3�֣�
��4��4Na2O2+4Fe2++6H2O=8Na++4Fe��OH��3��+ O2����3�֣�
��5��45��2�֣���56��2�֣�
�������������ͻ�Ƶ�����B�ڳ���������ɫҺ�壬��BΪ˭��CΪ����ɫ���壬����ˮ��Ӧ����G��Һ��F���嵥�ʣ���CΪNa2O2��GΪNaOH��FΪO2��LΪ���ɫ���壬ΪFe(OH)3����D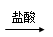 I��Һ��֪IΪFeCl3��JΪFeCl2��AΪ���������Ӷ������Ƶ����������ʷֱ�Ϊ��AΪFe��BΪH2O��CΪNa2O2��DΪFe3O4��EΪH2��FΪO2��GΪNaOH��HΪNa��IΪFeCl3��JΪFeCl2��KΪNaCl����1������AΪ����Fe����Ԫ�����ڱ���λ��Ϊ�������ڢ��塣��2����Ӧ��Ϊˮ��������Ƶķ�Ӧ�����ӷ�Ӧ����ʽΪ2Na2O2+2H2O=4NaOH+O2����3����Ӧ�ܵķ�ӦΪ����������������ķ�Ӧ�������ӷ�Ӧ����ʽΪFe3O4+8H+=Fe2++2Fe3++4H2O����4����Ӧ��Ϊˮ��������ƺ��Ȼ������ķ�Ӧ�����ӷ�Ӧ����ʽΪ4Na2O2+4Fe2++6H2O=8Na++4Fe(OH)3��+ O2��(5)��Ӧ��Ϊ���ˮ�ķ�Ӧ����Ӧ����ʽΪ2H2O
I��Һ��֪IΪFeCl3��JΪFeCl2��AΪ���������Ӷ������Ƶ����������ʷֱ�Ϊ��AΪFe��BΪH2O��CΪNa2O2��DΪFe3O4��EΪH2��FΪO2��GΪNaOH��HΪNa��IΪFeCl3��JΪFeCl2��KΪNaCl����1������AΪ����Fe����Ԫ�����ڱ���λ��Ϊ�������ڢ��塣��2����Ӧ��Ϊˮ��������Ƶķ�Ӧ�����ӷ�Ӧ����ʽΪ2Na2O2+2H2O=4NaOH+O2����3����Ӧ�ܵķ�ӦΪ����������������ķ�Ӧ�������ӷ�Ӧ����ʽΪFe3O4+8H+=Fe2++2Fe3++4H2O����4����Ӧ��Ϊˮ��������ƺ��Ȼ������ķ�Ӧ�����ӷ�Ӧ����ʽΪ4Na2O2+4Fe2++6H2O=8Na++4Fe(OH)3��+ O2��(5)��Ӧ��Ϊ���ˮ�ķ�Ӧ����Ӧ����ʽΪ2H2O 2H2��+O2��������3.01��1024�����ӷ���ת��ʱ��2.5molˮ����⣬����45gˮ�����ġ��������ɵ�����Ϊ�������Ҳ�������������ˮ�����ʵ�����ȣ���Ϊ2.5mol����ת�������Ϊ22.4L/mol��2.5mol=56L��
2H2��+O2��������3.01��1024�����ӷ���ת��ʱ��2.5molˮ����⣬����45gˮ�����ġ��������ɵ�����Ϊ�������Ҳ�������������ˮ�����ʵ�����ȣ���Ϊ2.5mol����ת�������Ϊ22.4L/mol��2.5mol=56L��
�����Ѷȣ�����
2��ѡ���� ����������������Һ��Ӧ����Ӧ�����ӷ���ʽ��ȷ����
A��0.2mol������300mL1mol/L������������Һ���
2Al3����3SO42����3Ba2����6OH����2Al(OH) 3����3BaSO4��
B��0.2mol������200mL1mol/L������������Һ���
Al3����SO42����Ba2����4OH����AlO2����BaSO4����2H2O
C��һ����������������ȫ��Ӧ�������ɳ������ʵ�������
Al3����2SO42����2Ba2����4OH����AlO2����2BaSO4����2H2O
D��һ������������Һ�м�������������Һ�����ɳ������ʵ������