微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法不正确的是
[? ]
A.共价化合物和离子化合物中,一定都含有非金属元素
B.一个化学反应的过程,本质上就是旧化学键断裂和新化学键形成的过程
C.全部由非金属构成的化合物一定不存在离子键
D.共价化合物都是由分子构成的,而离子化合物中一般不存在单个分子
参考答案:C
本题解析:
本题难度:简单
2、填空题 已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增大。其中A原子核外有三个未成对电子;A与B可形成离子化合物B3A2;C元素是地壳中含量最高的金属元素;D原予核外的M层中有两对成对电子;E原子核外最外层只有1个电子,其余各层电子均充满。请根据以上信息,回答下列问题:? (答题时,A、B、C、D、E用所对应的元素符号表示)
(1)E的核外电子排布式是?,A、B、C、D的第一电离能由小到大的顺序为?。
(2)B的氯化物的熔点远高于C的氯化物的熔点,理由是?;
(3)A的最高价含氧酸根离子中,其中心原子采取?杂化,D的低价氧化物分子的空间构型是?。
(4)A、E形成某种化合物的晶胞结构如下图所示,则其化学式为?;(每个球均表示1个原子)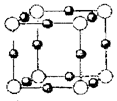
参考答案:(1)1s22s22p63s23p63d104s1(或[Ar] 3d104 s1)? A1<Mg<S<N
(2)MgCl2为离子晶体而A1C13为分子晶体? (3)sp2,V形? (4)Cu3N
本题解析:根据元素的结构及有关性质可知,A、B、C、D、E分别是N、Mg、Al、S、Cu。
(1)根据构造原理可知,铜原子的核外电子排布式是1s22s22p63s23p63d104s1(或[Ar] 3d104 s1) ;非金属性越强,第一电离能越大,所以四种元素的第一电离能大小顺序是A1<Mg<S<N。
(2)由于MgCl2为离子晶体,而A1C13为分子晶体,所以前者的熔点远高于后者。
(3)NO3-中氮原子能源孤对电子,所以其结构是平面三角形结构,氮原子是sp2杂化。由于SO2分子中,S原子含有2对孤对电子,所以SO2是V形结构。
(4)根据晶胞的结构可知,含有的氮原子是8×1.8=1,而含有的铜原子是12×1/4=3,所以该化合物的化学式是Cu3N。
本题难度:一般
3、简答题 现有部分短周期元素的性质或原子结构如下表:
| 元素编号 | 元素性质或原子结构
X
最外层电子数是次外层电子数的3倍
Y
常温下单质为双原子分子,其氢化物水溶液呈碱性
Z
第三周期元素的简单离子中半径最小
|
(1)元素X的一种单质在生活中常用作饮水机的消毒剂,该单质的化学式是______,元素Z的离子结构示意图为______.
(2)元素Y与氢元素形成一种离子YH4+,请写出检验溶液中存在该离子的实验操作、现象和结论______.
(3)写出Z元素最高价氧化物对应的水化物与NaOH溶液反应的离子方程式为______.
(4)元素X与元素Y相比,非金属性较强的是______(用元素符号表示),下列表述中能证明这一事实的是______.
a.Y的氢化物可在纯X2中燃烧生成X的氢化物和Y2
b.?X的单质比Y的单质更容易与H2?化合
c.X与Y形成的化合物中Y元素呈正价态.
参考答案:短周期元素中,最外层电子数是次外层电子数的3倍,即第一层电子数为2,第二层电子数为6,则X为氧元素;常温下单质为双原子分子,其氢化物水溶液呈碱性,即氢化物为氨气,则Y为氮元素;第三周期元素的简单离子中半径最小,阴离子的半径大于阳离子的半径,金属离子中原子序数越大的半径最小,则Z为铝元素;
(1)因氧元素的单质臭氧具有强氧化性,则可在生活中常用作饮水机的消毒剂,铝离子的质子数为13,核外电子数为10,其结构示意图为
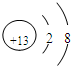
,
故答案为:O3;
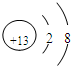
;
(2)因铵根离子能与碱反应生成氨气,且氨气能使湿润的红色石蕊试纸变蓝,故答案为:取少量溶液(或待测液)于试管中,滴加适量浓NaOH溶液后加热,将湿润的红色石蕊试纸沾在玻璃棒上靠近试管口部,若试纸变蓝,说明溶液中存在该离子,反之,不存在该离子;
(3)Z元素最高价氧化物对应的水化物,Al(OH)3与NaOH的反应为Al(OH)3+NaOH=NaAlO2+2H2O,离子反应为Al(OH)3+OH-=AlO2-+2H2O,
故答案为:Al(OH)3+OH-=AlO2-+2H2O;?
(4)因N、O元素处于同周期,同周期随原子序数的增大,非金属在增强,故O元素的非金属强,a中的氧化还原反应可判断氧气的氧化性大于氮气的氧化性,则氧的非金属性大于氮元素的非金属性,b中与氢气的化合的难易程度可知氧的非金属性强,c中氧比氮元素容易得到电子,则氧的非金属强,故答案为:O;a,b,c.
本题解析:
本题难度:一般
4、简答题 下列说法正确的是( )
A.非金属元素组成的化合物一定是共价化合物
B.离子化合物的熔点一定比共价化合物的高
C.元素周期律是元素的性质随元素相对原子质量的递增发生周期性递变的规律
D.含有阴离子的化合物一定含有阳离子
参考答案:A.只含共价键的化合物是共价化合物,由非金属元素组成的化合物不一定是共价化合物,如NH4Cl是离子化合物,故A错误;
B.离子化合物的熔点不一定比共价化合物的高,如氯化钠的熔点小于二氧化硅的熔点,故B错误;
C.结构决定其性质,所以元素周期律是元素的性质随元素原子核外电子排布周期性变化的必然结果,故C错误;
D.金属晶体中有金属阳离子,但没有阴离子,离子晶体中有阳离子,必定有阴离子,故D正确;
故选D.
本题解析:
本题难度:一般
5、选择题 下列各种元素的原子序数,期中能组成化学式为XY2型离子化合物的是( )
A.6和8
B.16和8
C.12和17
D.11和16
参考答案:C
本题解析:
本题难度:一般