| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
���л�ѧ֪ʶ����ɡ���ѧ��Ӧ���ʡ���Ƶ����Ԥ�⣨2017�����°棩(��)
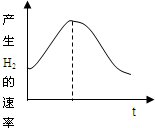 �ο��𰸣���ͼ�����������ķ�Ӧ������������С�������ķ�ӦΪMg+2H+�TMg2++H2���� ��������� �����Ѷȣ��� 2������� ijѧ����0.1��10��25�L3������������99.5%����Ƭ���ᷴӦ��ȡH2��ʵ��������±���
��2����Ӧ1-15min�ڣ���������ķ�Ӧ�����ӿ죬��ԭ����______�� ��3��������Ƭ����������ᷴӦ����IJ��죬����˼�������������²��룺 ����һ��______���������______�� �ο��𰸣���1����Ƭ���ᷴӦ2Al+6HCl=2AlCl3+3H2�������ӷ���ʽΪ��2Al+6H+�T2Al3++3H2�����ʴ�Ϊ��2Al+6H+�T2Al3++3H2����? ��������� �����Ѷȣ�һ�� 3������� �±���������ij�����£�����þ�����ֱ��������н���������Ӧʱ���ڽ�����������������Ĥ��ʵ���¼��
������������⣺ ��1����������������ʴ���ʿ����ý�������Ĥ��������������ʾ���������ǣ�__________ _______________________________________________________________________________�� ��2����������Ĥ��Ĥ��Y��ʱ��t�����ֵĹ�ϵ���ͣ�MgO����Ĥ��Y��t��___________�ͣ�NiO����ĤY����t��______________�ͣ��ֱ�ߡ��������ߡ�����������˫���ߡ������ͣ��� ��3��Mg��Ni�Ƚϣ���һ�ֽ������и����õ���������ʴ�ԣ�________________���������ǣ� _______________________________________________________________________________�� �ο��𰸣���1����Ӧ���ʿ����÷�Ӧ����������ʣ�Ҳ�����ò����������������ʾ �����������������������Ӧ����ƻ��dz�����һ������Ȼ������ͬ�Ľ����γɵ�����Ĥ���̶ܳȲ�ͬ�����ǵ���ʴ��Ҳ��ͬ����ѧ��Ӧ�Ŀ������ȿ����÷�Ӧ����������ʣ�Ҳ���ò����������������ʾ���ʽ�����ʴ���ʿ�����������Ĥ��������������ʾ���������б������ݣ��ɵ������¹�ϵʽ�� �����Ѷȣ��� 4��ѡ���� һ���������������п�۷�Ӧʱ��Ϊ�˼�����Ӧ���ʵ��ֲ�Ӱ������H2���������ɲ�ȡ�Ĵ�ʩ�ǣ������� �ο��𰸣�A����������NaOH��Һ��Ӧ���ᵼ�����������������٣���A��ѡ�� ��������� �����Ѷȣ�һ�� 5��ѡ���� ���ڷ�Ӧ2SO2(g)��O2(g) �ο��𰸣�A ��������� �����Ѷȣ�һ�� | ||||||||||||||||||||||||||||||
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ���߿���ѧ֪ʶ����ɡ�����ˮ���.. | |
| �����Ŀ |