微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、推断题 A、B、C、D分别代表四种不同的短周期元素。A元素的原子最外层电子排布为ns1,B元素的原子价电子排布为ns2np2,C元素原子的最外层电子数是其电子层数的3倍,D元素原子的M电子层的p轨道中有3个电子。
(1)C原子的电子排布式为___________,若A元素的原子最外层电子排布为1s1,则按原子轨道的重叠方式,A 与C形成的化合物中的共价键属于_______键。
(2)若A元素的原子最外层电子排布为2s1,B元素的原子电子排布为3s23p2,元素A在元素周期表中的位置是___________,A、B、C、D四种元素的第一电离能由大到小的顺序是_______(用元素符号表示)。
(3)若A原子的最外层电子排布为4s1,B原子的价电排布为3s23p2,A在元素周期表中的位置是_______,A、B、C、D四种元素的第一电离能由大到小的顺序是______________(用元素符号表示)。
参考答案:(1)1s22s22p4;σ
(2)第2周期第IA族;O>P>Si>Li
(3)第4周期IA族;N>O>Si>K
本题解析:
本题难度:一般
2、填空题 按要求填空:
(1)碱金属元素原子半径最小的是______,它作为新一代绿色可充电池的材料,放电时它是电池的______?极(填“正”或“负”);卤族元素中原子最外层的电子数都是______个,在化学反应中它们容易得到______个电子.在卤族元素中非金属性最强的元素是______,其离子的结构示意图:______;
(2)为防止碳素钢菜刀生锈,使用后特别是切过咸菜后,应采取的简易措施是______;?生活中和生产上最常用的燃料里所含的主要元素有______,它们在燃烧后生成的化合物主要是______.
(3)相对分子质量为58的烷烃的分子式是______,它可能的结构简式是______、______
(4)已知某反应的各物质浓度数据如下:aA(g)+bB(g)

2C(g)
起始浓度(mol/L):1.5?1.0?0
2s末浓度(mol/L):0.9?0.8?0.4
则①a=______,b______.
②2S内B的反应速率=______.
③3s末上述反应达平衡时,C浓度为0.6mol/L,则A的转化率为______.
(5)(6分)丙烯通入溴水中褪色的化学方程式:______(反应类型:______)硝基苯生成的化学方程式:______(反应类型:______)
参考答案:(1)碱金属元素的原子,从上到下原子半径逐渐增大,原子半径最小的是金属锂,锂电池放电时,锂是电池的负极,卤族元素的原子,从上到下非金属性逐渐减弱,所以非金属性最强的元素是F,第ⅤⅡA元素称为卤族元素,最外层电子数是7在化学反应中它们容易得到1个电子,形成8电子稳定结构,故答案为:锂;负;7;1;氟;
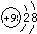
;
(2)铁生锈的原理是金属铁和水及空气接触,切过咸菜后的菜刀,防止生锈的简单做法是:立即将菜刀擦拭干净,生活中最常用的燃料是天然气,燃烧产物是水和二氧化碳,故答案为:立即将菜刀擦拭干净;C、H;CO2和H2O;
(3)烷烃具有通式:CnH2n+2,相对分子质量为14n+2,当相对分子质量为58时,所以n=4,即为丁烷,具有2种同分异构体:正丁烷和异丁烷,故答案为:C4H10;CH3-CH2-CH2-CH3;

;
(4)①A和B的浓度的变化量分别为:0.6mol/L和0.2mol/L,浓度的变化量之比等于方程式的系数之比,所以a=3,b=1,故答案为:3;1;
②2S内B的反应速率v=△ct=1.0mol/L-0.8mol/L2s=0.1mol/(L?S),故答案为:0.1mol/(L?S);
③3s末上述反应达平衡时,C浓度为0.6mol/L,则消耗的A的浓度为0.9mol/L,A的转化率=A的浓度或物质的量的变化量初始浓度或变化量×100%=0.9mol/L1.5mol/L×100%=60%,故答案为:60%;
(5)溴水和丙烯之间发生加成反应,原理是:
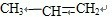
+Br2→
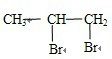
,属于加成反应,苯和浓硫酸以及浓硝酸的混合酸反应生成硝基苯,即

+HO-NO2浓硫酸
本题解析:
本题难度:一般
3、选择题 A、B两元素可形成AB型离子化合物,如果A、B两种离子的核外电子数之和为20,则A、B两元素所在的周期可以是
[? ]
A.两种元素在同一个周期
B.一种在第一周期,一种在第二周期
C.一种在第二周期,一种在第三周期
D.一种在第三周期,一种在第四周期
参考答案:C
本题解析:
本题难度:简单
4、选择题 元素性质呈周期性变化的决定因素是
[? ]
A.元素原子半径大小呈周期性变化
B.元素原子量依次递增
C.元素原子最外层电子排布呈周期性变化
D.元素的最高正化合价呈周期性变化
参考答案:C
本题解析:
本题难度:一般
5、填空题 在周期表中,同一主族元素化学性质相似。目前也发现有些元素的化学性质和它在周期表中左上方或右下方的另一主族元素性质相似,这称为对角线规则。据此请回答:
(1)锂在空气中燃烧,除生成_________外,也生成微量的_________。
(2)铍的最高价氧化物对应的水化物的化学式是_____________,属两性化合物,证明这一结论的有关离子方程式为________________;________________
(3)若已知反应Be2C+4H2O=2Be(OH)2+CH4↑,则Al4C3遇足量强碱溶液反应的离子方程式为_______________________________
(4)科学家证实,BeCl2属共价化合物,设计一个简单实验证明,其方法是________________________。
参考答案:(1)Li2O;Li3N
(2)Be(OH)2;Be(OH)2+2H+=Be2++2H2O、Be(OH)2+2OH-=BeO23-+2H2O
(3) Al4C3+4OH-+4H2O=4AlO2-+3CH4↑
(4)将BeCl2加热到熔融状态,如不能导电则证明BeCl2是共价化合物
本题解析:
本题难度:一般