| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点总结《电解池原理》高频试题特训(2017年最新版)(八)
参考答案:D 本题解析:A、电子沿 Zn→a,b→Cu 路径流动,a与b之间无电子流动,故A错误;B、铜电极上铜离子得电子发生还原反应,故B错误;C、甲池与乙池中的溶液互换,乙池中无法发生得电子反应,闭合K没有电流产生,故C错误;D、锌作负极,铜作正极,湿润的滤纸相当于电解池,滤纸上a作阴极,b作阳极,b上氢氧根离子放电,a上氢离子放电,所以a极附近氢氧根离子浓度增大,滤纸a点变红色,故D正确。 本题难度:一般 3、选择题 下图是模拟工业电解饱和食盐水的装置图, |
参考答案:
本题解析:
本题难度:一般
4、选择题 以铁为阳极,以铜为阴极,对足量的NaOH溶液进行电解。一段时间后得到2molFe(OH)3沉淀,此间共消耗的水的物质的量为
A.2mol
B.3mol
C.4mol
D.5mol
参考答案:D
本题解析:根据铁原子守恒知,2molFe(OH)3→2molFe(OH)2,所以生成2molFe(OH)3需要2molFe(OH)2;
活泼金属铁作电解池阳极时,电解氢氧化钠溶液的电解方程式为Fe+2H2O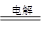 H2+Fe(OH)2↓,
H2+Fe(OH)2↓,
根据电解方程式得,生成2molFe(OH)2需要水的物质的量为4mol;
又氢氧化亚铁不稳定,能被氧气氧化成氢氧化铁沉淀,反应方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3,
根据方程式得,生成2molFe(OH)3需要水的物质的量为1mol,
所以得到2molFe(OH)3沉淀消耗水的物质的量共为5mol.故选D。
考点:电解池
点评:电解池是历年高考常考知识点,注重考查学生分析问题、解决问题的能力。近年来常以新型电解池进行考查。
本题难度:一般
5、选择题 某同学为了使反应2HCl+2Ag===2AgCl+H2↑能进行,设计了如图所示的四个实验,你认为可行的方案是( )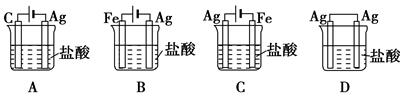
参考答案:C
本题解析:考查电解池的应用。银剩余不活泼的金属,和盐酸不能发生置换反应生成氢气。要是反应能够进行,则必须借助于电解,此时银和电源的正极相连,作阳极,所以选项C是正确的。答案选C。
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学必备知识点《原电池原理.. | |