��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��10�֣����ü�����������ȡ������Ŀǰ��Ϊ�Ƚ��ļ��������漰�ķ�Ӧ���£�
��CH4(g)��2H2O(g)��CO2(g)��4H2(g) ��H1����165.0 kJ/mol ��Ӧ���Ea1="243.9" kJ/mol
��CH4(g)��2O2(g)��CO2(g)��2H2O(g) ��H2����802.6 kJ/mol ��Ӧ���Ea2="125.6" kJ/mol
��1��2H2(g) + O2(g)= 2H2O(g)��H3�� kJ/mol��
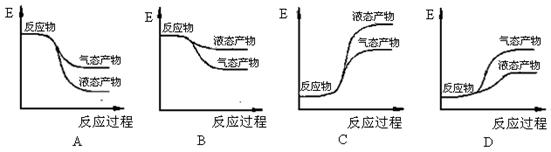
��2����������ȷ��ʾ������������Ӧ����ˮ�������仯ʾ��ͼ���� ������ĸ��ţ���
��3�����ü�����������ȡ������Ŀǰ��Ϊ�Ƚ��ļ�������ͬһ��Ӧϵͳͬʱͨ����顢������ˮ�������������Ϸ�Ӧ�ٺͷ�Ӧ�ڣ���Ӧ��ʼʱ����Ӧ�ٵķ�Ӧ���� ��Ӧ�ڵķ�Ӧ���ʣ���������������������������� ���������Ƕȷ������ڸ����������ͨ����������������Ӧ�ڵ�Ŀ���� ��
�ο��𰸣���1��-483.8 ��2�֣��� ��2��A ��2�֣�
��3������2�֣�����Ӧ�ٵĻ�ܱȷ�Ӧ�ڵĻ�ܸߣ���2�֣�
������������Ӧ���ȣ�Ϊ��Ӧ���ṩ����������2�֣�
�����������1���ɸ�˹���ɿ�֪��2H2(g) + O2(g)= 2H2O(g)��H3��-1/2��H1+1/2��H2="-483.8" kJ/mol����2��������������Ӧ����ˮΪ���ȷ�Ӧ���ʷ�Ӧ������������������������������̬ˮ��Һ̬ˮΪ���ȹ��̣���A����ȷ������ɿ�֪��Ӧ�ٵĻ�ܱȷ�Ӧ�ڵĻ�ܸߣ��ʷ�Ӧ�ٵķ�Ӧ����<��Ӧ�ڵķ�Ӧ���ʣ���Ӧ��Ϊ���ȣ���Ӧ��Ϊ���ȣ��ʴ������Ƕȷ������ڸ����������ͨ����������������Ӧ�ڵ�Ŀ���Ǽ�����������Ӧ���ȣ�Ϊ��Ӧ���ṩ����������
���㣺��ѧ��Ӧ�����仯��
�����Ѷȣ�����
2������� ��֪��Ӧ��Fe(s)+CO2(g) FeO(s)+CO(g) ��H=akJ��mol-1,ƽ�ⳣ��ΪK;
FeO(s)+CO(g) ��H=akJ��mol-1,ƽ�ⳣ��ΪK;
��Ӧ��CO(g)+1/2O2(g) CO2(g) ��H=bkJ��mol-1;
CO2(g) ��H=bkJ��mol-1;
��Ӧ��Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g) ��H=ckJ��mol-1������ڲ�ͬ�¶���,Kֵ����:
2Fe(s)+3CO2(g) ��H=ckJ��mol-1������ڲ�ͬ�¶���,Kֵ����:
�¶�/��
| 500
| 700
| 900
|
K
| 1.00
| 1.47
| 2.40
|
(1)��500 ��ʱ���з�Ӧ��,CO2����ʼŨ��Ϊ2 mol��L-1,CO��ƽ��Ũ��Ϊ ��(2)��Ӧ��Ϊ (ѡ����ȡ����ȡ�)��Ӧ��(3)700 ��ʱ��Ӧ�ٴﵽƽ��״̬,Ҫʹ��ƽ�������ƶ�,������������ʱ,���Բ�ȡ�Ĵ�ʩ�� (�����)��A.��С��Ӧ����� B.ͨ��CO2
C.�¶����ߵ�900 �� D.ʹ�ú��ʵĴ���
E.����Fe����
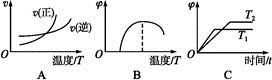
(4)����ͼ����Ϸ�Ӧ�ٵ��� (�����)(ͼ��vΪ����,��Ϊ�������CO����,TΪ�¶���T1>T2)��
(5)�ɷ�Ӧ�ٺ͢ڿ����,��Ӧ2Fe(s)+O2(g) 2FeO(s)�Ħ�H= ��
2FeO(s)�Ħ�H= ��
(6)�����ø�˹����д��Fe(����)��O2(����)�����õ�Fe2O3(����)���Ȼ�ѧ����ʽ: ��
�ο��𰸣�(1)1 mol��L-1 (2)���� (3)BC (4)A
(5)2(a+b) kJ��mol-1(6)2Fe(s)+3/2O2(g) Fe2O3(s)��H="(3b-c)" kJ��mol-1
Fe2O3(s)��H="(3b-c)" kJ��mol-1
�����������1����2�����ݷ�Ӧ��,��д���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽK=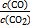 ,�ӱ������ݹ۲쵽:Kֵ���¶����߶�����,˵������ӦΪ���ȷ�Ӧ����500 ��ʱ,����CO2ת����x mol��L-1,�ﵽƽ��״̬ʱ,����ʽ����:K=
,�ӱ������ݹ۲쵽:Kֵ���¶����߶�����,˵������ӦΪ���ȷ�Ӧ����500 ��ʱ,����CO2ת����x mol��L-1,�ﵽƽ��״̬ʱ,����ʽ����:K=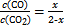 =1.00,���x=1,��ƽ��ʱCO��Ũ��Ϊ1 mol��L-1��
=1.00,���x=1,��ƽ��ʱCO��Ũ��Ϊ1 mol��L-1��
(3)��,700 ��ʱ��Ӧ�ٴﵽƽ��,Ҫʹ��ƽ�������ƶ�,����������ϵ�¶ȡ�����Ӧ��Ũ��(ͨ��CO2),ע�ⲻҪ��ѡѡ��E,��Ϊ��Ӧ��Fe�ǹ���,�ı�����Һ�������ƽ����Ӱ�졣
(4)��,ͼ��A���¶ȸı�Է�Ӧ���ʵ�Ӱ��,���ڷ�Ӧ�ٵ�����Ӧ�����ȷ�Ӧ,���������¶�,���淴Ӧ���ʾ�����,������Ӧ��������ķ��ȴ�,��A��ȷ��ͼ��B���¶ȸı�Ի������CO������Ӱ��,�¶Ƚϵ�ʱ��Ӧ������,�����¶����������CO�ĺ���������,�����С,��B����ͼ��C��T1>T2,�¶�����ƽ�������ƶ�,��CO�ĺ�����,��C����
(5)��,�ɷ�Ӧ�ٺ͢�,�������´���:��+��,�õ�:
Fe(s)+O2(g) FeO(s) ��H="(a+b)" kJ��mol-1,
FeO(s) ��H="(a+b)" kJ��mol-1,
�ʷ�Ӧ2Fe(s)+O2(g) 2FeO(s)�Ħ�H="2(a+b)" kJ��mol-1��
2FeO(s)�Ħ�H="2(a+b)" kJ��mol-1��
(6)��,�ɷ�Ӧ�ۺ͢�,�������´���:��-�ڡ�3,�õ�:
Fe2O3(s) 2Fe(s)+O2(g) ��H="(c-3b)" kJ��mol-1,
2Fe(s)+O2(g) ��H="(c-3b)" kJ��mol-1,
����Fe���屻O2�����õ�Fe2O3������Ȼ�ѧ����ʽΪ:
2Fe(s)+O2(g) Fe2O3(s) ��H="(3b-c)" kJ��mol-1��
Fe2O3(s) ��H="(3b-c)" kJ��mol-1��
�����Ѷȣ�����
3������� �ճ�����ˮ��NO3һ�ĺ�����ˮ�������������Ҫ��֮һ���ﵽһ��Ũ��ʱ������ཡ������Σ����Ϊ�˽�������ˮ��NO3һ��Ũ�ȣ�ij��ȤС��������·�����
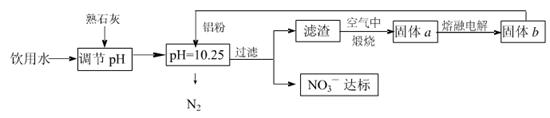
��ش��������⣺
��1���÷����ڵ���pHʱ����pH������С������� �������ʽ��͡�
��2����֪���˺�õ�����Һ�м���������Ԫ�ء�������Һ�����ۺ�NO3һ��Ӧ�����ӷ���ʽΪ ��
�������ڿ��������չ������漰����ط�Ӧ����ʽΪ
��3����H2����ԭ��Ҳ�ɽ�������ˮ��NO3����Ũ�ȣ���֪��Ӧ�еĻ�ԭ���������������ɲ������ѭ���������ԭ�������ӷ���ʽΪ ��
��4������ˮ�е�NO3�� ��Ҫ������NH4������֪�����������£�NH4�� ����������Ӧ��������NO3�� ��������Ӧ�������仯ʾ��ͼ���£�
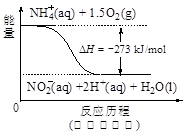
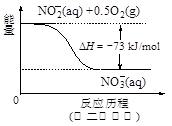
��д��1 mol NH4�� (aq)ȫ��������NO3�� (aq)���Ȼ�ѧ����ʽ�� ��
��5������a���ڵ��ʱ������ӦʽΪ
�ο��𰸣���1��������Al��(2��)
��2����10Al+6NO3��+18H2O��10Al(OH)3��+3N2��+6OH��(2��)
��4Al+ 3O2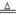 2 Al2 O3 2Al(OH)3
2 Al2 O3 2Al(OH)3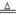 Al2 O3+3 H2O����2�֣�
Al2 O3+3 H2O����2�֣�
��3��5H2+2NO3�� N2��+4H2O+2OH�� (2��)
N2��+4H2O+2OH�� (2��)
����5H2+2NO3����2H�� N2��+6H2O��
N2��+6H2O��
��4��NH4�� (aq)��2O2(g)��2H��(aq)��NO3�� (aq)��H2O(l) ��H����346 kJ��mol��1(2��)
��5��Al3++3e-= Al��2�֣�
�����������1���������ܺ�����ܷ�Ӧ���÷����ڵ���pHʱ����pH������С�������������Al�� �������ʽ��͡���2������������������ӷ���������ԭ��Ӧ���ɹ��壬�����Ϊ���������������ᱻ��ԭΪ������������Һ�����ۺ�NO3
�����Ѷȣ�����
4��ѡ���� �����й��Ȼ�ѧ����ʽ�ı�ʾ��˵����ȷ���ǣ�������
A����֪c��ʯī��s��=c�����ʯ��s����H��0������ʯ��ʯī�ȶ�
B����֪H2��g��+F2��g���T2HF��g����H=-270kJ/mol����2L����������ֽ��1L������1L��������270kJ����
C��HCl��NaOH��Ӧ���к���Ϊ-57.3kJ/mol����H2SO4��Ba��oH��2��Ӧ���к��ȡ�H=2����-57.3��kJ/mol
D����֪I2��g��+H2��g���T2HI��g����H1��I2��s��+H2��g���T2HI��g����H2�����H1����H2
�ο��𰸣�D
���������
�����Ѷȣ�һ��
5��ѡ���� ��֪��C(s)��O2(g)===CO2(g) ��H1 CO2(g)��C(s)==="2CO(g)" ��H2
2CO(g)��O2(g)===2CO2(g) ��H3 4Fe(s)��3O2(g)===2Fe2O3(s) ��H4
3CO(g)��Fe2O3(s)===3CO2(g)��2Fe(s) ��H5
���й���������Ӧ�ʱ���ж���ȷ����
A����H1>0, ��H3<0
B����H2>0����H4>0
C����H1����H2����H3
D����H3����H4����H5