微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 常温下,往H2O2溶液中滴加少量FeSO4溶液,可发生如下两个反应:
2Fe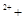 H2O2
H2O2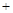 2H
2H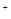 → 2Fe
→ 2Fe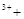 2H2O 2Fe
2H2O 2Fe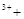 H2O2 → 2Fe
H2O2 → 2Fe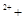 O2↑
O2↑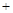 2H
2H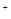
下列说法正确的是( )
A.H2O2的氧化性比Fe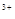 强,其还原性比Fe
强,其还原性比Fe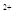 弱
弱
B.在H2O2分解过程中,溶液的pH逐渐下降
C.在H2O2分解过程中,Fe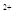 和Fe
和Fe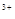 的总量保持不变
的总量保持不变
D.H2O2生产过程要严格避免混入Fe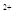
参考答案:CD
本题解析:首先要明确铁离子是起催化剂的作用,两个反应相加得2H2O2=2H2O+O2↑。因此在分解过程中H+的浓度不变,故溶液的pH不变。由于双氧水的量远大于亚铁离子,而且两个反应循环进行,故亚铁离子、铁离子的总量不变。在双氧水的生成中要避免其分解,故D的说法正确。对于A选项,第一个反应是在酸性条件下,得出的结论是正确的,但是第二个反应是在中性条件下进行的,得出的结论相反,故要比较其氧化还原性要指明反应条件的介质。答案选CD。
本题难度:一般
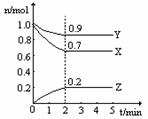
2、选择题 某温度时,2 L容器中三种物质的物质的量随时间的变化曲线如图所示。由图中数据分析,该反应的化学方程式和反应开始至2 min末Z的平均速率分别为
A.3X+Y 2Z; 0.05 mol/(L・min)
2Z; 0.05 mol/(L・min)
B.2X+Y 2Z; 0.1 mol/(L・min)
2Z; 0.1 mol/(L・min)
C.3X+Y 2Z; 0.1 mol/(L・min)
2Z; 0.1 mol/(L・min)
D.X+3Y 2Z; 0.05 mol/(L・min)
2Z; 0.05 mol/(L・min)
参考答案:A
本题解析:由图象可以看出,反应中X、Y的物质的量减少,应为反应物,Z的物质的量增多,应为生成物,当反应进行到3min时,△n(Y)=0.1mol,△n(Z)=0.2mol,△n(X)=0.3mol,
则△n(Y):△n(Z):△n(X)=1:2:3,参加反应的物质的物质的量之比等于化学计量数之比,则反应的方程式为:3X+Y 2Z,故答案为:3X+Y
2Z,故答案为:3X+Y 2Z;反应开始至2min末,Z的反应速率为:v=
2Z;反应开始至2min末,Z的反应速率为:v=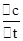 =
=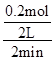 ="0." 05 mol/(L・min),故答案为:0. 05 mol/(L・min);选A
="0." 05 mol/(L・min),故答案为:0. 05 mol/(L・min);选A
本题难度:一般
3、选择题 下列变化能加快反应速率,且反应物活化分子百分数增加的是
①?升高温度 ②使用证催化剂? ③增大压强? ④增加浓度
A ②④? ?B? ③④?C? ①② ?D ②③
?B? ③④?C? ①② ?D ②③
参考答案:C
本题解析:略
本题难度:简单
4、选择题 对于反应:A+B=C下列条件的改变一定能使化学反应速率加快的是
[? ]
A.增加A的物质的量
B.升高体系的温度
C.增加体系的压强
D.减少C的物质的量浓度
参考答案:B
本题解析:
本题难度:一般
5、选择题 某温度下,体积一定的密闭容器中进行如下反应:2X(g)+Y(g)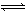 Z(g)+W(s) ΔH>0,下列叙述正确的是
Z(g)+W(s) ΔH>0,下列叙述正确的是
A.在容器中加入氩气,反应速率不变
B.加入少量W,逆反应速率增大
C.升高温度,正反应速率增大,逆反应速率减小
D.将容器的体积压缩,可增大单位体积内活化分子的百分数,有效碰撞次数增大
参考答案:A
本题解析:A、在容器中加入氩气,压强增大,但物质的浓度,所以反应速率不变,A正确;B、W是固体,所以加入少量W,正逆反应速率均不变,B不正确;C、升高温度,正逆反应速率均增大,C不正确;D、将容器的体积压缩,可增大单位体积内活化分子数,有效碰撞次数增大,反应速率加快,但单位体积内活化分子的百分数不变,D不正确,答案选A。
本题难度:一般