��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �й�����������������У�����ȷ����?
[? ]
A����������SO2��ˮ��Һ��������?
B��������ȶ������ֽ�Ϊˮ��SO2?
C�����������Ư���ԣ��ܹ�ʹƷ����Һ��ɫ
D��������������к���������SO2Ư����ʳƷ����ʳ��
�ο��𰸣�D
���������
�����Ѷȣ���
2������� ��1��ij��ѧ̽��С���SO2�Ļ�ѧ���ʽ�������̽����д����ʵ�鱨�森����������ʵ�鱨��
| ���� | ��� | ��ѧ��
��Ԥ�� | ʵ����֤���������Թܡ���ͷ�ιܣ�
ʵ�����
����
ʵ�ʣ����ӷ���ʽ��ʾ��
|
| SO2 | ����������
���Ժ�ˮ��Ӧ
��ʢ����������������Թܵ�����ˮ�У����ⶨ�Թ�����Һ��pH
SO2+H2O=H2SO3
��Ӧ
���ְ�ɫ����
|
��2����һ��ѧ̽��С�����SO2��SԪ�صĻ��ϼۣ�Ԥ�Ⲣͨ��ʵ��̽����֤��SO2���������ʣ�̽��������ѡ�õ�ʵ��ҩƷ��Ũ���ᡢNa2SO3���塢Na2S��Һ������KMnO4��Һ��Ʒ����Һ�ȣ�̽������ʵ��װ��ͼ���£�����ش��й�����
����������������
| װ�� | ҩƷ | ����
B
����KMnO4��Һ
��֤SO2�Ļ�ԭ��
C
D
|
��B�з�Ӧ�����ӷ���ʽΪ______��
��D�е�����Ϊ______��
�ο��𰸣���1�����������ˮ��Ӧ���������ᣬ�����Թ��������ѹǿ��С������ѹ���䣬�����Թ���ˮ�����������������ᣬ������ˮ��Һ��PHС��7����������ͳ����ʯ��ˮ��Ӧ���ɲ�����ˮ��������ƣ����ӷ���ʽΪSO2+Ca2++2OH-=CaSO3��+H2O��
�ʴ�Ϊ���Թ���ˮ������������ҺpH��7�����Թ��г���ˮ����Һ�����ԣ���
��SO2����ͨ�����ʯ��ˮ�У�SO2+Ca2++2OH-=CaSO3��+H2O��
��2���ٶ�����������Ԫ�صĻ��ϼ���+4�ۣ������м��̬��Ԥ����������������л�ԭ�ԣ�
���������ǿ�����ԣ��������������ʹ���������ɫ����֤���������л�ԭ�ԣ�
�����л�ԭ�ԣ����������������Ʒ�Ӧ����֤���������������ԣ�
�������������ʹƷ����Һ��ɫ�������ָֻ�ԭɫ����֤SO2ʹƷ����ɫ�Ŀ����ԣ�
�ʴ�Ϊ��
װ��ҩƷ̽��Ŀ��CNa2S��Һ��֤SO2��������DƷ����Һ��֤SO2ʹƷ����ɫ�Ŀ����Ԣڶ��������л�ԭ�ԣ���������������ԣ����������������ܷ���������ԭ��Ӧ��
���ӷ���ʽΪ5SO2+2MnO4-+2H2O�T2Mn2++5SO42-+4H+��
�ʴ�Ϊ��5SO2+2MnO4-+2H2O�T2Mn2++5SO42-+4H+��
�۶����������ɫ���ʷ�Ӧ������ɫ���ʣ����Ⱥ��ָֻ�ԭɫ�����Կ�����������ͨ��SO2����Ʒ����Һ��ɫ�������ձ�����Һ�ָֻ���ɫ��
�ʴ�Ϊ��ͨ��SO2����Ʒ����Һ��ɫ�������ձ�����Һ�ָֻ���ɫ��
���������
�����Ѷȣ�һ��
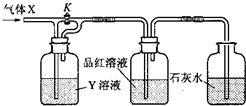
3��ѡ���� ������ʵ��װ�ã���ͼ����ͨ������X�����ر�K��ʱ��Ʒ����Һ����ɫ��ʯ��ˮ����ǣ�������K��ʱ��Ʒ����Һ��ɫ����X������Y��ҺӦ�ǣ�������
| A | B | C | D
X����
C12
SO2
CO2
HCl
Y��Һ
NaCl
NaHCO3
Na2SO3
NaHSO3
|
A��A
B��B
C��C
D��D