��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ijͬѧ�������е�Na2O2��CO2��Ӧ��֪ʶ����Ǩ�ƣ���ΪNa2O2Ҳ�ɺ�SO2��Ӧ����Ӧʽ����Ϊ2Na2O2+2SO2=2Na2SO3+O2��Ϊ���������һ��װ�ã�����֤Na2O2��SO2�ķ�Ӧ�����ͼ��װ���������װ�������Ժ�����ҩƷ����������Ũ���ᣬ�ش��������⣺

��1����ȼ�ٴ��ƾ��ƣ����ã��۲쵽�ٴ������������壻�۴���ͨ�ܹܱڷ��ȣ�����ҩƷ����ɫ�仯Ϊ______ɫ��Ϊ______ɫ��
��2���ڷ�Ӧ����������ýϼ��IJ���֤����Ӧ������O2��______��
��3��������ˮ���ռ����壬��ʲô�����֤���ռ����������Ѳ���SO2��______��
��4������Ӧ������ȡ��ͨ�����������壬װ���Թ��У���ˮ�ܽ�ʱδ�������壬���֤����������Na2SO3��______��
��5������Ӧ������ȡ��ͨ�����������壬װ���Թ��У���������������Һ���ټ����Ȼ�����Һ���а�ɫ�������ɣ��Է�������������ԭ��______��
�ο��𰸣���1��Na2O2Ϊ����ɫ���壬��Ӧ�����ɵ�Na2SO3��Na2SO4��Ϊ��ɫ���壮�ʴ𰸣�����ҩƷ����ɫ�仯Ϊ����ɫ��ɰ�ɫ
?��2������O2�ķ������ô��л��ǵ�ľ�����ʴ𰸣��ô����ǵ�ľ���������ˮ����Ϸ�����ľ����ȼ����֤����Ӧ������O2?
?��3������SO2�ķ�������Ʒ����Һ���ʴ𰸣��ݴ�Ʒ����Һ����ɫ��˵�������в����ж�������
? ��4������ķ���ͨ��Ϊ�����ᣬ��������������ʣ��ʴ𰸣��������ᣬ���д̼�����ζ�������ݳ�����֤�������к���Na2SO3?
? ��5�����������������ԣ�����SO2��Ӧ��Na2O2+SO2�TNa2SO4���ʴ𰸣����ڹ��������������ԣ���Ӧ�������в����������Ʊ�����ΪNa2SO4��BaCl2��Ӧ���������������BaSO4
���������
�����Ѷȣ�һ��
2������� Ŀǰ�ⶨ������SO2������Ҫ��������ԭ��Ӧ����֪SO2����������KMnO4��Һ��Ӧʱ��MnO4-?����ԭΪMn2+��SO2��������SO42-��
Ϊ�ⶨij�ط��Ŀ�����SO2�Ϳ���������ĺ�������ͬѧ�������ͼ��ʾ��ʵ��װ�ã�

������

��

��ʾ�ܱ�������
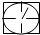
?��ʾ�������ٹܣ���λʱ����ͨ�����������㶨���������������������ã���

��ʾ���������������������տ�����Ŀ���������ʾ���������
������KMnO4��Һ���Ϊ200mL��Ũ��Ϊ0.1mol?L-1���ش��������⣺
��1������200mL0.1mol?L-1����KMnO4��Һ�����õ���������ʹ�õ��Ⱥ�˳��������______����������______��______��______����������������______��
��2��д������ƽ�ⶨSO2���������ӷ���ʽ��______
��3�����������ٹ�����������Ϊacm3/min����tminʱ����KMnO4��Һǡ����ɫ���������SO2�ĺ���Ϊ______��g/cm3����
��4��ʵ��������������______��
��Ҫ�ⶨ�����п���������ĺ�����g/L��������Ҫ�����������______
��5����ͬѧ����ͬ���ķ�������������SO2�ĺ���������õ���ֵ���DZ�ʵ�ʺ���ƫ�ͣ�����ܵ�ԭ���ǣ�������Һ���ơ���������ȡ�����ֶ���������______��
�ο��𰸣���1������200mL0.1mol?L-1����KMnO4��Һ������ʵ����û��200mL����ƿ��Ӧ��250mL����ƿ���ƣ�����������ƽ����������ع��壬���ձ��м�ˮ�ܽⲢ�ò��������裬��ȴ���ò�����ת��������ƿ�У�����������������������ˮ����Һ��̶���1��2cmʱ���ý�ͷ�ιܵμ����̶��ߣ�
�ʴ�Ϊ����ƽ���ձ���250mL����ƿ����ͷ�ιܣ������������
��2��SO2���л�ԭ�ԣ�������ؾ��������ԣ����߷���������ԭ��Ӧ����SO42-��Mn2+���ӣ�
��Ӧ�ķ���ʽΪ5SO2+2MnO4-+2H2O�T5SO42-+2Mn2++4H+��
�ʴ�Ϊ��5SO2+2MnO4-+2H2O�T5SO42-+2Mn2++4H+��
��3��������ص����ʵ���Ϊ0.2L��0.1moL/L=0.02moL��
���ݷ�Ӧ����ʽ5SO2+2MnO4-+2H2O�T5SO42-+2Mn2++4H+��
��֪atml�����к���SO2�����ʵ���Ϊ52��0.02mol=0.05mol��
����Ϊ0.05mol��64g/moL=3.2g��
���Կ�����SO2�ĺ���Ϊ3.2atg/cm3��
�ʴ�Ϊ��3.2at��
��4�������������ԣ������������еĿ�������ֹ������������������ܻ�������Ը��������Һ�У�ʹ��������������Ҫ�ⶨ�����п���������ĺ�����g/L��������Ҫ���������������ǰ�����������������ʢ����������������
�ʴ�Ϊ����ֹ������������������ܻ�������Ը��������Һ�У�ʹ����������������ǰ�����������������ʢ������������������װ���ñ�ű�ʾ�ش𣬻�����������������ʢ��������������������ֵ����
��5�����õ���ֵ���DZ�ʵ�ʺ���ƫ�ͣ�˵����������δ�����Ը��������Һ��ַ�Ӧ������ԭ�����������ʹ��죬
�ʴ�Ϊ��ͨ���������ʹ��죬��������δ�����Ը��������Һ��ַ�Ӧ���Ѿ����ų���
���������
�����Ѷȣ���
3��ѡ���� ����������ȷ���ǣ�������
A��Na��Al��Fe����������һ����������ˮ��Ӧ������H2�Ͷ�Ӧ�ļ�
B��Ư�ۺ�����������������ˮ�Ĵ��������ߵ�����ԭ������ͬ
C����SO2ͨ��Ca��ClO��2��Һ������CaSO3����
D��������ͭ��Ũ���ᷴӦ�����ɵ�����ֻ��NO2
�ο��𰸣�A������3Fe+4H2O ?����?.??Fe3O4+4H2������A����
B������Ư�����õ��Ǵ������ǿ�����ԣ�������ˮ���õ��������ӵ�ˮ��ԭ����������ԭ����ͬ����B��ȷ��
C�����ڴ��������ǿ�����ԣ��Ὣ��������������������Ca��ClO��2+SO2+H2O=CaSO4��+HCl+HClO����C����
D���տ�ʼ��Ӧ�����ɶ������������ŷ�Ӧ�Ľ��У�Ũ����Ũ�ȼ�С�����ϡ���ᣬ������һ����������D����
��ѡB��
���������
�����Ѷȣ���
4��ѡ���� ����������ɫ��Һ��SO2�������þ�����ɫ����ʵ����ͬ����
[? ]
�����Ը��������Һ����Ʒ����Һ�� ��ˮ���ܵ��з�̪������������Һ
A���٢�
B���ڢ�
C���٢�
D���ڢ�
�ο��𰸣�A
���������
�����Ѷȣ���
5��ѡ���� ������������������CO��SO2���壬���й��������������˵����ȷ���ǣ�������
A�����߶���Ⱦ������Σ������
B�����߶����γ��������Ҫԭ��
C�����߶���ʹƷ����Һ��ɫ
D�����߶�������ˮ
�ο��𰸣�A
���������
�����Ѷȣ�һ��