| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点归纳《离子方程式的书写及正误判断》高频试题预测(2017年最新版)(八)
(3)加硒盐中含有的硒元素是人体微量元素中的“抗癌之王”,写出证明硒元素非金属性比硫元素弱的一个实验事实: 。 (4)加碘盐可防治碘缺乏症,其中的碘酸钾(KIO3)在酸性溶液中可氧化亚硫酸钠,生成物能使淀粉变蓝,1mol KIO3被还原时,转移电子 mol,该反应的离子方程式为 。 参考答案:(共12分)(1)A(2分) 本题解析:(1)人体吸收的是钙元素的化合物,同时还不能对人体产生危害。A.CaCO3不会对人体产生危害,会与人体内的酸发生反应产生CaCl2,补充钙元素,正确; B.CaO与水发生反应产生Ca(OH)2,对人体产生腐蚀,、危害,不能使用,错误; C.Ca(OH)2溶于水放热,对人体造成伤害,电离产生的OH-也会对人体造成腐蚀,不能使用,错误;D.Ca是很活泼的金属单质,与人体内的水发生反应产生氢气和强碱Ca(OH)2,对人产生一定危害,错误。故选项是A;(2)低钠盐因含有氯化钾和硫酸镁可防治高血压和心血管病,往其溶液中滴入氨水,发生复分解反应产生沉淀。反应的化学方程式是MgSO4 +2NH3・H2O=Mg (OH)2↓+ (NH4) 2SO4或Mg2++2NH3・H2O= Mg (OH)2↓+2NH4+;(3)硒元素、硫元素是同一主族的元素,元素的非金属性越强,其最高价氧化物对应的水化物的酸性就越强,相应的氢化物的稳定性就越强,形成氢化物越容易进行解析比较。所以可以通过硒与氢气化合比硫更难(或硒酸酸性比硫酸弱,或硒化氢稳定性比硫化氢弱,或硫能置换出硒等)。(4)加碘盐可防治碘缺乏症,其中的碘酸钾(KIO3)在酸性溶液中可氧化亚硫酸钠,生成物能使淀粉变蓝,说明产生了I2,根据元素化合价升高或降低的总数等于原子的原子失去或获得的电子数可知:1mol KIO3被还原时,转移电子5mol,该反应的离子方程式为2IO3-+5SO32-+2H+===I2+5SO42-+H2O。 本题难度:一般 2、选择题 下列离子方程式书写正确的是 |
参考答案:A
本题解析:铁和稀盐酸反应生成Fe2+B错,石灰石是不溶物要写成化学式,C错;硫酸铜溶液和氢氧化钡溶液反应还有BaSO4沉淀生成D错,选A。
考点:离子方程式的正误判断。
本题难度:一般
3、选择题 下列离子方程式书写不正确的是
A.在氢氧化钡溶液中逐滴加入硫酸氢钠溶液至恰好呈中性:
Ba2++2OH-+2H++SO42-====BaSO4↓+2H2O
B.在苯酚钠溶液中通入少量二氧化碳:C6H5O-+H2O+CO2→C6H5OH+HCO3-
C.在澄清石灰水中滴加过量碳酸氢钠溶液:
Ca2++2HCO3-+2OH-====CaCO3↓+2H2O+ CO32-
D.向100mL0.2mol/L溴化亚铁的溶液中慢慢通入448mL(标准状况)Cl2:
2Fe2++4Br-+3Cl2====2Fe3++2Br2+6Cl-
参考答案:D
本题解析:略
本题难度:一般
4、选择题 往含0.2 mol NaOH和0.1 mol Ba(OH)2的溶液中持续稳慢地通入CO2气体,使CO2气体充分参加反应,当通入气体为6.72 L(S.T.P)时立即停止,则这一过程中,溶液中离子的物质的量和通入CO2气体的体积关系正确的图像是(气体的溶解忽略不计) ( )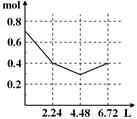
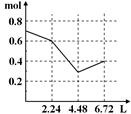
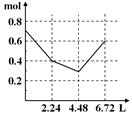
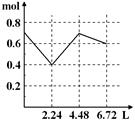
A. B. C. D.
参考答案:A
本题解析:由题溶液中所含离子有Na+ 0.2mol,Ba2+0.1mol,OH―0.4mol,总量0.7mol通入CO2,首先Na+、Ba2+进行沉淀,减少到0.4mol处,在通入CO2,BaCO3转化为BaHCO3,当转化完全时,开始转化NaCO3,离子浓度开始回升。
考点:考查沉淀与溶解平衡
本题难度:一般
5、选择题 下列反应既属于离子反应,又属于氧化还原反应的是
A.铝与盐酸反应
B.Na与O2常温下反应
C.NaHCO3受热分解
D.Al(OH)3受热分解
参考答案:A
本题解析:A、HCl电离出离子,有离子参加,属于离子反应,且Al、H元素的化合价变化,属于氧化还原反应,正确;B、Na与O2常温下反应生成氧化钠,属于氧化还原反应,不属于离子反应,错误;C、不是在溶液中进行的反应,所以不属于离子反应,无化合价变化,不属于氧化还原反应,错误;D、Al(OH)3受热分解,不是在溶液中进行的反应,所以不属于离子反应,无化合价变化,不属于氧化还原反应,错误。
考点:考查离子反应,氧化还原反应。
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点归纳《元素周期律.. | |