| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
�߿���ѧ֪ʶ���ܽᡶ���ʵķ��롢�ᴿ����Ƶ����̣�2017�����°棩(��)
��3�����̿����������KOH��KClO3������״̬�·�Ӧʱ����������__________________���ѧʽ������Ӧ���ˮ�ܽ�õ�����Һ����Ҫ����KCl��K2MnO4������Һ�ữʱ������Ӧ�����ӷ���ʽΪ _______________________________�� ��4����֪KMnO4�����ȵľ������ữ��Na2C2O4��Ӧ����Mn2����CO2��ȡ�����Ƶõ�KMnO4��Ʒ0.33 g��ǡ����0.67 g Na2C2O4��ȫ��Ӧ����KMnO4�Ĵ���Ϊ________���� �ο��𰸣���10�֣� ��������� �����Ѷȣ�һ�� 4�������� ���б����ᡢ���������Ҵ����õĻ��Һ��ijͬѧ��Ʒ��������������ʣ����������е�ijЩ���Ӻ����ʡ�
��ѡ���Լ���10%����������Һ��0.1mol/L���ᡢ0.1mol/LNa2CO3��0.1mol/L NaHCO3��Ũ��ˮ����ʯ�ҡ�0.1mol/L FeCl3��0.1mol/L BaCl2��CO2��0.1mol/L��ˮ������ʯ��ˮ ��1�����������������£� 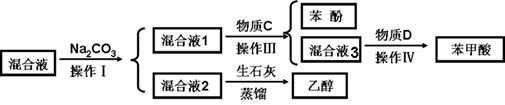 ������C��_____________������IV��_____________�� �ڲ���III��������Ҫ��ѧ��Ӧ����ʽ_________________? _______________________________�� �ۻ��Һ2�м�����ʯ�ҵ�ԭ����_______�� ��2����ͬѧ������Һ1���Ƿ��б��Ӻ�NaHCO3����֤�����Ե�ǿ����
��3����ȡ2.0g������ͱ��ӵĻ�Ϲ������������Ҵ��У��μ���������NaHCO3��Һ����÷ų���CO2����״���£�������CO2����ˮ��Ϊ33.6mL ���������������Ϊ_________________________��ֻ��ʽ�������㣩�����Ϊ________�����������1λС���������������Է�������Ϊ122��������Է�������Ϊ94�� �ο��𰸣���17�֣� �����������1������������ǿ����HCl>������>H2CO3>����> HCO3��������ͱ��ӵ��Ҵ���Һ��̼���ƻ��ʱ����������̼���Ʒ�Ӧ�����ɱ������ơ�������̼��ˮ��������̼���Ʒ�Ӧ���ɱ����ƺ�̼�����ƣ����Ҵ���̼���ƶ�����Ӧ����ͼ�ɵã����Һ1����Ҫ�ɷ��DZ������ơ������ơ�̼�����ơ�̼���Ƶ����ʣ����Һ2����Ҫ�ɷ����Ҵ������ʣ���������ǿ��˳��������C��̼��������̼���壬��������̼��������̼��ˮ�������ֽⷴӦ�����ɱ��ӡ�̼�����ƣ�������������̼��������̼��ˮ����Ӧ������Һ3����Ҫ�ɷ��DZ������ƺ�̼�����Ƶ����ʣ�����D�������HCl�������뱽�����Ʒ������ֽⷴӦ�����ɱ�������Ȼ��ƣ�������̼�����Ʒ������ֽⷴӦ�������Ȼ��ơ�������̼�����ˮ�����ڱ���������ˮ���������뱽�����Ʒ�Ӧ�����γɱ�����Ĺ�������Һʱ���������������ᾧ�壬����Һ�з���������ᾧ��IJ���IV�ǹ��ˣ����ԣ�����ʯ��Ϊ�����ƣ�CaO�Ǽ��������������ˮ��Ӧ�������ܷе�ϸߵ��������ƣ����Ҵ��������Ʋ���Ӧ�����Ҵ����ܷе�ϵͣ�����ʱ�Ҵ����״ӻ�����з��룻��2������̼���ƹ���������Һ1�п��ܺ��б������ơ������ơ�̼�����ơ�̼���Ƶ����ʣ�����̼�����ܸ���̼�����Ƶļ��飬��˲����Ӧ��ȡ�����ټ������0.1mol/L BaCl2�������ã���̼���������ȫ����Ϊ̼�ᱵ���ų�̼������Ӷ�̼��������ӵĸ��ţ����ݲ����������ͽ������ƣ�����̼�����������ǿ�������¿��Ա�Ϊ������̼���壬˵������ٵ��ϲ���Һ�еμ�����0.1mol/L���ᣬ�ٽ�����������ͨ�����ʯ��ˮ�У�����ʯ��ˮ����ǣ�˵����Һ1�к���̼��������ӣ����ڲ���2�м������������Խ�������ת��Ϊ���ӣ���˲������Ҫ��ȡ���Һ1�����ڱ������Ȼ�����Һ����ɫ�����������Ȼ�����Һ����ɫ��������Ũ��ˮ��Ӧ���ɰ�ɫ��������������Ũ��ˮ���ܲ�����ɫ�������������Ʒ�м���0.1mol/L FeCl3��Ũ��ˮ������Һ������ɫ�����ְ�ɫ�ij�������˵�����Һ1�����з��ǻ��ӣ���3�����������̼�����ʵ�����33.6��10��3/22.4mol�����ٸ��ݱ������뱥��̼��������Һ��Ӧ�б������������̼��ϵ��֮�ȵ������ʵ���֮����������ʵ�����33.6��10��3/22.4mol����Ȼ�����Ħ�����������������33.6��10��3/22.4mol��122g/mol���������ݻ�Ϲ�������������������������[33.6��10��3/22.4mol��122g/mol]��2.0g��100%=9.15%��9.2%�� �����Ѷȣ�һ�� 5��ѡ���� ���з������ʵķ����У�����ȷ���ǣ������� �ο��𰸣�B ��������� �����Ѷȣ��� |
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ���߿���ѧ֪ʶ���ܽᡶ���ӹ��桷.. | |
| �����Ŀ |