微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 将AgCl分别投入下列溶液中:
①20ml 0.1mol/L的(NH4)2CO3溶液
②40ml 0.03mol/L的HCl溶液
③50ml 0.03mol/L的AgNO3溶液
④30ml 0.02mol/L的CaCl2溶液
⑤10ml 蒸馏水
⑥30ml 0.2mol/L的NH4NO3溶液
AgCl的溶解度由大到小的顺序是――――
参考答案:
①>⑥>⑤>②=③>④
本题解析:
在水中AgCl存在溶解平衡(注:第一个方程式是双向箭头)
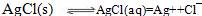
(注:s表示为溶解的固体,aq表示已被溶解,但未电离的AgCl)
当溶液中存在Ag+或者 时,溶解平衡逆向移动,AgCl的溶解度减小。溶液中Ag+和
时,溶解平衡逆向移动,AgCl的溶解度减小。溶液中Ag+和 的浓度越大,逆向移动的程度越大,溶解度就越小。
的浓度越大,逆向移动的程度越大,溶解度就越小。
以中性的水为参照,溶解度5>2="3>4"
又由于有反应:(注:双向)
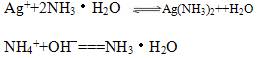
说明溶液碱性越强,NH4(+)的浓度越大,银离子越容易被消耗,AgCl的溶解度也越大。由于作为弱酸弱碱盐的(NH4)2CO3的PH值显然大于强酸弱碱盐的NH4NO3,所以与水比较有1>6>5
综上所述:1>6>5>2=3>4
本题难度:简单
2、选择题 下述实验不能达到预期实验目的是( )
| 序号 | 实验内容 | 实验目的
A
向盛有10滴0.1mol/L AgNO3溶液的试管中滴加0.1mol/L NaCl溶液,至不再有沉淀生成,再向其中滴加0.1mol/L Na2S溶液
证明AgCl能转化为溶解度更小的Ag2S
B
向2mL甲苯中加入3滴KMnO4酸性溶液,振荡;向2mL苯中加入3滴KMnO4酸性溶液,振荡
证明与苯环相连的甲基易被氧化
C
向Na2SiO3溶液中通入CO2
证明碳酸的酸性比硅酸强
D
向淀粉溶液中加入稀硫酸,水浴加热,一段时间后,再加入新制的氢氧化铜并加热
验证淀粉已水解
|
A.A
B.B
C.C
D.D
参考答案:A.再向其中滴加0.1mol/LNa2S溶液,会生成黑色沉淀,说明有Ag2S生成,可说明Ag2S的溶解性更小,故A正确;
B.甲苯可与酸性高锰酸钾反应生成苯甲酸,而苯不反应,说明与苯环相连的甲基易被氧化,故B正确;
C.二氧化碳与水反应生成碳酸,向Na2SiO3溶液中通入CO2产生沉淀,可说明碳酸的酸性比硅酸强,故C正确;
D.淀粉在酸性条件下水解生成葡萄糖,与氢氧化铜的反应应在碱性条件下进行,应先调节溶液至碱性,故D错误.
故选D.
本题解析:
本题难度:一般
3、简答题 硫酸钙是一种用途非常广泛的产品.
(1)25℃时,Ksp(CaSO4)=7.10×10-5.在1L0.1mol?L-1CaCl2溶液中加入1L0.2mol?L-1的Na2SO4溶液,充分反应后(假设混合后溶液的体积变化忽略不计)溶液中Ca2+物质的量的浓度为______mol?L-1.
(2)某校课外活动小组为测定已部分脱水的生石膏的组成(xCaSO4?yH2O),做如下实验:将固体放在坩埚中加热,经测量剩余固体质量随时间变化如图所示.

①x:y=______.
②t2~t3时间段固体的化学式为______.
③t5~t6时间段固体质量减轻的原因是产生了两种气体,其中一种能使品红溶液褪色,则该时间段所发生反应的化学方程式为______.
参考答案:(1)1L0.1mol?L-1CaCl2溶液中加入1L0.2mol?L-1的Na2SO4溶液,充分反应后,Na2SO4过量,
反应后溶液中c(SO42-)=1L×0.2mol/L-1L×0.1mol/L2L=0.05mol/L,
又:Ksp(CaSO4)=c(Ca2+)×c(SO42-)=7.10×10-5,
c(Ca2+)=7.10×10-50.05mol/L=1.42×10-3mol/L,
故答案为:1.42×10-3;
(2)①在加热到t1时xCaSO4?yH2O开始分解,t1~t2时间段和t3~t4时间段个固体的质量变化比较少,而t5~t6时间段固体质量变化较大,原因是t1~t2时间段生石膏脱去部分水,t3~t4时间段完全脱水,
则m(H2O)=3.26g-2.72g=5.4g,m(CaSO4)=2.72g,
n(H2O)=5.4g18g/mol=0.3mol,n(CaSO4)=2.72g136g=0.2mol,
所以n(CaSO4):n(H2O)=x:y=0.2:0.3=2:3,
故答案为:2:3;
②生石膏在加热条件下失去部分水生成熟石膏,熟石膏的主要成分为2CaSO4?H2O 或CaSO4?12H2O,
故答案为:2CaSO4?H2O 或CaSO4?12H2O;?
③在t4时完全生成CaSO4,在t5~t6时间段温度较高,CaSO4开始分解,产生了两种气体,其中一种能使品红溶液褪色,则该气体为二氧化硫,反应的方程式为2CaSO4?高温?.?2CaO+2SO2↑+O2↑,
故答案为:2CaSO4?高温?.?2CaO+2SO2↑+O2↑.
本题解析:
本题难度:一般
4、选择题 已知Ag2SO4的Kw为2.0×10-3,将适量Ag2SO4固体溶于100 mL水中至刚好饱和,该过程中Ag+和SO42-浓度随时间变化关系如图〔饱和Ag2SO4溶液中c(Ag+)=0.034 mol・L-1〕。若t1时刻在上述体系中加入100 mL0.020 mol・L-1 Na2SO4溶液,下列示意图中,能正确表示t1时刻后Ag+和SO42-浓度随时间变化关系的是
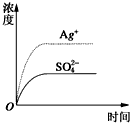
[? ]
A.
B.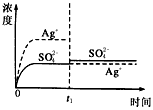
C.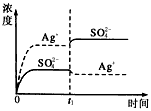
D.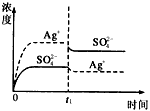
参考答案:B
本题解析:
本题难度:一般
5、选择题 下列关于难溶电解质溶液说法正确的是 ( )
A.在含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+)增大
B.相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水、②0.1 mol・L-1盐酸、③0.1 mol・L-1氯化镁溶液、④0.1 mol・L-1硝酸银溶液中,Ag+浓度:①>④=②>③
C.向AgCl悬浊液中滴加Na2S溶液,白色沉淀变成黑色:2AgCl+S2-=Ag2S↓+2Cl-
D.25 ℃时,在Mg(OH)2悬浊液中加入少量的NH4Cl固体后,c(Mg2+)增大