��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���·�Ӧ�в�����������ԭ��Ӧ����
A��2KMnO4��16HCl(Ũ)��2KCl��2MnCl2��5Cl2����8H2O
B��2Na2O2��2H2O��4NaOH��O2��
C��FeO��4HNO3(Ũ)��Fe(NO3)3��NO2����2H2O
D��Mg(HCO3)2��4NaOH��Mg(OH)2����2Na2CO3��2H2O
�ο��𰸣�D
���������������Ԫ�ػ��ϼ������ķ�Ӧ����������ԭ��Ӧ��A��Mn�Ļ��ϼ۽��ͣ���Ԫ�صĻ��ϼ����ߣ�B����Ԫ�صĻ��ϼ۲������ߣ����ֽ��ͣ�C����Ԫ�صĻ��ϼ����ߣ���Ԫ�صĻ��ϼ۽��ͣ�����������ԭ��Ӧ��D���Ǹ��ֽⷴӦ�����ϼ۲��䣬����������ԭ��Ӧ����ѡD��
�����������dz�ʶ��֪ʶ�Ŀ��飬��Ҫ�ǿ���ѧ����������ԭ��Ӧ�жϵ��˽�������������ʹ��̲̽ģ��������������Ĺؼ���ȷ�жϳ��й�Ԫ�صĻ��ϼ۱仯�����Ȼ��������ͻ�ѧ����ʽ������ü��ɡ�
�����Ѷȣ���
2������� (12��)����ұ���ʹ������漰���෴Ӧ��
��1������������ұ����Ӧ����ʱ���õ�ⷨ����______
a��Fe2O3 b��NaCl c��Cu2S d��Al2O3
��2����ͭ��Cu2S���ɷ�����Ӧ2Cu2S + 2H2SO4 + 5O2 �� 4CuSO4 + 2H2O���÷�Ӧ�Ļ�ԭ����______����1molO2������Ӧʱ����ԭ����ʧ���ӵ����ʵ���Ϊ______mol��
��3��ͼΪ��⾫������ʾ��ͼ��______����a��b����Ϊ�������ʵĴ�������b������������ɫ�������ɣ������ɸ�����ĵ缫��ӦʽΪ ��

��4��Ϊ������������ĺڰߣ�Ag2S�������������������������ʳ��ˮ�в������Ӵ���Ag2Sת��ΪAg��ʳ��ˮ������Ϊ �����ܷ�ӦʽΪ�� ��
��5����¯������ұ��������Ҫ��������������Ҫ��ӦΪ��Fe2O3��s��+3CO��g��= 2Fe��s��+3CO2��g��
��֪����FeO(s) + CO(g) �� Fe(s) + CO2(g) ��H1����11KJ/mol
��3Fe2O3(s) + CO(g) �� 2Fe3O4(s) + CO2(g) ��H2����47KJ/mol
��Fe3O4(s) + CO(g) �� 3FeO(s) + CO2(g) ��H3��+19KJ/mol
��ӦFe2O3��s�� + 3CO��g��= 2Fe��s��+ 3CO2��g���ġ�H�� ��
�ο��𰸣���12�֣�
(1)b d (2��)
(2) Cu2S�� 4 (��1��)
(3)a (1��)�� NO3�� + 2H+ + e�� =NO2 ��+H2O(2��)
(4)�ٵ��磨�����������Һ������ˮ�����˻�ѧ��Ӧ(���������һ�㼴��1��)�� 3Ag2S+2Al+3H2O=2Al(OH)3+3H2S��+6Ag (2��)
(5)-25kJ/mol (2��)
�����������1�����õ�ⷨ����ұ���Ľ���һ���ǽϻ��õĽ������������ڵ��Ȼ��ơ�����������ȡ�ơ�������ȡ����ͭͨ�����û�ԭ�������Դ�ѡbd��
��2��2Cu2S + 2H2SO4 + 5O2 �� 4CuSO4 + 2H2O�У���ԭ����Ԫ�ػ��ϼ����ߵ�Ԫ�أ�����CuԪ�صĻ��ϼ۴�+1�����ߵ�+2�ۣ�����Cu2S����ԭ������1molO2������Ӧʱ����ԭ��ʧȥ���ӵ����ʵ���Ҳ���������õ����ӵ����ʵ������÷�Ӧ����������������1mol������Ӧʱ�õ�4mol���ӣ����Ի�ԭ��ʧȥ���ӵ����ʵ�����4mol��
��3����⾫����ʱ���������������������������������Դ����������������aΪ������b����������ɫ���壬�����ɫ����Ϊ����������˵�����ֵ���������ӷ�����ԭ��Ӧ���ɶ����������缫��ӦʽΪNO3�� + 2H+ + e�� =NO2 ��+H2O��
��4��Ϊ������������ĺڰߣ�Ag2S�������������������������ʳ��ˮ�в������Ӵ���ʹAl��Ag2S��ʳ��ˮ����ԭ��أ���Al����صĸ�������������Ӧ����Ag2S������ԭ��Ӧ������ԭΪAg������ʳ��ˮ���������Һ��������ã�ͬʱˮҲ�����˷�Ӧ���ܷ�ӦΪAl��ˮ��Ag2S����������ԭ��Ӧ����Ag���������������⣬��ѧ����ʽΪ3Ag2S+2Al+3H2O=2Al(OH)3+3H2S��+6Ag��
��5�����ݸ�˹���ɣ������� �Ȼ�ѧ����ʽ��δ���ֵ�������ȥ����������Ȼ�ѧ����ʽΪ����+2��+6�٣�/3������Fe2O3��s�� + 3CO��g��= 2Fe��s��+ 3CO2��g���ġ�H��[����47KJ/mol��+2����+19KJ/mol��+6��(��11KJ/mol)]/3=-25kJ/mol��
���㣺����������ԭ��Ӧ�ķ��������ԭ����Ӧ�ã���˹���ɵ�Ӧ�ã�
�����Ѷȣ�����
3��ѡ���� ���л�ѧ������ȷ���ǣ�?��
A����ϩ�ı���ģ�ͣ�
B��HClO�Ľṹʽ��HClO
C��H2O2�ĵ���ʽ��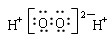
D���Ҵ��ķ���ʽ��CH3CH2OH
�ο��𰸣�A
���������A����ȷ��B��HClO�Ľṹʽ��H�DO�DCl��?B����C��H2O2�ĵ���ʽ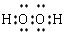 ��C����D���Ҵ��ķ���ʽ��C2H6O��D����ѡA��
��C����D���Ҵ��ķ���ʽ��C2H6O��D����ѡA��
�����Ѷȣ�һ��
4��ѡ���� ��4.48g Fe����1L 0.2mol��L-1��ϡ���ᣬ�ټ���50mL 0.4mo1��L-1KNO3��Һ�����е�Fe2+ȫ��ת����Fe3+��NO3����ʣ�࣬����һ�ֵ�������NYOX����õ�������Ļ�ѧʽ��
A��N2O
B��NO
C��N2O3
D��NO2