| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点总结《影响化学反应速率的因素》考点强化练习(2017年押题版)(六)
参考答案:D 本题解析:根据图像,若要使曲线b变为曲线a,反应的平衡状态没有变化,但反应速率加快,达到平衡的时间减少。该反应是反应前后体积不变的可逆反应,因此改变的条件只可能是使用了催化剂或增大压强,答案D。 本题难度:一般 3、选择题 铝与过量的稀盐酸反应,为了减慢反应速率,但是又不影响生成的氢气总量,可以采取的措施是( ) 参考答案:A.升高温度,反应速率加快,故A不选; 本题解析: 本题难度:一般 4、简答题 为了研究外界条件对H2O2分解速率的影响,某同学做了以下实验,请回答下列问题.
(2)实验①的目的是______. (3)实验②未观察到预期的实验现象,为了帮助该同学达到实验目的,你提出的对上述操作的改进意见是______(用实验中所提供的几种试剂). (4)某同学在50mL一定浓度的H2O2溶液中加入一定量的二氧化锰,放出气体的体积(标准状况下)与反应时间的关系如图1所示,则A、B、C三点所表示的瞬时反应速率最快的是______(填“A”或“B”或“C”). 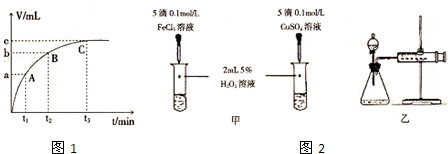 (5)对于H2O2分解反应,Cu2+也有一定的催化作用.为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图2甲、乙所示的实验.请回答相关问题: ①定性分析:如图甲可通过观察______,定性比较得出结论.有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是______. ②定量分析:用图乙所示装置做对照实验,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略.实验中需要测量的数据是______. 参考答案:(1)氯化铁作催化剂条件下,双氧水迅速分解生成氧气和水,反应方程式为:2H2O2 FeCl3. 2H2O+O2↑, 本题解析: 本题难度:一般 5、选择题 对于反应2SO2+O2 |
参考答案:D
本题解析:①增大压强,单位体积内的分子数增多,单位体积内的活化分子数增多,而活化分子百分数不变,反应速率加快,错误;②升高温度单位体积内的分子数不变,单位体积内的活化分子数增多,活化分子百分数增多,反应速率加快,正确;③增大O2浓度单位体积内的分子数增多,单位体积内的活化分子数增多,而活化分子百分数不变,反应速率加快,错误;④使用催化剂单位体积内的分子数不变,单位体积内的活化分子数增多,而活化分子百分数增多,反应速率加快,正确。因此选项是D。
考点:考查影响化学反应速率的知识。
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点总结《化学基本理.. | |