微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 分析化学中常用X射线研究晶体结构,有一种蓝色晶体可表示为:[MxFey(CN)z],研究表明它的结构特性是Fe2+、Fe3+分别占据立方体的顶点,自身互不相邻,而CN一位于立方体的棱上,其晶体中的阴离子晶胞结构如图示,下列说法正确的是?(?)
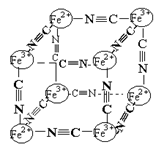
A.该晶体属于原子晶体
B.该晶体的化学式为M [Fe2(CN)6] 或M [FeFe(CN)6]
C.M的离子位于上述立方体的体内,呈+1价
D.该晶体属于离子化合物,M呈+2价
参考答案:BC
本题解析:根据晶胞的结构特点可知,该晶体是离子晶体,不是原子晶体,A不正确。根据阴离子的晶胞结构可判断,含有的铁离子和亚铁离子均是4
+
本题难度:简单
2、选择题 下列叙述正确的是( )?
A.离子晶体中一定含有活泼金属元素的离子?
B.原子晶体都是化合物?
C.固态不导电、水溶液能导电,这一性质能说明某晶体一定是离子晶体?
D.离子晶体一般具有较高的熔点?
参考答案:D?
本题解析:某些离子晶体可能只含有非金属元素的原子,如NH4Cl、CH3COONH4等,因此选项A不正确。原子晶体可以是化合物,如水晶,也可以是单质,如金刚石,所以B选项不正确。离子晶体和某些分子晶体(如冰醋酸)都具有固态不导电、水溶液能导电的性质,因此这一性质不能说明某晶体一定是离子晶体,选项C不正确。?
一般来说,固态不导电,溶于水或熔融状态均能导电这一性质能较充分说明某晶体是离子晶体,因为熔融状态下分子晶体不导电。
本题难度:一般
3、选择题 下表中有关晶体的说明,错误的是( )
选项
| 晶体名称
| 组成晶体微粒
| 晶体内作用力
|
A
| 碘化钾
| 阴阳离子
| 离子键
|
B
| 干冰
| 分子
| 共价键
|
C
| 晶体硅
| 原子
| 共价键
|
D
| 碘
| 分子
| 范德华力
参考答案:B
本题解析:干冰晶体中分子之间的作用力是范德华力。
本题难度:一般
4、填空题 (6分) 有下列物质①铁?②干冰?③金刚石?④水晶?⑤氯化钠?⑥碘?⑦氢氧化钠,用编号填写下列空格。
(1)离子晶体有?,分子晶体有?,原子晶体有?;
(2)已知微粒间作用力包括化学键及分子间作用力。上述物质所含的微粒间作用力中,仅有共价键的有?,仅有离子键的有?,既含共价键又含离子键的有?;
参考答案:(1)⑤⑦;②⑥;③④(2)③④;⑤;⑦
本题解析:略
本题难度:简单
5、选择题 下列说法中正确的是
A.C60气化和I2升华克服的作用力相同
B.分子晶体在水溶液中一定导电
C.氯化钠和氯化氢溶于水时,破坏的化学键都是离子键
D.用作高温结构陶瓷材料的Si3N4固体是分子晶体
参考答案:A
本题解析:B项:分子晶体在熔融状态下都不导电,在水溶液中不都导电,主要看它是不是电解质,大多数非金属单质及其形成的化合物如干冰(CO2)、I2、HF、H2O、NH3、CH3CH2OH大多数有机物,其固态均为分子晶体。它们的水溶液几乎都导电。比如酸类的就导电,而蔗糖也是分子晶体但他水溶液不导电,故错;C项:氯化氢溶于水破坏的是共价键,故错;D项:Si3N4是原子晶体,故错。故选A。
点评:本题考查的是分子间作用力、分子晶体、原子晶体和化学键的相关知识,比较综合,题目难度适中。
本题难度:一般
|