��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����������Ԫ���γɻ���������й������������(����)
A��ˮ���ӵĽṹʽΪ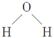
B��������γɵĻ�����(OF2)�У���Ԫ�صĻ��ϼ�Ϊ��2��
C��Na2O2�ĵ���ʽΪNa��[����������������������������]2��Na��
D����MgO�����У�O2���Ľṹʾ��ͼ�ɱ�ʾΪ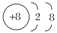
�ο��𰸣�B
�����������������˲�ͬ���Ӽ������Ҫ��ȷд������ʽ��ԭ�ӽṹʾ��ͼ���ṹʽ�����ϼ۵�Ӧ����ȷ��������ԭ�ӻ������ӡ����ӣ��ǹ��ۻ����ﻹ�����ӻ�����������ȷ����Ĺؼ���������γɵĻ�����(OF2)�У����ķǽ����Աȷ������������ۡ�
�����Ѷȣ�һ��
2������� ����ѧ����ѡ��3�����ʽṹ�����ʡ���15�֣�
��֪X��Y��Z����Ԫ�ص�ԭ������֮�͵���48��X��һ��1��2���⻯������м��ЦҼ����Цм�������ԭ�ӹ�ƽ�档Z�ǽ���Ԫ�أ�Z�ĵ��ʺͻ������й㷺����;����֪Z�ĺ˵����С��28���Ҵ������2��δ�ɶԵ��ӡ���ҵ������ZO2��̼�ᱵ������״̬����ȡ������M��M�ɿ���һ�ֺ������Σ�����X���߷�����M�������С�ظ���ԪΪ�����壨����ͼ��������λ��ΪZ4+��ռ������λ��ΪBa2+��ռ����������λ��ΪO2�C��ռ��
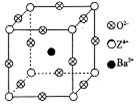
��1��Y2+�Ľṹʾ��ͼ________________��Z�ļ۲�����Ų�ʽΪ____________��
��2��X�ڸ��⻯������_____________��ʽ�ӻ���X��Y�γɵĻ�����YX2�ĵ���ʽΪ_____________________��
��3�����Ʊ�M�Ļ�ѧ��Ӧ����ʽ��______________________________________��
����M�����У�����Z4+��������������ģ�Ba2+����������Ķ��㣬��O2�C�����������_______________��
����֪O2�C�뾶Ϊ1.4��10�C10 m��Z4+�İ뾶Ϊ6.15��10�C11m������ӵ�����ΪNA����M���ܶ�Ϊ_______________g��cm�C3�������ػ���
�ο��𰸣�����(3)��3��,����ÿ��2��,��15�֣�
��1��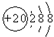 ? 3d24s2?��2��sp2?
? 3d24s2?��2��sp2?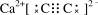
��3���� TiO2 + BaCO3 = BaTiO3 + CO2��?������?��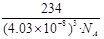
���������
��X��һ��1��2���⻯������м��ЦҼ����Цм�������ԭ�ӹ�ƽ�档��XΪ̼������Z�ǽ���Ԫ�أ�Z�ĵ��ʺͻ������й㷺����;����֪Z�ĺ˵����С��28���Ҵ������2��δ�ɶԵ��ӡ�ZΪ22���ѣ�1s22s22p63d24s2��YΪ48-6-22=20���ơ�
��1��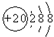 ? 3d24s2?��2��sp2?
? 3d24s2?��2��sp2?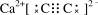
��3���� TiO2 + BaCO3 = BaTiO3 + CO2��?������
���ɾ�̯����ѧʽΪ��BaTiO3,137��48��48=233,������ı߳�Ϊ��1.4��10�C10 m+6.15��10�C11m����2=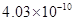 m=4.03��10-8cm,
m=4.03��10-8cm,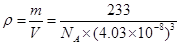 ?g��cm�C3
?g��cm�C3
�����Ѷȣ�һ��
3������� ��Ϣһ����ͬ�����ܡ����Ƚ������Թ��ɸ��ºϽ𡢵��ȺϽ𡢾��ܺϽ�ȣ����ں��ա�����������DZ��ȹ�ҵ���š�
��Ϣ�����Ȼ�������CrO2Cl2���Ǹ���һ�ֻ���������¸û������ǰ���ɫҺ�壬�۵�Ϊ��96.5�棬�е�Ϊ117�棬�ܺͱ�ͪ��CH3COCH3�������Ȼ�̼��CS2���л��ܼ����ܡ�
��1��д��Fe��26��Ԫ�أ�ԭ�ӵĻ�̬�����Ų�ʽΪ ?��
��2��CH3COCH3�����к���?���м�������?���ļ���
��3����̬�Ȼ���������?���壬��ͪ��̼ԭ�ӵ��ӻ���ʽΪ?������̼����?����ԡ��Ǽ��ԡ�)���ӡ�
��4��K[Cr(C2O4)2(H2O)2]Ҳ�Ǹ���һ�ֻ�����û������������ӻ�������г������Ӽ������ۼ��⣬��������?����
��5���������ľ�������ͼ��ʾ��һ�������к���?����ԭ�ӡ�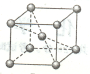
�ο��𰸣�
��1��1s22s22p63s23p63d64s2��[Ar] d64s2����2�֣�
��2��1 ��2�֣���9 ��2�֣�
��3�����ӣ�1�֣���?��̼ԭ��sp3���ʻ�̼ԭ��sp2?��2�֣���?�Ǽ��ԣ�2�֣�
��4����λ��1�֣�
��5��2?��3�֣�
�����������1����Ϊ26��Ԫ�أ����ڵ������ڵ�VIII�壬���Կ��Ժܼ�д�����̬�����Ų�ʽ����2��CH3COCH3�����ʻ��к���1���м�������2��C��C�ļ���6��C��H�ļ���1��C��O�ļ��� ��3��ͨ���Ȼ����������µ��۷е㡢�ܽ��Կ�֪���ڷ��Ӿ��壻��ͪ�к�������̼ԭ�ӣ���̼ԭ���ӻ���ʽ�����̼ԭ����ͬ���ʻ�̼ԭ���У�ɾȥ�����ԭ��������ԭ�ӹ��棬���ʻ�̼ԭ���ӻ���ʽΪsp2����ͪ�����Ȼ�̼�ǷǼ��Է��ӣ�����̼Ҳ�ǷǼ��Է��ӡ���4��K[Cr(C2O4)2(H2O)2]����λ��������п϶�������λ������5����������ʾ����9��ԭ�ӣ���8��λ�ھ������㣬ÿ�������ϵ�ԭ������8�������������ڸþ�����ֻ��1/8�������ڵ�ԭ����ȫ���ڸþ��������һ�������к���2����ԭ�ӡ�
�����Ѷȣ�һ��
4��ѡ���� �������ʲ�����ͬ����������� ��?��?
A�����ʯ��ʯī
B��ˮ����ʯӢ
C�����Ͱ���
D��C60�ͽ��ʯ
�ο��𰸣�B
���������ͬ����������ָͬ��Ԫ�ع��ɵIJ�ͬ����,Bѡ���е����ʹ�����Ҫ�ɷ���SiO2,�ǻ�����,������ͬ��������.
�����Ѷȣ� 91EXAM.orgһ��
5��ѡ���� ���й�������˵����ȷ����
[? ]
A.ֻҪ�������ӣ������������
B.ֻҪ�������ӣ������������
C.������һ�����л�ѧ��
D.�ǽ���Ԫ��ֻ���γɹ��ۻ�����
�ο��𰸣�B
���������
�����Ѷȣ���