微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (15分)甲醚(CH3OCH3)被称为21世纪的新型燃料,它清洁、高效、具有优良的环保性能,甲醚是一种无色气体,具有轻微的醚香味,其燃烧热为1455 kJ/mol,甲醚可作燃料电池的燃料。
(1)写出甲醚燃烧的热化学方程式 ;已知H2(g)和C(s)的燃烧热分别是285.8 kJ・mol-1、393.5 kJ・mol-1;计算反应4C(s)+6H2(g)+O2(g)==2CH3OCH3 (g)的反应热为 ;
(2)工业上利用H2和CO2合成二甲醚的反应如下:6H2(g)+2CO2(g) CH3OCH3(g)+3H2O(g) △H<0
CH3OCH3(g)+3H2O(g) △H<0
①一定温度下,在一个固定体积的密闭容器中进行该反应.下列能判断反应达到化学平衡状态的是
______(选填编号,注意大小写)
a.c(H2)与c(H2O)的比值保持不变
b.单位时间内有2mol H2消耗时有1mol H2O生成
c.容器中气体密度不再改变
d.容器中气体压强不再改变
②温度升高,该化学平衡移动后到达新的平衡,CH3OCH3的产率将
________(填“变大”、“变小”或“不变”,下同),混合气体的平均式量将__________;
(3)以甲醚、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。该电池的负极反应式为____________________;
(4)用(3)中的燃料电池为电源,以石墨为电极电解500 mL滴有酚酞的NaCl溶液,装置如图所示:
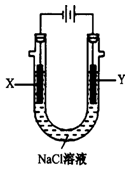
请写出电解过程中Y电极附近观察到的现象 ;当燃料电池消耗2.8 LO2(标准状况下)时,计算此时:NaCl溶液的pH= (假设溶液的体积不变,气体全部从溶液中逸出)。
参考答案:(1)CH3OCH3(g)+3O2(g)=2CO2(g)+3H2O(l) △H= ―1455kJ/mol(2分)
△H=―378.8kJ/mol(3分) (2)①a d;(各1分,共2分)②变小;变小;(各1分,共2分)
(3)CH3OCH3+16OH-―12e-=2CO32-+11H2O(2分)
(4)Y电极附近溶液中有气体产生,上部分呈黄绿色(2分) 14(2分)
本题解析:(1)燃烧热是在一定条件下,1mol可燃物完全燃烧生成稳定的氧化物时所放出的热量,甲醚的燃烧热为1455 kJ/mol,则甲醚燃烧的热化学方程式为CH3OCH3(g)+3O2(g)=2CO2(g)+3H2O(l) △H= ―1455kJ/mol;已知H2(g)和C(s)的燃烧热分别是285.8 kJ・mol-1、393.5 kJ・mol-1,则有关的热化学方程式为:①H2(g)+1/2O2(g)=H2O(l)△H=-285.8KJ/mol;②C(s)+O2(g)=CO2(g)△H=-393.5KJ/mol;③CH3OCH3(g)+3O2(g)=2CO2(g)+3H2O(l)△H=-1455kJ/mol,所以根据盖斯定律可知①×3+②×2-③得到反应热化学方程式为:2C(s)+3H2(g)+1/2O2(g)=CH2OCH3(g) △H=-169.4kJ/mol,即4C(s)+6H2(g)+O2(g)=2CH2OCH3(g) △H=-378.8kJ/mol;
(2)①在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态。A、氢气是反应前,水蒸气是生成物,因此当c(H2)与c(H2O)的比值保持不变时可以说明反应达到平衡状态,a正确;b、根据方程式可知单位时间内有2mol H2消耗时一定有1mol H2O生成,因此不能据此说明达到平衡状态,b错误;c、密度是混合气的质量和容器容积的比值,在反应过程中质量和容积始终是不变的,因此容器中气体密度不再改变不能说明达到平衡状态,c错误;D、正方应是压强减小的可逆反应,因此当容器中气体压强不再改变是能说明达到平衡状态,d正确,答案选ad。
②正方应是放热反应,因此温度升高,该化学平衡向逆反应方向移动,到达新的平衡,CH3OCH3的产率将变小。混合气的平均相对分子质量是混合气的质量和混合气的总的物质的量的比值,质量不变,物质的量增大,则混合气体的平均式量将变小。
(3)原电池负极失去电子,发生氧化反应。因此甲醚在负极放电,碱性条件下生成碳酸根离子与水,则电极反应式为CH3OCH3+16OH-―12e-=2CO32-+11H2O;
(4)根据装置图可知Y电极与电源的正极相连,作阳极。溶液中的氯离子放电生成氯气,因此Y电极附近溶液中有气体产生,上部分呈黄绿色;标准状况下2.8LO2的物质的量是2.8L÷22.4L/mol=0.125mol,根据电极反应O2+2H2O+4e-=4OH-可知电子转移为0.125mol×4=0.5mol。所以根据电子守恒可知电解池中也转移0.5mol电子,因此根据阳极电极反应为4OH--4e-=2H2O+O2↑可知生成氢氧根离子的物质的量是0.5mol,其浓度是0.5mol÷0.5L=1.0mol/L,所以溶液中氢离子浓度是10-14mol/L,因此溶液的pH=14。
考点:考查燃烧热、热化学方程式、盖斯定律、平衡状态判断、外界条件对平衡状态的影响以及电化学原理的应用等
本题难度:一般
2、填空题 某课外化学兴趣小组设计了如图所示装置(虚框内部分未画出),在装置内起初发生的反应为: ? Cu+H2SO4===H2↑+CuSO4
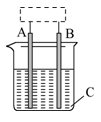
(1)该装置的名称是________.
(2)A、B中至少有一种是金属________,接________.
(3)C溶液中含有________.
参考答案:(1)电解池
(2)铜 ;电源的正极
(3)H2SO4
本题解析:
本题难度:一般
3、填空题 工业氢氧化钾的溶液中含有某些含氧酸的钾盐杂质,可用离子交换膜法电解提纯。电解槽内装有阳离子交换膜,其工作原理如图所示。

(1)该电解槽的阳极反应式为:? ?
?
(2)阳离子交换膜的作用是?
(3)通电开始后,阴极附近溶液pH会增大,其主要原因是?(填序号)
A.阳极区的OH-移向阴极所致
B.阴极产生的金属钾与水反应生成了大量OH-
C.阴极由H2O电离出的H+放电生成H2,促进水的电离,使OH-浓度增大
(4)除去杂质后的氢氧化钾溶液从溶液出口_____________(填写“A”或“B”)导出。
参考答案:①4OH――4e ―=2H2O+O2↑(或2H2O―4e―=4H++O2↑)
―=2H2O+O2↑(或2H2O―4e―=4H++O2↑)
②阻止阴离子和气体分子通过?(或其它合理说法)
③C? ④ B
本题解析:略
本题难度:简单
4、选择题 金属镍有广泛的用途。粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍,下列叙述正确的是(已知:氧化性Fe2+<Ni2+<Cu2+)
[? ]
A.阳极发生还原反应,其电极反应式:Ni2++2e-== Ni
B.电解过程中,阳极质量的减少与阴极质量的增加相等
C.电解后,溶液中存在的金属阳离子只有Fe2+和Zn2+
D.电解后,电解槽底部的阳极泥中只有Cu和Pt
参考答案:D
本题解析:
本题难度:一般
5、选择题 用铂电极(惰性)电解下列溶液时,阴极和阳极上的主要产物分别是H2和O2的是?
[? ]
A.稀NaOH溶液?
B.HCl溶液
C.酸性CuSO4溶液?
D.酸性AgNO3溶液
参考答案:A
本题解析:
本题难度:一般