微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 A、B、C是单质,X、Y、Z、H、J、L是化合物,组成B的元素是绿色植物生长所必需的大量元素之一,且B在空气中燃烧可以得到X和J,X和J均为固体,X水解可生成两种碱性物质。在适当条件下,它们相互之间有下图所示的转化关系:
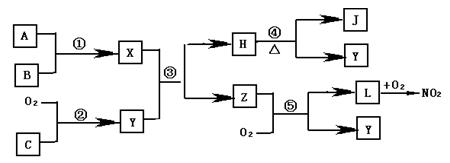
(1)写出物质J的电子式_____________
(2)与Z具有相同电子数的两种离子反应可生成Z和Y,这两种离子是?、 ?。
(3)反应③的化学方程式?。
(4)反应⑤的化学方程式?。
参考答案:(1) Mg2+[:O:]2-? (2) NH4+?OH-? (3) Mg3N2 + 6H2O ="=" 3Mg(OH)2 + 2NH3
(4) 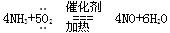
本题解析:略
本题难度:一般
2、填空题 (10分)下已知A~K均为中学化学中的常见物质,它们之间的转化关系如下图所示,其中A、D为金属单质,反应过程中生成的水及其他部分产物已略去。

请回答以下问题:
(1)E中阳离子的结构示意图为?。
(2)CO2的电子式为?。
(3)向F中通入足量CO2生成K的离子方程式?。
(4)写出H在空气中生成I的化学方程式?。
( 5 )写出E到F的离子方程式??。
参考答案:(1)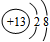 ?(2)
?(2) (3)AlO2―+CO2+H2O=Al(OH)3↓+HCO3―
(3)AlO2―+CO2+H2O=Al(OH)3↓+HCO3―
(4)4Fe(OH)2+O2+2H2O=4Fe(OH)3?Al 3+ + 4OH- ?= AlO2-?+ 2H2O
本题解析:本题是无机框图题,关键是找准突破点。I是红褐色固体,所以I是氢氧化铁,H是氢氧化亚铁,J是氯化铁,G是氯化亚铁,所以D是铁。由于B是氧化铁,所以A是铝,C是氧化铝,E是氯化铝,F是偏铝酸钠,K是氢氧化铝。
本题难度:一般
3、填空题 (9分)A、B、C、D、E 5种元素,已知:
①A原子最外层电子数是次外层电子数的2倍,B的阴离子与C的阳离子跟氖原子的电子层结构相同。E原子M层上的电子比K层多5个。
②常温下B2是气体,它对氢气的相对密度是16。
③C的单质在B2中燃烧,生成淡黄色固体F。F与AB2反应可生成B2。
④D的单质在B2中燃烧,发出淡紫色火焰,生成有刺激性气味的气体DB2。DB2中D的质量分数为50%。根据以上情况回答:
(1)A是______、B是______、C是______、D是______、E是______(写元素符号)。
(2)E的原子结构示意图__________,C的离子结构示意图__________。
(3)F和AB2反应的化学方程式________________________________________________。
参考答案:(共9分)
(1)C , O , Na , S , Cl(各1分,共5分)
(2) ?(
?( 各1分,共2分)
各1分,共2分)
(3)2Na2O2+2CO 2=2Na2CO3+O2↑(2分)
2=2Na2CO3+O2↑(2分)
本题解析:略
本题难度:一般
4、简答题 已知物质M由同一短周期的X、Y两种元素组成,X原子的最外层电子数是最内层电子数的一半,Y元素最高正价与它的负价代数和为6.M与其他物质的转化关系如图(部分产物已略去):
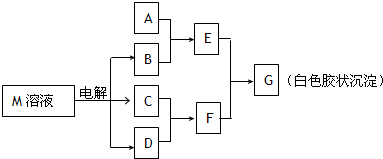
(1)若A是与X、Y同周期的一种常见金属,则A元素在周期表中的位置是______周期______族,写出A与B溶液反应的化学方程式______.
(2)若A是某元素的一种常见酸性氧化物,可用于制造光导纤维,则该元素原子结构示意图为______,写出E与F反应的离子方程式______.
(3)B的电子式为______,其中的化学键为______.用电子式表示M的形成过程______.
(4)工业上用电解物质M的产物之一氧化有毒含氰(CN-)碱性废水,得到无毒的N2、CO2等.写出此反应的离子反应方程式______.
参考答案:X原子的最外层电子数是最内层电子数的一半,则X是Na元素,X和Y属于同一周期,且Y元素最高正价与它的负价代数和为6,则Y是Cl元素,物质M由同一短周期的X、Y两种元素组成,则M是NaCl,电解氯化钠溶液生成氢气、氯气和氢氧化钠,
(1)若A是与X、Y同周期的一种常见金属,则A是铝,铝能和氢氧化钠反应,则B是氢氧化钠,铝在元素周期表中位于第三周期第IIIA族,铝和氢氧化钠溶液反应生成偏铝酸钠和氢气,其反应方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,
故答案为:第三;IIIA族;2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
(2)若A是某元素的一种常见酸性氧化物,可用于制造光导纤维,则A是二氧化硅,所以该元素是硅元素,二氧化硅能和B溶液反应生成E,则B是氢氧化钠溶液,二氧化硅和氢氧化钠溶液生成E硅酸钠,氯气和氢气反应生成F氯化氢,硅酸钠和盐酸反应生成G硅酸,硅原子核外有14个电子,其原子结构示意图为:

,盐酸和硅酸钠反应生成硅酸的离子反应方程式为:2H++SiO32-=H2SiO3↓,
故答案为:

;2H++SiO32-=H2SiO3↓;
(3)B是氢氧化钠,其电子式为:

;?氢氧化钠中钠离子和氢氧根离子之间存在离子键,氢原子和氧原子之间存在共价键,氯化钠的形成过程中钠原子失电子,氯原子得电子,所以氯化钠的形成过程为:

,
故答案为:

;离子键和共价键;

;
(4)氯气氧化氰(CN-)生成N2、CO2,自身被还原生成氯离子,其离子反应方程式为:5Cl2+2CN-+8OH-=10Cl-+N2+2CO2+4H2O,故答案为:5Cl2+2CN-+8OH-=10Cl-+N2+2CO2+4H2O.
本题解析:
本题难度:一般
5、填空题 (16分)X、Y为常见的两种单质,Z是氧气,A、B为常见化合物。它们在一定条件下可发生如图所示的反应(均是在非溶液中进行的反应):

(1)画出Z的原子结构示意图?;
(2)当X为金属,Y为非金属时,A可能的电子式为? ?或? ;
(3)当X为非金属,Y为金属时,X可能的化学式为? ?或? ?;
(4)当X与Y均为金属时,写出X与A反应的化学方程式? ?;
(5)当X与Y均为非金属时,若X与Y同主族,写出X与A反应的化学方程式? ?;
若X与Y不在同一主族,写出X与A反应的化学方程式? ??。
参考答案:(1)? ?(2)
?(2) ?或?
?或? ?
?
(3)? C?或? H2?(4)8Al+ 3Fe3O4 ?9Fe+4Al2O3
?9Fe+4Al2O3
(5)2C+SiO2 Si+2CO↑? C+H2O
Si+2CO↑? C+H2O H2+CO
H2+CO
本题解析:(1)氧原子的原子序数是8,位于第二周期第ⅥA,所以原子结构示意图为 。
。
(2)当X为金属,Y为非金属时,A可能是水或CO2,电子式分别是 ?或?
?或? 。
。
(3)当X为非金属,Y为金属时,则X可以是氢气或碳。
(4)当X与Y均为金属时,反应应该是铝热反应,方程式为8Al+ 3Fe3O4 ?9Fe+4Al2O3
?9Fe+4Al2O3
(5)(5)当X与Y均为非金属时,若X与Y同主族,则可以是碳置换硅,方程式为2C+SiO2 Si+2CO↑;若X与Y不在同一主族,则应该是碳和水蒸气的反应,方程式为C+H2O
Si+2CO↑;若X与Y不在同一主族,则应该是碳和水蒸气的反应,方程式为C+H2O H2+CO
H2+CO
本题难度:一般