微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题
 ?
?
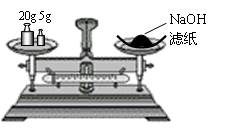
称量氢氧化钠固体?配制150mL0.10mol/L盐酸
A、?B、
 ?
?
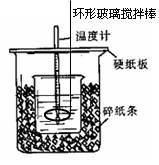
测定中和热?分离苯和甲苯
C、?D、
参考答案:C
本题解析:本题考查实验基本操作技能,较易题。氢氧化钠固体易潮解,应放在小烧杯或称量瓶中称量,且要“左物可码”,故A错;将溶液转移到容量瓶中须用玻璃棒引流,B也错;C正确;D中冷凝水应“下进上出”,故D 也错。
本题难度:一般
2、选择题 用一充满氨气的烧瓶做喷泉实验,当水充满整个烧瓶后,烧瓶内的氨水的物质的量浓度是(按标准状况下计算)
A.1mol・L-1
B.0.045mol・L-1
C.0.029mol・L-1
D.不能确定
参考答案:B
本题解析:设烧瓶的容积是VL,则氨气的物质的量是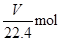 ,由于氨气极易溶于水,所以水充满烧瓶,则烧瓶内的氨水的物质的量浓度是
,由于氨气极易溶于水,所以水充满烧瓶,则烧瓶内的氨水的物质的量浓度是 ,答案选B。
,答案选B。
点评:该题是高考中的常见题型和考点,属于基础性试题的考查。试题难易适中,注重解题的灵活性,侧重对学生能力的培养,有利于培养学生的逻辑思维能力,也有助于调动学生的学习兴趣和学习积极性。
本题难度:简单
3、实验题 某中学化学课外活动小组欲探究铁在氯气中燃烧产物的成份、性质和用途,设计了如下实验步骤:
(1)用下列实验装置制取干燥纯净的氯气

①制备并收集得到干燥纯净的氯气,上述各装置按气流从左到右方向连接顺序为? (填仪器接口的字母编号)
②该实验还存在不足之处,应如何改进??
(2)某同学将一定量铁粉与Cl2恰好完全反应得到一固体物质a,然后通过实验确定其成分。探究过程如下:
①提出假设:(请把下列假设补充完整)假设①:该固体物质是FeCl3;假设②:? ;假设③:? 。
②设计实验方案:取少量固体物质a于烧杯中,加适量水溶解,然后取两份a溶液分别进行实验,实验现象与结论如下表,请在表格内的横线处填空。

由此得出结论:假设?_______?成立(填序号①②③)。
(3)为进一步探究物质a的性质,他们又利用a溶液做了如下一些实验,其中现象、结论均正确的是_____________(填写序号)
A.向氢氧化镁悬浊液中滴加a溶液出现红褐色沉淀,证明Fe(OH)3溶解度小于Mg(OH)2溶解度
B.向a溶液中加入少量铁粉,铁粉溶解,溶液颜色由浅绿色变成黄色
C.向沸水中滴加a的饱和溶液,立即出现红褐色沉淀
D.将a溶液加热蒸干并灼烧,得到Fe2O3固体
(4)a溶液常作印刷电路铜板的腐蚀剂,得到含有Cu2+等的废液,有人提出可以利用如下图的装置从得到的废液中提炼金属铜。该过程中甲池负极的电极反应式是?,若乙池中装入废液500mL,当阴极增重3.2g时,停止通电,此时阳极产生气体的体积(标准状况)为? (假设气体全部逸出)。

参考答案:(1)①aedbcgf?
②在C后接NaOH溶液尾气处理装置
(2)(1 )FeCl2;FeCl3和FeCl2的混合物;
(2)由此得出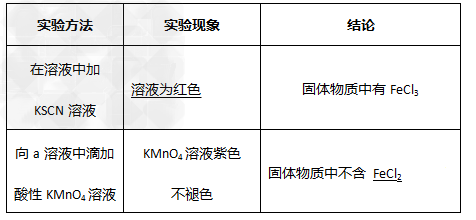
结论:假设①结论成立
(3)AD
(4)CH4+10OH--8e-=CO32-+7H2O;1.12L
本题解析:
本题难度:一般
4、简答题 某研究性学习小组通过实验来探究乙二酸(又名草酸)受热分解的产物,他们设计的实验装置如图所示:
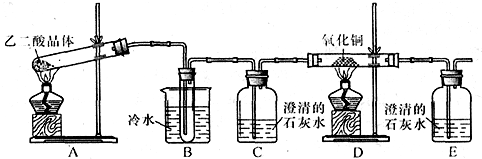
查阅资料可知:乙二酸晶体(H2C2O4?2H2O)熔点100.1℃,草酸钙是难溶于水的白色固体;Cu2O能溶于稀硫酸,立即发生歧化反应生成Cu2+和Cu.
(1)实验过程中观察到C、E装置中的溶液均变浑浊,且D装置中黑色粉末变为红色,写出A中发生反应的化学方程式:______;
(2)装置B的作用是______;上述装置中有两处需要改进(假设洗气装置每次吸收气体均完全),改进方法是______;______.
(3)实验结束后向装置B的试管中加入NaHCO3溶液,产生大量无色气体,由此可以证明两种物质的酸性强弱顺序是______.
(4)有人认为D装置中得到的红色固体可能是Cu,也可能是Cu和Cu2O的混合物.实验小组进一步探究:①取少量红色固体加入到盛稀硫酸的试管中,充分振荡,溶液变为蓝色,试管底部仍有红色固体,由此可以得出的结论是______.②取6.8g红色固体与足量的稀硝酸反应,收集到标准状况下的NO气体1.12L.则红色固体中含单质铜的质量分数是______.
参考答案:(1)C、E装置中的溶液均变浑浊,且D装置中黑色粉末变为红色,说明乙二酸晶体加热生成一氧化碳、二氧化碳和水,反应的化学方程式:H2C2O4?2H2O?△?.?CO↑+CO2↑+3H2O;
故答案为:H2C2O4?2H2O?△?.?CO↑+CO2↑+3H2O;
(2)乙二酸可以和氢氧化钙发生反应,所以防止对检验分解产物CO2的干扰,要除去生成物中带出的乙二酸蒸汽,一氧化碳在还原氧化铜之前要将气体干燥,一氧化碳有毒,所以要进行尾气处理,
故答案为:除去生成物中带出的乙二酸蒸汽,防止对检验分解产物CO2的干扰;在C与D之间再装配一个盛浓硫酸的洗气瓶(或装有碱石灰的干燥管),将装置E中出来的气体引到酒精灯火焰上让其燃烧(或收集装置E中逸出的尾气);
(3)B的试管中是乙二酸,加入NaHCO3溶液,产生大量无色气体应该是二氧化碳,化学反应遵循强酸制弱酸的原理,所以酸性是乙二酸大于碳酸(或H2C2O4>H2CO3),故答案为:乙二酸大于碳酸(或H2C2O4>H2CO3);
(4)①金属铜和硫酸不反应,但是氧化亚铜可以和硫酸反应生成金属铜和硫酸铜,根据实验现象:溶液变为蓝色,则证明红色固体中含有Cu2O,故答案为:红色固体中含有Cu2O;
②设红色固体中氧化亚铜的物质的量是x,金属铜的物质的量为y,根据质量关系得:144x+64y=6.8,根据电子守恒,得出:2x+2y=1.12L22.4L/mol×(5-2),两式联立解得x=0.025mol,y=0.05mol,所以Cu的质量分数为:0.05mol×64g/mol6.8g×100%=50%,故答案为:50%.
本题解析:
本题难度:一般
5、实验题 Ⅰ?下图所示A-H为实验室常见的仪器、装置(部分固定夹持装置略去),请根据要求回答下列问题。

(1)A仪器的名称是________________________。
(2)用图示仪器设计一套制取纯净、干燥的氨气的装置,仪器的连接顺序是(用管口字母符号表示)j-___、-_____、-____、-___、-____、-____(可不填满)。
Ⅱ?某校化学兴趣小组为研究Cl2单质的性质,设计如下图所示装置进行实验。装置III中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。

(3)Ⅰ的反应方程式为:________________________
(4)加入药品前,检查I中气体发生装置气密性的操作是:_________________
(5)实验过程中,装置IV中的实验现象为________________________________
(6)实验结束后,该组同学在装置III中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为应在_________之间还需添加洗气瓶(选填装置序号),该装置的作用是______________________。
参考答案:(1)容量瓶
(2)j--l,k--d,c--h(或i)
(3)MnO2?+?4HCl(浓)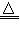 MnCl2?+?Cl2↑?+?2H2O
MnCl2?+?Cl2↑?+?2H2O
(4)用止水夹夹住C处橡皮管,然后向分液漏斗中加水,打开分液漏斗活塞,液体不能顺利流下则气密性好
(5)无色溶液变蓝色
(6)Ⅱ和Ⅲ;干燥Cl2
本题解析:
本题难度:一般