��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1�������
��һ����ȫ���¼��������д���K2CO3��ʵ�鲽�輰�������
1.ȡ�������Ʒ����ˮ���ֱ�ȡ������Һ��������ʵ��
2._________________________________________��һ������K+;
3.___________________________________________________��һ������CO32����
�������ⶨK2CO3��������
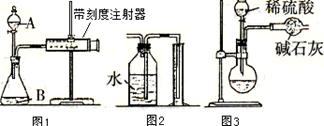
(1)��ͬѧ��ͼ1��ʾװ�ã���xg�Ļ����������ϡ���ᷴӦ�ⶨ������CO2����������ʵ�鿪ʼʱ����װ�������Եķ�����?
?��
(2)��ͬѧ��ͼ2����ͼ1�е��ռ�װ�ã�������K2CO3��������??(�ƫ����ƫС���������䡱)����ĸĽ�������?��
(3)��ͬѧ��ͼ3װ�òⶨCO2����������װ�ô��ڽ϶�ȱ�ݣ��Ӷ�����ʵ����������д���е�����ȱ�ݣ�I?��
��?
��?
�ο��𰸣���һ��2. ����ɫ��Ӧ��ͬʱ���ܲ���Ƭ�ۿ�ȼ�յĻ��棬�������ɫ��; 3.�����Ȼ�����Һ�а�ɫ�������ټ�����������ܽ�������ɫ��ζʹ����ʯ��ˮ���ǵ����塣
��������1���ر�A����������ע������������һ�����룬һ��ʱ����ɿ��������۲�����Ƿ�ص�ԭλ����2��ƫС;��ˮ���ɱ���̼��������Һ;
��3�����ٲ�����CO2�����л���ˮ������ͬʱ����ʯ�����գ����½��ƫ�ڷ�Ӧ������װ���ڲ�����CO2���岻��ȫ���ų������½��ƫС�������θ�����������ͨ��Ҳ�����տ����е�CO2��ˮ���������½��ƫ��ʵ�鿪ʼʱ��װ���ڵĿ����л��в���CO2Ҳ�ᱻ��ʯ�����գ����½��ƫ��ȡ�
�����������
�����Ѷȣ���
2��ʵ���� (18��)ij��ѧ��һ������ȤС��Ϊ̽��ͭ������ķ�Ӧ������������ͼ��ʾװ�ý����й�ʵ�顣

��1���ȹرջ���a����6.4gͭƬ��12 mLijŨ�ȵ�Ũ�������Բ����ƿ�й�������Ӧ��ϣ�������ƿ�л���ͭƬʣ�ࡣ�ٴ���a���������е�������������Բ����ƿ�����ͭƬ��ȫ��ʧ��
��д��������������ƿ�ڷ����Ļ�ѧ����ʽ���رջ���a?��
����a?��
��B�������ռ�ʵ���в����������װ�ã�������δ��ȫ��������ͼ�аѵ��ܲ���������
��ʵ�������װ��C�е���Һ�п��ܺ��е�������?��
��2����С���ͬѧ�ԡ���μ���SO2�л�������CO2���������ܸ���Ȥ������A��ͭƬ����ľ̿�ۣ�����A��B֮������������װ�ã�

�Լ���a. NaOH��Һ? b. Ʒ����Һ? c. ����KMnO4��Һ? d. Ca(OH)2��Һ
��ش�
�ٸ�ͬѧ��ʵ��װ��A�з����Ļ�ѧ����ʽ? ?��
?��
����Ҫ�ﵽ��Ŀ�ģ������ڣ�(�����ṩ�Լ����)
D���?��E���?��F���?��
��3����ʵ֤ʵ���ڣ�1����ͭƬ��ȫ��ʧ����������ʣ�࣬��ͬѧ���ⶨ��������ʵ���Ũ�ȣ����跴Ӧǰ����Һ����仯���Բ��ƣ�����Ӧ����Һ�м��뺬����a mol ��NaOH��Һ�պ�ʹ��Һ��Cu2+ȫ���������ݴˣ����������������ʵ���Ũ�������ܣ���д���������ʵ���Ũ�ȵı���ʽ��?mol/L(
��NaOH��Һ�պ�ʹ��Һ��Cu2+ȫ���������ݴˣ����������������ʵ���Ũ�������ܣ���д���������ʵ���Ũ�ȵı���ʽ��?mol/L( �ú�a�Ĵ���ʽ��������ܣ��ÿղ���)��
�ú�a�Ĵ���ʽ��������ܣ��ÿղ���)��
�ο��𰸣�
��1����Cu+2H2SO4(Ũ)  CuSO4+SO2?+2H2O����2�֣�
CuSO4+SO2?+2H2O����2�֣�
2Cu+O2+2H2SO4 2CuSO4+2H2O ��2��
2CuSO4+2H2O ��2�� ��
��
(��ֲ�д�ɣ�2Cu+O2=2CuO��CuO+H2SO4=CuSO4+H2O��Ҳ��)
��
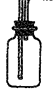 ? (2��)
? (2��)
��NaOH? Na2SO3? Na2SO4?��3�֣�
��2����C+2H2SO4��Ũ�� ?CO2?+2SO2?+2H2O?��3�֣�
?CO2?+2SO2?+2H2O?��3�֣�
��? c? b? d?��3�֣�
��3��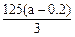 ?��3�֣������������ʽ���ɣ�
?��3�֣������������ʽ���ɣ�
�����������
�����Ѷȣ���
3��ѡ���� ���й���ʵ��ԭ��������������У���ȷ�� ��?��?��
��?��?��
A������ˮ�Ҵ��ӵ�ˮ����ȡ���ʵ�
B��ϡ��Ũ ����ʱ��Ӧ��Ũ���Ỻ��ע��ʢ��ˮ����Ͳ��
����ʱ��Ӧ��Ũ���Ỻ��ע��ʢ��ˮ����Ͳ��
C�����ƣ�FeCl3��Һʱ������Һ�м�������Fe��ϡ����
D���ᴿ��������������Ҵ������ȼ���ʯ��������
�ο��𰸣�D
���������
�����Ѷȣ���
4��ʵ���� ij��ѧ�� ��С�����ʵ��̽�����Ļ���������ʣ�װ������ͼ��ʾ(Aװ��δ����)������AΪ���巢��װ�á�A�������Լ��������й���������ѡȡ����NH4HCO3����NH4Cl����Ca(OH)2����NaOH��
��С�����ʵ��̽�����Ļ���������ʣ�װ������ͼ��ʾ(Aװ��δ����)������AΪ���巢��װ�á�A�������Լ��������й���������ѡȡ����NH4HCO3����NH4Cl����Ca(OH)2����NaOH��
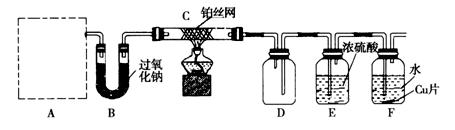
���װ�������Ժ��Ƚ�C����˿�����������ȣ��ٽ�A������������ͨ��Bװ��Ƭ�̺�ȥC���ƾ��ƣ���˿�������ֺ��ȣ�F��ͭƬ���ܽ⡣
(1)ʵ������ȡA������ʱ��ֻ��һ���Լ������Լ���_________________(�������ѡ�Լ������)����ʱA����Ҫ�IJ���������__________________________________(������)��
(2)�������A�������Լ���˵����ȷ����___________________��
A.ʩ�ø����ʻ��������ʳ�������Ի�����Ӱ��
B.������ʵ���Һ�м�����������������Һ������Ӧ�����ӷ���ʽΪ��NH4+ + OH�C = NH3?H2O
C.��ͨ�����ȷ���������Լ���(NH4)2SO4
D.��ҵ����NH3�Ⱥϳɸ����ʵĹ��̿ɳ�Ϊ���Ĺ̶�
(3)װ��C�з�����������Ӧ�Ļ�ѧ����ʽΪ_________________________��װ��E������Ӧ�Ļ�ѧ����ʽΪ_________________________________________________��
(4)����A��B�е�ҩƷ���㣬��װ��F�п��Թ۲쵽��������________________________
___________________________________________________________________ __��
__��
(5)ָ����ʦ�Ӱ�ȫ�뻷���Ƕȿ��ǣ�ָ����װ�����������Ե�ȱ�ݣ���������Ľ��飺_____________________________________________________________________________________ ____________________________________________________________��
____________________________________________________________��
�ο��𰸣�(1) NH4HCO3(2��)?�Թܡ��ƾ���(2��)? (2) C(2��)
(3) 4NH3 + 5O2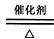 4NO + 6H2O(2��)? 2NH3 + H2SO4 = (NH4)2SO4(2��)
4NO + 6H2O(2��)? 2NH3 + H2SO4 = (NH4)2SO4(2��)
(4)ˮ�в������ݣ���Һ��Ϊ��ɫ�������� ���ƿ�Ϸ���Ϊ����ɫ(3��)
���ƿ�Ϸ���Ϊ����ɫ(3��)
(5)��װ��E��F֮������һ��������װ�ã���װ��F��������һ��β������װ��(2��)
�����������
�����Ѷȣ�һ��
5��ѡ���� ���ʵ�鲻�ܱ���Ԥ��Ŀ�ĵ���?��?��
?
| ���ʵ��
| Ԥ��Ŀ��
|
A
| �ѵ�����������ͬ�ִ���ʯ���е�һ���гɷ�ĩ����ͬ�¶��·ֱ�������ͬŨ�ȵ����ᷴӦ���۲�ų����������
| ��֤�Ӵ�����Ի�ѧ��Ӧ���ʵ�Ӱ�졣
|
B
| ��װ����ɫ��ͬ��NO2��N2O4��������С�Թܣ��ܷ⣩�ֱ������ˮ����ˮ�У��۲��Թ���������ɫ�仯��
| ��֤�¶ȶԻ�ѧƽ���Ӱ�졣
|
C
| ֱ�ӽ��������ͬ��������þ��Ͷ��ͬ�¶ȵ��з�̪����ˮ�У��۲�������ݵ����ʼ���Һ����ɫ�仯��
| �Ƚ�ͬ���ڽ���Ԫ�صĽ�����ǿ����
|
D
| ��������ˮ�ֱ����ʢ���廯����Һ���Ȼ�����Һ���Թ��У��۲���Һ��ɫ�仯��
| ��֤��Ԫ�غ͵�Ԫ�صķǽ�����ǿ����
|
?
�ο��𰸣�CD
�����������
�����Ѷȣ���