微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (14分)A、B、C、D、G都是含有同一种短周期元素的化合物,E是氧化物,H是单质。根据下图转化关系(反应条件及部分产物已略去)填空:&s.5*u.c.om
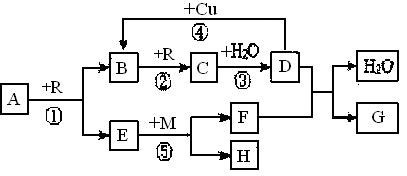
(1)若A、B、C、D、G 均含X元素,且A的一个分子中只含有10个电子,G是复合肥料,则反应①、②、③是工业生产?的基本原理,M的化学式为?;其中反应①的化学方程式为?;反应④的离子方程式为?;
(2)若A、B、C、D、G均含Y元素,Y元素处于X的相邻周期、相邻族,G可作净水剂,则反应①、②、③均是工业生产?的基本原理,M形成的晶体类型为?;其中反应①的化学方程式为?;反应⑤的化学方程式为?。
参考答案:(1)硝酸(1分),K或K2O2或KO2;(2分)
4NH3+5O2
3Cu+8H++2NO3-?3Cu2++2NO↑+4H2O(2分)
(2)硫酸(1分),金属晶体 (2分)? 4FeS2+11O2 ?2Fe2O3+8SO2 (2分)
Fe2O3 + 2Al 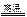 ?Al2O3+ 2Fe (2分&s.5*u.c.om)
?Al2O3+ 2Fe (2分&s.5*u.c.om)
本题解析:略
本题难度:一般
2、填空题 (10分)下图表示的反应关系中,部分产物被略去。已知2mol白色固体粉末X受热分解,恢复到室温生成白色固体A,无色液体B,无色气体C各1mol。X.E.G的焰色反应均为黄色。
回答下列问题:
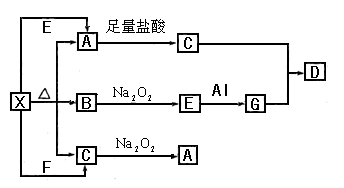
(1)写出下列物质的化学式:A.??
(2)写出X受热的化学反应方程式:?
(3)写出X+E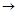 A的离子方程式:?
A的离子方程式:?
(4)写出C与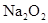 参加反应的化学方程式______________________________________,若0.2mol
参加反应的化学方程式______________________________________,若0.2mol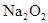 参加反应,则转移的电子数为_____________个。
参加反应,则转移的电子数为_____________个。
参考答案:(10分)(1)? Na2CO3? (2) 2NaHCO3 Na2CO3? + CO2↑+ H2O
Na2CO3? + CO2↑+ H2O
(3) HCO3- + OH- = CO32-?+ H2O
(4)? 2Na2O2 +2 CO2 ="2" Na2CO3 + O2? 0.2NA
本题解析:本题是无机框图题,关键是找准突破点。B是液体,所以B是水。因此E是氢氧化钠,G是偏铝酸钠。2mol白色固体粉末X受热分解,因此X是碳酸氢钠,A是碳酸钠,C是CO2,D是氢氧化铝沉淀。在过氧化钠和CO2的反应中,过氧化钠既是氧化剂,又是还原剂,。所以根据方程式2Na2O2 +2 CO2 ="2" Na2CO3 + O2,如果0.2mol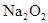 参加反应,则转移的电子数为0.2NA。
参加反应,则转移的电子数为0.2NA。
本题难度:一般
3、填空题 (8分)A、B、C、D、E、F六种物质的相互转化关系如右图所示。图中反应条件均未标出,部分产物(包括水)已略去,反应①是置换反应。
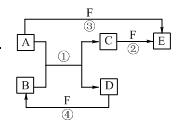
(1)若B、C、F都是气态单质,且B为黄绿色有毒气体。③和④两个反应中都有水生成,反应②需要放电才能发生。A、D均为极易溶于水的气态氢化物,且相遇有白烟生成。则A分子的立体构型为?,反应③的化学方程式为 ?。
?。
(2)若A、D为短周期元素的单质,且所含元素的原子序数A是D的2倍,所含元素的原子最外层电子数D是A的2倍。F是一种含氧酸,③和④两个反应中都有红棕色气体生成。则E的化学式为
? ?
? ?,反应④的化学方程式为?。
?,反应④的化学方程式为?。
参考答案:(1)三角锥形(2分);?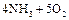

 (2分)
(2分)
(2)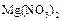 (2分);?
(2分);?

 ?(2分)
?(2分)
本题解析:略
本题难度:一般
4、推断题 下图每一方框中的字母代表一种反应物或生成物:
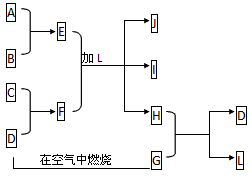
产物J是含A金属元素的胶状白色沉淀,I为NaCl溶液,D是淡黄色固体单质。试填写下列空白:
(1)L的化学式为:____________。
(2)F的化学式为:__________。
(3)写出J受热分解反应的化学方程式:______________________。
(4)H和G之间反应的化学方程式为:____________________。
参考答案:(1)H2O
(2)Na2S
(3)2Al(OH)3 Al2O3+3H2O
Al2O3+3H2O
(4)2H2S+SO2==3S+2H2O
本题解析:
本题难度:一般
5、简答题 A、B、C、D、E、F、G、H、I、J、K都是中学课本常见物质,它们与X具有下图相互转化关系.
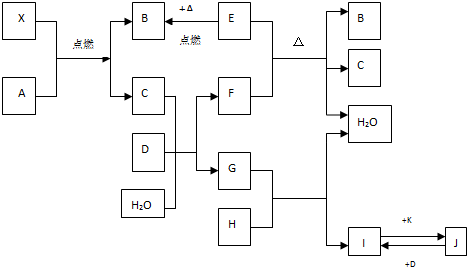
已知:①A、D、E、K为单质,其中E为黑色固体;
②X、A、B、C、D为气体,B、C均能使澄清石灰水变浑浊,C、D均能使品红溶液褪色;
③H是一种红棕色固体氧化物.
请回答下列问题:
(1)B分子的电子式:______;
(2)J与氨水反应的离子方程式:______;反应全过程的现象是:______;
(3)E和F反应的化学方程式:______;
(4)气体X中含有三种元素,分子中各原子均达到8电子稳定结构,其对H2的相对密度为30,试推断X的分子式:______;X的结构式:______.
参考答案:X、A、B、C、D为气体,其中B、C均能使澄清石灰水变浑浊,分别为SO2、CO2中的一种,C、D均能使品红溶液褪色,应为SO2、Cl2中的一种,可推知C为SO2、B为CO2、D为Cl2;
SO2、Cl2与水反应生成F、G分别为HCl、H2SO4中的一种,E为黑色固体单质,点燃生成二氧化碳,能与F反应生成二氧化碳、二氧化硫与水,可推知E为碳,则F为H2SO4,G为HCl;
H是一种红棕色固体氧化物,应是Fe2O3,与盐酸反应生成I为FeCl3,FeCl3与单质K反应生成J,J与氯气反应又得到FeCl3,可推知K为Fe、J为FeCl2;
(4)中气体X中含有三种元素,与单质A在点燃条件下生成SO2、CO2,则A为O2,由元素守恒可知X中含有C、S、O三种元素,其对H2的相对密度为30,则X的相对分子质量为60,故X的分子式为SCO,分子中各原子均达到8电子稳定结构,与CO2为等电子体,则X的结构式为S=C=O,
(1)由上述分析可知,B为CO2,其电子式为: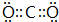 ,故答案为:
,故答案为: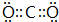 ;
;
(2)J为FeCl2,与氨水反应生成氢氧化亚铁与氯化铵,反应离子方程式为:Fe2++2NH3?H2O=Fe(OH)2↓+2NH4+,整个过程现象是:先生成白色沉淀,立即变为灰绿色,最终变为红褐色,
故答案为:Fe2++2NH3?H2O=Fe(OH)2↓+2NH4+;先生成白色沉淀,立即变为灰绿色,最终变为红褐色;
(3)E和F是碳与浓硫酸在加热条件下生成二氧化碳、二氧化硫与水,反应化学方程式为:C+2H2SO4(浓)△.CO2↑+2SO2↑+2H2O,
故答案为:C+2H2SO4(浓)△.CO2↑+2SO2↑+2H2O;
(4)中气体X中含有三种元素,与单质A在点燃条件下生成SO2、CO2,则A为O2,由元素守恒可知X中含有C、S、O三种元素,其对H2的相对密度为30,则X的相对分子质量为60,故X的分子式为SCO,分子中各原子均达到8电子稳定结构,与CO2为等电子体,则X的结构式为S=C=O,
故答案为:SCO;S=C=O.
本题解析:
本题难度:一般