微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 在一定条件下进行的下列化学反应,请根据以下的转化关系回答下列问题.
已知A、B、C中均含有同种元素.
(1)若D为金属单质,且以上反应均为氧化还原反应,请写出B→C反应的离子方程式:______.
(2)若D为碱,且以上反应均为非氧化还原反应,则A、B、C、D分别可以是:(按顺序写出合理的一组物质的化学式即可)A是______;B是______;C是______;D是______.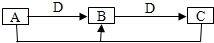
参考答案:根据题给反应关系,
(1)已知A、B、C中均含有同种元素,若D为金属单质,则可以是锌,A可以是FeCl3,锌适量时,Zn+2FeCl3=ZnCl2+2FeCl2;锌过量时,Zn+FeCl2=ZnCl2+Fe,且Fe+2FeCl3=3FeCl2符合题意,所以B为FeCl2,C为Fe,B→C反应的离子方程式为:Zn+Fe2+=Fe+Zn2+;或D为Fe,A为Cl2,B为FeCl3,C为FeCl2,故B→C反应的离子方程式为:2Fe3++Fe=3Fe2+;
故答案为:Zn+Fe2+=Fe+Zn2+;或2Fe3++Fe=3Fe2+;
(2)若D为碱,且以上反应均为非氧化还原反应,所以与碱能发生连续反应的最典型的物质是Al3+,A和C反应是氯化铝和偏铝酸钠反应生成氢氧化铝沉淀,所以反应的离子方程式为:Al3++3AlO2-+6H2O=4Al(OH)3↓;则A可以是AlCl3,B是Al(OH)3,C是NaAlO2,D为NaOH;
故答案为:AlCl3;Al(OH)3;NaAlO2;NaOH.
本题解析:
本题难度:一般
2、简答题 如图表示某些物质之间的转化关系,每个字母代表一种物质,部分产物已略去.A是一种酸式盐,也是一种常用的化学肥料,B是能使湿润的红色石蕊试纸变蓝色的无色气体,D是无色无味的气体.回答下列问题.
(1)物质A的名称是:______
(2)写出物质B的一种主要用途:______
(3)写出工业上制取气体B的化学方程式:______
(4)实验室收集EF的方法:E______D______.
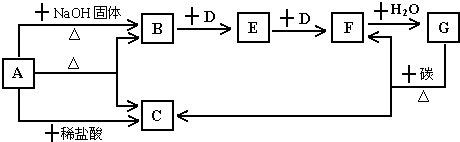
参考答案:A是一种酸式盐,也是一种常用的化学肥料,B是能使湿润的红色石蕊试纸变蓝色的无色气体是NH3,是A和氢氧化钠反应生成,说明A中含铵根离子,B和D发生两部连续反应,说明D是无色无味的气体O2,E为NO,F为NO2,G为HNO3,G和C反应生成二氧化氮和二氧化碳,所以C为CO2,A是一种酸式盐,确定A为碳酸氢铵,
(1)依据判断A为碳酸氢铵,故答案为:碳酸氢铵;
(2)物质B是NO,工业用途可以工业制硝酸(或制氮肥,制氨水等),故答案为:工业制硝酸(或制氮肥,制氨水等);
(3)工业上制取气体B(NH3)是用氢气和氮气高温高压催化剂条件下合成氨,反应的化学方程式为:N2+3H2催化剂.高温高压2NH3,故答案为:N2+3H2催化剂.高温高压2NH3;
(4)E(NO)一氧化氮易和空气中的氧气反应,难溶于水,可以用排水法收集,F(NO2)和水反应,比空气重,可以用向上排空气法收集,故答案为:排水法 向上排空气法.
本题解析:
本题难度:一般
3、填空题 下列框图所示的物质转化关系中,甲是日常生活中常见的金属,乙、丙、丁是常见的气体单质。气体B与气体C相遇产生大量的白烟生成E,A是强碱,D的焰色为紫色 (部分反应物和生成物及水已略去)。

请回答下列问题
(1)写出工业制备B的化学方程式_____________________________________;
(2)写出常温下,A与丁反应的离子方程式________________________________;
(3)下图装置为用排空气法收集气体的实验装置

Ⅰ.当从M端通入气体时,可收集的气体有?;
Ⅱ.当从N端通入气体时,可收集的气体有 ?; (填数字编号)
①气体乙?②气体丙?③气体丁?④气体B?⑤气体C?
(4)E中所含阳离子的检验方法为(包括实验步骤、现象及结论)?;
(5)A中所含阳离子的检验方法为(包括实验步骤、现象及结论)?。
参考答案:(1)N2+3H2 2NH3(2)Cl2+2OH-=Cl-+ClO-+H2O(3)I、③⑤;Ⅱ、②④(4)加入NaOH溶液,加热,用湿润的红色石蕊试纸靠近试管口,试纸变蓝,证明含有NH4+。(5)用洁净的铂丝蘸取A溶液,在无色火焰上灼烧,透过蓝色钴玻璃观察,火焰呈紫色,证明含有K+。
2NH3(2)Cl2+2OH-=Cl-+ClO-+H2O(3)I、③⑤;Ⅱ、②④(4)加入NaOH溶液,加热,用湿润的红色石蕊试纸靠近试管口,试纸变蓝,证明含有NH4+。(5)用洁净的铂丝蘸取A溶液,在无色火焰上灼烧,透过蓝色钴玻璃观察,火焰呈紫色,证明含有K+。
本题解析:乙、丙为单质,在高温高压下催化生成B,且B与C相遇生成大量白烟,可知B为NH3,C为HCl,则丙为H2,乙为N2,丁为黄绿色气体,应为Cl2,E为NH4Cl,可与A反应生成NH3,D的焰色为紫色,应为有K+,说明A应为KOH,D为KCl,则甲为Al。
(1)工业上制备NH3在500℃,20~50MPa,在铁触媒的催化下,N2和H2合成NH3,反应方程式:N2+3H2 2NH3(2)氯气在NaOH溶液中发生反应生成氯化钠和次氯酸钠,反应的离子方程式为:2OH-+Cl2=Cl-+ClO-+H2O(3)I、从M端用排空气发收集通入气体时,收集气体密度应大于空气密度,则M端进气,N端出气,故为③Cl2⑤HCl ;II、从N端用排空气发收集通入气体时,收集气体密度应小于空气密度,则N端进气,M端出气,故为②H2④NH3(4)E为NH4Cl,检验方法为加入NaOH溶液,加热,用湿润的红色石蕊试纸靠近试管口,试纸变蓝,证明含有NH4+;(5)A为NaOH,用洁净的铂丝蘸取A溶液,在无色火焰上灼烧,透过蓝色钴玻璃观察,火焰呈紫色,证明含有K+。
2NH3(2)氯气在NaOH溶液中发生反应生成氯化钠和次氯酸钠,反应的离子方程式为:2OH-+Cl2=Cl-+ClO-+H2O(3)I、从M端用排空气发收集通入气体时,收集气体密度应大于空气密度,则M端进气,N端出气,故为③Cl2⑤HCl ;II、从N端用排空气发收集通入气体时,收集气体密度应小于空气密度,则N端进气,M端出气,故为②H2④NH3(4)E为NH4Cl,检验方法为加入NaOH溶液,加热,用湿润的红色石蕊试纸靠近试管口,试纸变蓝,证明含有NH4+;(5)A为NaOH,用洁净的铂丝蘸取A溶液,在无色火焰上灼烧,透过蓝色钴玻璃观察,火焰呈紫色,证明含有K+。
本题难度:一般
4、填空题 A、B、C、D是中学化学的常见物质,其中A、B、C均含有同一种元素.在一定条件下相互转化的关系如图所示(部分反应中的H2O已略去).请填空:
(1)若D是生产、生活中用量最大、用途最广的金属单质
①若A可用于自来水消毒,则用A制备漂白粉的化学方程式是______.则C的化学式是______.配制C的溶液时可加入少量的______(填物质名称)以抑制水解.
②若A是某强酸的稀溶液,则A的化学式可能是______.
(2)若A是一种能使湿润的红色石蕊试纸变蓝的气体,B是汽车尾气之一,遇空气会变色,则反应①的化学方程式为______.
(3)若B有两性
①若D是强酸,则能确定A、C中肯定含的离子的化学式分别是______、______.
②若D是强碱,则反应②的离子方程式是______.
(4)若A、B、C的焰色反应都呈黄色,D是气态酸性氧化物,则D可能是______或______(填化学式),鉴别它们常可选用______、______(任填两种试剂名称).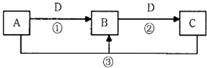
参考答案:(1)若D是生产、生活中用量最大、用途最广的金属单质判断为Fe;
①若A可用于自来水消毒,证明为Cl2,则用A制备漂白粉的化学方程式是氯气和氢氧化钙反应生成氯化钙、次氯酸钙和水,反应的化学方程式为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
;C为FeCl2;配制FeCl2的溶液时可加入少量盐酸可以防止亚铁离子的水解,故答案为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;FeCl2 ;盐酸;
②若A是某强酸的稀溶液,实现上述转化必须要求酸是氧化性酸,判断为HNO3,故答案为:HNO3;
(2)若A是一种能使湿润的红色石蕊试纸变蓝的气体,判断A为碱性气体为NH3,B是汽车尾气之一,遇空气会变色,证明D为O2,反应①是氨气的催化氧化反应生成一氧化氮和水;化学方程式为:4NH3+5O2催化剂.△4NO+6H2O,故答案为:4NH3+5O2催化剂.△4NO+6H2O;
(3)若B有两性可能是两性氧化物或两性氢氧化物;
①若D是强酸,B为两性 氢氧化物为Al(OH)3,则能确定A、C中肯定含的离子的化学式分别是:AlO2-、Al3+,故答案为:AlO2-;Al3+;
②若D是强碱,B为两性氢氧化物为Al(OH)3,A为Al3+反应②是氢氧化铝和强碱反应,反应的离子方程式是:Al(OH)3+OH-=AlO2-+2H2O,
故答案为:Al(OH)3+OH-=AlO2-+2H2O;
(4)若A、B、C的焰色反应都呈黄色,证明含有钠元素,D是气态酸性氧化物实现上述变化,D可以是CO2,SO2,依据性质鉴别可以用高锰酸钾溶液,品红试液,
故答案为:品红溶液;溴水或高锰酸钾溶液;
本题解析:
本题难度:简单
5、简答题 有A、B、C、D、E五种物质,其中A为金属单质,灼烧时火焰呈黄色,C为淡黄色固体,它们之间的转化关系如图所示:
请写出各物质的化学式
A______;B______;C______;D______;E______.
参考答案:①根据题眼A为金属单质,灼烧时火焰呈黄色,判断:A是Na;
②根据A置于空气中,钠极易和氧气反应生成氧化钠,判断:B是Na2O;
③根据A在空气中燃烧生成C,C为淡黄色固体,判断:C是Na2O2;
④A、C分别与水反应都生成D,2Na+2H2O=2NaOH+H2↑、2Na2O2+2H2O=4NaOH+O2↑,
根据方程式知其相同产物是NaOH,所以D是NaOH;
⑤B、C分别与二氧化碳反应都生成E,Na2O+CO2=Na2CO3、2Na2O2+2CO2=2Na2CO3+O2↑,
根据方程式知其相同产物是Na2CO3,所以E是Na2CO3;
故答案为:Na;Na2O;Na2O2;NaOH;Na2CO3.
本题解析:
本题难度:一般