微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 若电解含有0.04mol CuSO4和0.04mol NaCl的混合溶液400mL,当阳极产生672mL(标准状况下)气体时,下列叙述正确的是
A.电解后溶液的c(H+)="0.1mol/L"
B.阴极产物除了Cu,还有H2
C.要恢复到原来的浓度和pH,可以向溶液中加入一定量的CuCl2固体
D.在整个电解过程中,共转移了0.08mol电子,且在阴极上Cu2+得电子被氧化
参考答案:A
本题解析:阳极首先是氯离子放电,生成氯气,其次是溶液中的OH-放电,生成氧气。由于氯离子的物质的量是0.04mol,则生成氯气是0.02mol,标准状况下的体积是448ml。但阳极实际生成气体是762ml,这说明阳极还有224ml的氧气生成,其中氧气的物质的量是0.01mol,则反应中共转移电子的物质的量是0.08mol。阴极首先是铜离子放电,其次是溶液中的氢离子放电。0.04mol铜离子恰好得到0.08mol电子生成0.04mol单质铜,所以电解后溶液中的溶质是0.02mol硫酸钠,和0.02mol硫酸,则溶液中氢离子的浓度是0.04mol÷0.4L=0.1mol/L,A正确。B不正确,没有氢气生成;C不正确,除了加入氯化铜外,还应该加入氧化铜;D不正确,在阴极上Cu2+得电子被还原,答案选A。
点评:
本题难度:简单
2、填空题 (10分)如图为相互串联的甲乙两个电解池,请回答:
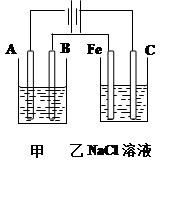
甲池若为用电解精炼铜的装置:
(1)A极电极反应为 ,
B极电极反应为_ _,
乙池中的总反应离子方程式为 。
(2)若甲槽阴极增重12.8g,则乙槽阴极放出气体在标准状况下的体积为 。
(3)若乙槽剩余液体为400mL,则电解后得到碱液的物质的量浓度为 。
参考答案:(10分) (1) Cu2+ + 2e
本题解析:
本题难度:一般
3、填空题 (1)有人研究证明:使用氯气作自来水消毒剂,氯气会与水中有机物反应,生成如CHCl3等物质,这些物质可能是潜在的致癌致畸物质。目前人们已研发多种饮用水的新型消毒剂。下列物质不能作自来水消毒剂的是_____________(填序号)。
A.硫酸铜 B.二氧化氯 C.臭氧 D.硫酸亚铁
(2)高铁(VI)酸盐(如Na2FeO4)是新一代水处理剂。其制备方法有:次氯酸盐氧化法(湿法)和高温过氧化物法(干法)等。湿法是在碱性溶液中用次氯酸盐氧化铁(III)盐,写出该法的离子方程式:
___________________________。
(3)用高铁(VI)酸盐设计的高铁(VI)电池是一种新型可充电电池,电解质溶液为KOH溶液,放电时的总反应:3Zn+2K2FeO4+8H2O→3Zn(OH)2+2Fe(OH)3+4KOH
①写出正极发生的电极反应式:______________________。
②用高铁(VI)电池作电源,以Fe作阳极,以Cu作阴极,对足量KOH溶液进行电解,当电池中有
0.2molK2FeO4反应时,则在电解池中生成H2 __________L(标准状况)。
③下表列出了某厂排放的含锌废水中的含量及国家环保标准值的有关数据

该厂只用调节pH处理废水,当调整为pH=7时,此时废水中Zn2+的浓度为__________mg/L,_________(填“符合”或“不符合”)国家环保标准。(常温下,Ksp[Zn(OH)2]=1.2×10-17)
参考答案:(1)AD
(2)①10OH-+3ClO-+2Fe3+==3Cl-+2FeO42-+5H2O
(3)①FeO42-+4H2O+3e-=Fe(OH)3+5OH- ;②6.72;③78;不符合
本题解析:
本题难度:困难
4、简答题 课题式研究性学习是培养学生创造思维的良好方法,某研究性学习小组将下列装置如图连接,C、D、E、F、G、H?都是惰性电极.将电源接通后,向乙中滴入酚酞试液,在F极附近显红色.试回答下列问题:
(1)电源A?极的名称______.
(2)甲装置中C极反应式______.
(3)E极反应式______.在C、D、E、F各电极上析出生成物的物质的量比是______
(4)欲用丙装置精炼粗铜,G应该是______(填“纯铜”或“粗铜”);欲用丙装置向铁棒上镀铜,H应该是______(填“铜”或“铁”),开始G、H两极材料质量相同,电镀一段时间后,两极质量之差为2.56g,则经过电路中电子数目为______.
参考答案:(1)根据题意知,F极有氢离子得电子析出氢气,所以F极是阴极,与阴极相连的原电池电极是负极,所以B是负极,A是正极,故答案为:正极;
(2)甲装置中C极是阳极,阳极上失电子发生氧化反,溶液中氢氧根离子的放电能力大于硫酸根离子,所以在C极上氢氧根离子放电生成水和氧气,电极反应式4OH--4e-=2H2O+O2↑,
故答案为:4OH--4e-=2H2O+O2↑;
(3)通过(1)知,F是阴极,所以E是阳极,溶液中氯离子的放电能力大于氢氧根离子,所以氯离子在E极上失电子生成氯气,电极反应式为2Cl--2e-=Cl2↑,
在阳极上失电子阴极上得电子,甲装置中氢氧根的失电子能力大于硫酸根离子,铜离子得电子能力大于氢离子得电子能力,乙装置中氯离子失电子能力大于氢氧根离子,
氢离子得电子能力大于钠离子,所以在C、D、E、F分别析出氧气、铜、氯气、氢气;电解时,通过的电子数相同,通过相同数目的电子时析出氧气、铜、氯气、氢气的物质的量
之比为1:2:2:2,故答案为:2Cl--2e-=Cl2↑;1:2:2:2;
(4)电镀时,镀层作阳极,所以G应是粗铜;镀件作阴极,铁作镀件,所以H是铁;
电镀时,阳极上铜失电子生成铜离子进入溶液,所以质量减少,阴极上铜离子得电子生成铜,质量增加,
所以两极质量差为阳极减少的质量加上阴极增加的质量.
设通过x个电子,铜质量与电子的关系为:
? 2Cu--2e-
128g?2N A
?2.56g? x
所以x=0.04N A
故答案为:粗铜;铁;0.04N A.
本题解析:
本题难度:一般
5、选择题 用隔膜电解法处理高浓度乙醛废水的原理是使乙醛分别在两极发生反应,转化为乙醇和乙酸。实验室中,以一定浓度的乙醛―Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置示意图如图所示。有关说法不正确的是
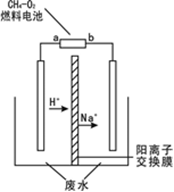
A.图中燃料电池的a极应通入氧气
B.乙醇在阴极产生
C.电解过程中,阴极区有NaOH产生
D.每生成1mol乙酸,理论上至少消耗标况下氧气22.4L