微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在20 mL 0.1mol・L-1NaOH溶液中逐滴加入0.1 mol・L-1 CH3COOH溶液,曲线如图所示,有关粒子浓度关系正确的是
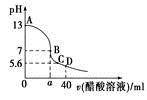
A.溶液?性时,回滴加入适量的NaOH,溶液中离子浓度可能为c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
B.C点时其pH=5.6,溶质恰好为等物质的量CH3COONa和CH3COOH,则溶液中微粒浓度关系为:c(Na+)>c(CH3COO-)
C.在B点,a>20,且有c(Na+)=c(CH3COO-)=c(OH-)=c(H+)
D.在D点:c(CH3COOH)=c(OH-)-c(H+)
参考答案:D
本题解析:A项因违背电荷守衡而错误;溶液的pH=5.6,溶液呈酸性,即c(H+)>c(OH-),可以判断CH3COOH的电离程度大于CH3COONa的水解程度,所以离子浓度的大小顺序是:c(CH3COO-)>c(Na+),选项B错误;因为NaOH溶液中加入CH3COOH溶液当物质量相等时恰好生成CH3COONa,但此时溶液为中性,故只有醋酸过量即a>20,由于电荷守衡c(Na+)+c(H+)=c(CH3COO-)+c(OH-),又此时溶液为中性,因此c(OH-)=c(H+),c(Na+)=c(CH3COO-),但是c(Na+)=c(CH3COO-)>c(OH-)=c(H+),选项C错误;D点看作溶液总体积为40 ml,钠离子的量就等于溶液中醋酸存在的所有形式,既c(CH3COO-)+c(CH3COOH)=c(Na+),而c(CH3COO-)+c(OH-)-c(H+)=c(Na+),两式子合并可得c(CH3COOH)=c(OH-)-c(H+),D项正确。
本题难度:一般
2、选择题 PH=2的两种一元酸x和y,体积均为100ml,稀释过程中PH与溶液体积的关系如图所示,分别滴加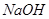 溶液(c=0.1
溶液(c=0.1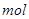 /L)至PH=7,消耗
/L)至PH=7,消耗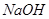 溶液的体积为Vx,Vy,则
溶液的体积为Vx,Vy,则
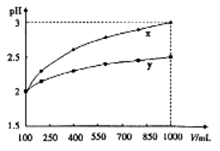
A.x为弱酸Vx<Vy
B.x为强酸Vx>Vy
C.y为强酸Vx>Vy
D.y为弱酸Vx<Vy
参考答案:D
本题解析:酸稀释过程中溶液的PH与稀释的关系为:
若为强酸,加水稀释至原溶液体积的10n倍,PH增加n个单位;
若为弱酸,加水稀释至原溶液体积的10n倍,PH增加的单位数少于n。
注:无论是强酸还是弱酸,无论稀释多少倍溶液PH均小于7。
由图分析,当加水稀释至原溶液体积的10倍时,X酸的PH由2增大为3,即X为一元强酸;而Y酸PH变化少于1介于2、3之间,所以Y酸为一元弱酸。
等体积等PH的一元强酸与一元弱酸,弱酸的物质的量过量,中和NaOH溶液,消耗的NaOH的物质的量更多。
综上所述,正确确答案为D。
本题难度:一般
3、选择题 对pH值相同的盐酸和醋酸两种溶液的说法正确的是( )
A.中和碱的能力相同
B.盐酸和醋酸的物质的量浓度相同
C.OH-的物质的量浓度相同
D.H+的物质的量浓度不同
参考答案:A.中和碱的能力与酸的物质的量成正比,酸的物质的量未知,无法判断中和碱能力强弱,故A错误;
B.醋酸是强电解质,氯化氢是强电解质,pH相等的醋酸和盐酸,醋酸的浓度大于盐酸,故B错误;
C.根据c(OH-)=Kwc(H+)知,pH相等的醋酸和盐酸中氢离子浓度相等,温度相等,水的离子积常数相等,则氢氧根质量浓度相等,故C正确;
D.根据c(H+)=10-pH 知,pH相等的醋酸和盐酸中,氢离子浓度相等,故D错误;
故选C.
本题解析:
本题难度:一般
4、计算题 在25℃下,将a mol・L-1的氨水与0.01mol・L-1的盐酸等体积混合后,溶液中c(NH4+)=c(Cl-)。试用含a的代数式计算NH3・H2O的电离常数Kb。
参考答案: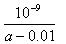 ?mol・L-1
?mol・L-1
本题解析:略
本题难度:简单
5、选择题 pH相同的醋酸溶液和盐酸,分别用蒸馏水稀释至原体积的m倍和n倍,稀释后两溶液pH仍相同,则m和n的关系是( )
A.m=n
B.m>n
C.m<n
D.无法判断