微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下表为4种常见溶液中溶质的质量分数和物质的量浓度

这4种溶液中密度最小的是
[? ]
A.HCl
B.NaOH
C.CH3COOH
D.HNO3
参考答案:C
本题解析:
本题难度:简单
2、选择题 下列对于“摩尔”的理解正确的是
[? ]
A.摩尔是国际科学界建议采用的一种物理量
B.摩尔是物质的量的单位,简称摩,符号为mol
C.摩尔可以把物质的宏观数量与微观粒子的数量联系起来
D.国际上规定,0.012kg碳原子所含有的碳原子数目为1摩
参考答案:B
本题解析:
试题分析:
解:A.物质的量是物理量,摩尔是单位,故A错误;
B.物质的量是含有一定数目粒子的集体,单位是摩尔,简称摩,符号为mol,故B正确;
C.物质的量是连接宏观物质与微观粒子的桥梁,摩尔是单位,故C错误;
D.0.012?kg碳原子所含有的碳原子数目为1?mol,碳原子指含有6个质子6个中子的原子,若为14C则不是1mol,本选项未明确,故D错误.
故选B.
本题难度:简单
3、选择题 设阿伏加德罗常数的数值为NA,则下列说法正确的是:(?)
A.常温常压下,11.2 L甲烷中含有的氢原子数为2NA
B.标准状况下,0.3 mol二氧化碳中含有氧原子数为0.3 NA
C.常温下,2.7 g铝与足量的盐酸反应,失去的电子数0.3 NA
D.常温下,1 L 0.1 mol / L MgCl2溶液中含Mg2+数为0.2 NA
参考答案:C
本题解析:A错误,非标准状况下的气体摩尔体积题目没有给出,所以无法计算.
B错误,标准状况下,0.3 mol二氧化碳中含有氧原子数为0.6 NA
C正确,铝不足,以铝的量来计算,0.1molAL失去0.3mol电子,数目为0.3 NA
D错误, 1 L 0.1 mol / L MgCl2溶液中含Mg2+数为0.1 NA
本题难度:一般
4、计算题 有一瓶100ml硫酸和硝酸的混合溶液,取出10.00ml该混合溶液,加入足量氯化钡溶液,充分反应后过滤、洗涤、烘干,得4.66g沉淀。滤液跟2.00mol/L的NaOH溶液反应共用去35.00mlNaOH溶液时恰好使溶液呈中性,则混合酸中硫酸和硝酸的物质的量的浓度是多少?
参考答案:c(H2SO4)=2.00mol/L?c(HNO3)=3.00mol/L
本题解析:硫酸与硝酸的混合溶液,取出10mL加入足量BaCl2溶液,过滤、洗涤、烘干后得到4.66g的沉淀为硫酸钡,根据n=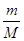 计算硫酸钡的物质的量,再根据硫酸根守恒n(H2SO4)=n(BaSO4),滤液中氢离子物质的量不变,与2.0mol?L-1NaOH溶液反应,用去35mL碱液时恰好完全中和,酸与氢氧化钠恰好反应,H+与OH-1:1反应,故n(HNO3)+2(H2SO4)=n(NaOH),根据c=
计算硫酸钡的物质的量,再根据硫酸根守恒n(H2SO4)=n(BaSO4),滤液中氢离子物质的量不变,与2.0mol?L-1NaOH溶液反应,用去35mL碱液时恰好完全中和,酸与氢氧化钠恰好反应,H+与OH-1:1反应,故n(HNO3)+2(H2SO4)=n(NaOH),根据c=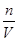 计算硫酸、硝酸的物质的量浓度。
计算硫酸、硝酸的物质的量浓度。
解:硫酸与硝酸的混合溶液,取出10mL加入足量BaCl2溶液,过滤、洗涤、烘干后得到4.66g的沉淀为硫酸钡,硫酸根守恒,故n(H2SO4)=n(BaSO4)=4.66g÷233g/mol=0.02mol
故原溶液中c(H2SO4)=0.02mol÷0.01L=2.00mol/L
滤液中氢离子物质的量不变,与2.0mol?L-1NaOH溶液反应,用去35mL碱液时恰好完全中和,酸与氢氧化钠恰好反应,H+与OH-1:1反应
故n(HNO3)+2(H2SO4)=n(NaOH)
即n(HNO3)+2×0.02mol=0.035L×2mol/L
解得n(HNO3)=0.03mol
所以原溶液中c(HNO3)=0.03mol÷0.01L=3.00mol/L,
本题难度:一般
5、选择题 NA表示阿伏加德罗常数的值,下列叙述正确的是
A.5.6 g铁与足量硫的反应中,铁失去的电子数为0.3NA
B.标准状况下,22.4 L SO3所含原子数为4 NA
C.1.8g的NH4+离子中含有的电子数为NA
D.20 g D2O中所含的中子数为8 NA、
参考答案:C
本题解析:略
本题难度:简单