微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列各项比较中正确的是
A.共价键极性CCl4>SiCl4
B.沸点CH3CH2OH>CH3CH2Cl
C.元素的电负性Ca>Mg
D.晶格能KCl>NaCl
参考答案:B
本题解析:A:所涉及的Cl、C、Si元素的非金属性Cl > C > Si,所以SiCl4的极性大
B:前者为液太,后者为气态,正确;C:二者相比,前者金属性强,电负性小;
D:二者相比,Na+的半径小于K+半径,NaCl晶格能更大。
本题难度:一般
2、选择题 X,Y,Z是3种短周期元素,其中X,Y位于同一族,Y,Z处于同一周期。X原子的最外层电子数是其电子层数的3倍,Z原子的核外电子数比Y原子少1。下列说法正确的是
[? ]
A.元素非金属性由弱到强的顺序为Z<Y<X
B.Y元素最高价氧化物对应水化物的化学式可表示为H3YO4
C.3种元素的气态氢化物中,Z的气态氢化物最稳定
D.原子半径由大到小的顺序为Z>Y>X
参考答案:AD
本题解析:
本题难度:一般
3、选择题 下列叙述正确的是
A.同周期元素ⅦA族元素的原子半径最大
B.ⅥA族元素的原子,其半径越大,越容易得到电子
C.室温时,零族元素的单质都是气体
D.第ⅠA族中全是金属元素
参考答案:C
本题解析:在同周期中,零族元素的原子半径最大,而在同主族中,半径越大,越难得电子.单原子离子的化合价和它的族序数不一定相等,如ⅣA族的Pb2+.
本题难度:一般
4、简答题 下表标出的是元素周期表的一部分元素,回答下列问题
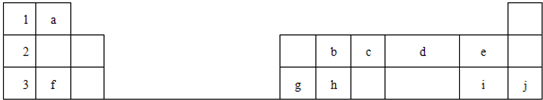
(1)表中列出的10种元素中,化学性质最不活泼的是______(填元素名称,下同),非金属性最强的是______,原子半径最小的是______.
(2)分子bd2的电子式______,元素e的负一价阴离子的结构示意图______.
(3)物质bd2和hd2在物理性质上有着巨大差异,其原因是物质bd2属于______晶体,物质hd2属于______晶体.
(4)元素e的气态氢化物比元素i的气态氢化物______(填“稳定”或“不稳定”)
(5)元素f、g的最高价氧化物对应水化物之间反应的离子方程式是______;
(6)物质fda含有的化学键类型是______.
参考答案:根据元素在周期表中的分布知识,可以确定a是H,b是C,c是N,d是O,e是F,f是Na,g是Al,h是Si,i是Cl,j是Ar.
(1)表中列出的10种元素中,稀有气体元素Ar化学性质稳定,同一周期,元素原子半径从左到右半径在减小,同一主族元素的原子半径从上到下逐渐增大;所以原子半径最小的是H,同周期元素的原子从左到右,元素的非金属性逐渐增强,同一主族,元素的原子从上到下,元素的非金属性逐渐减弱,所以费金属性最强的是F,故答案为:氩;氟;氢;
(2)二氧化碳是碳原子和氧原子之间通过共价双键形成的共价化合物,电子式为:
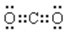
,氟离子核外电子数为10,离子的结构示意图为:
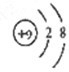
,故答案为:
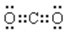
;

;
(3)二氧化碳是分子晶体,二氧化硅是原子晶体,分子晶体的熔点低于原子晶体,故答案为:分子;原子;
(4)同主族元素的原子,从上到下氢化物越来越稳定,所以元素F的气态氢化物比元素Cl的气态氢化物稳定,故答案为:稳定;
(5)元素f的最高价氧化物对应水化物是氢氧化钠,g的最高价氧化物对应水化物是氢氧化铝,氢氧化铝是两性氢氧化物,能和强碱反应,实质是:Al(OH)3+OH-=[Al(OH)4]-,故答案为:Al(OH)3+OH-=[Al(OH)4]-;
(6)氢氧化钠中钠离子和氢氧根之间是离子键,氧和氢之间是共价键,故答案为:离子键和共价键.
本题解析:
本题难度:一般
5、填空题 按要求填空:
(1)与Ne原子电子层结构相同的-2价阴离子,填写微粒的结构示意图:___________________;
(2)用电子式表示两核10电子的共价化合物形成过程:___________________________;
(3)在1~18号元素中,气态氢化物的水溶液呈碱性的化合物的结构式:__________ 。
(4)相对分子质量为58的烷烃的分子式是_______________,它可能的结构简式是 ______________________________________________
参考答案:“略”
本题解析:
本题难度:一般