微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 如果你在厨房不小心将花生油与凉开水混在一起,你将采用下列何种方法进行分离
A.过滤
B.蒸馏
C.分液
D.萃取
参考答案:C
本题解析:萃取适合于溶质在不同溶剂中的溶解性不同而分离的一种方法,分液适用于互不相溶的液体之间的一种分离方法,蒸馏是依据混合物中个组分沸点不同而分离的一种法,适用于除去易挥发、难挥发或不挥发杂质,过滤适用于不溶性固体和液体之间的一种分离方法。花生油不溶于水,分液即可,答案选C。
本题难度:困难
2、填空题 (7分)氮元素可以形成多种化合物。
(1)基态氮原子的价电子轨道表示式是 。
(2)已知尿素的结构式为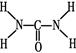 ,则尿素分子中C和N原子的杂化方式分别是、。
,则尿素分子中C和N原子的杂化方式分别是、。
(3)肼(N2H4)分子可视为NH3分子中的一个氢原子被―NH2(氨基)取代形成的另一种氮化物。
①NH3分子的空间构型是;
②肼可用作火箭燃料,燃烧时发生的反应是:
N2O4(l)+2N2H4(l)=3N2(g)+4H2O(g)△H=-1038.7kJ・mol-1
当肼燃烧放出519.35kJ热量时,形成的π键有mol。
参考答案:(1) (2分)(2)sp2(1分)sp3(1分)
(2分)(2)sp2(1分)sp3(1分)
(3)①三角锥形(1分)②3(2分)
本题解析:(1)氮元素的核外电子数是7个,则根据核外电子排布规律可知基态氮原子的价电子轨道表示式是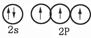 。
。
(2)根据尿素的结构简式可知,分子中氮元素全部形成单键,因此是sp3杂化;碳元素形成2个单键,1个双键,因此是sp2杂化。
(3)①氨气分子中氮原子的价层电子对数=4,其中有一对孤对电子,所以氨气是三角锥形。
②当肼燃烧放出519.35kJ热量时,根据热化学方程式可知生成氮气的物质的量是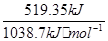 ?×3=1.5mol。氮气分子中含有2个π键,则π键的物质的量是3mol。
?×3=1.5mol。氮气分子中含有2个π键,则π键的物质的量是3mol。
本题难度:一般
3、选择题 几种短周期元素的原子半径及主要化合价如下表:
元素代号
| X
| Y
| Z
| W
|
原子半径
| 160
| 143
| 70
| 66
|
主要化合价
| +2
| +3
| +5、+3、-3
| -2
|
下列叙述正确的是
A.X、Y元素的金属性 X<Y
B.一定条件下,Z单质与W的常见单质直接生成ZW2
C.Y的最高价氧化物对应的水化物能溶于稀氨水
D.第一电离能由大到小的顺序是Z>W>X>Y
参考答案:D
本题解析:根据元素的主要化合价和原子半径可知,X是镁,Y是Al,Z是N,W是氧元素。A不正确,镁的金属性强于铝的。氮气和氧气直接化合生成物是NO,B不正确。氧化铝是两性氧化物,但不溶于氨水,C不正确。非金属性越强,第一电离能越大,但由于氮元素的2p轨道是半充满,稳定性强,所以第一电离能大于氧元素的,D正确。答案选D。
本题难度:一般
4、选择题 主族元素在周期表中的位置,取决于元素原子的
A.相对原子质量和核电荷数
B.电子层数和中子数
C.电子层数和最外层电子数
D.金属性和非金属性的强弱
参考答案:C
本题解析:周期表分为周期和族,周期数是电子层数,主族序数是最外层电子数,所以答案选C。
本题难度:简单
5、选择题 我国最新报导的高超导体中,铊(Tl)是其中之一,已知位于第六周期第ⅢA族,关于铊的说法,可能错误的是:(?)
A.Tl(OH)3 有两性
B.是银白色金属
C.与稀盐酸反应生成盐酸盐
D.铊的金属性强于铝的金属性
参考答案:A
本题解析:同主族元素从上到下元素的金属性逐渐增强,最高价氧化物的水化物的碱性逐渐增强,所以Tl(OH)3 显碱性,故A不正确;金属大部分是银白色金属,B正确;同主族元素从上到下元素的金属性逐渐增强,则铊的金属性强于铝,与稀盐酸反应生成盐酸盐,所以选项CD均是正确的,答案选A。
点评:该题是高考中的常见题型,属于中等难度的试题。试题紧扣教材,基础性强,主要是考查学生灵活运用元素周期律解决实际问题的能力,有利于培养学生的逻辑思维能力和发散思维能力。
本题难度:简单