微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 现有CaCl2、NaOH、CH4、H2、H2O、(NH4)2SO4、Si、Fe、Ne?9种物质。 ?
(1)只含有离子键的是__________(填写物质的化学式,下同)。 ?
(2)含有共价键,但其晶体属于离子晶体的是__________。?
(3)含有共价键,其晶体属于分子晶体,且晶体微粒间相互作用力只有一种的是______________,这种分子间作用力也叫__________。 ?
(4)含有共价键,其晶体属于分子晶体,且晶体微粒间相互作用力有多种类型的是__________,这种物质中区别于(3)中的相互作用力叫______________。 ?
(5)单质形成的晶体,晶体微粒间的相互作用相同的是__________和__________,这两物质形成的晶体__________(填“属于”或“不属于”)同种类型晶体。 ?
(6)除(NH4)2SO4外,晶体结构中存在正四面体构型的是___________。
参考答案:(1)CaCl2?
(2)?NaOH和(NH4)2SO4?
(3)CH4和H2;范德华力?
(4)?H2O;氢键?
(5)H2;Ne;属于 ?
(6)CH4
本题解析:
本题难度:一般
2、选择题 有关晶体的下列说法中正确的是
[? ]
A.晶体中分子间作用力越大,分子越稳定
B.原子晶体中共价键越强,熔点越高
C.冰熔化时水分子中共价键发生断裂
D.氯化钠熔化时离子键未被破坏
参考答案:B
本题解析:
本题难度:简单
3、选择题 北京大学和中国科学 91eXaM.org院的化学工作者合作,已成功研制出碱金属与C60的形成的球碳盐K3C60。实验测知该物质属于离子晶体,具有良好的超导性。下列关于K3C60的组成和结构的分析中正确的是
[? ]
A.K3C60中既有离子键,又有极性键
B.1 mol K3C60中含有的离子数目为63×6.02×1023
C.该晶体在熔融状态下能导电
D.该物质的化学式可写为KC20
参考答案:C
本题解析:
本题难度:一般
4、选择题 下列数据是对应物质的熔点,据此做出的下列判断中错误的是
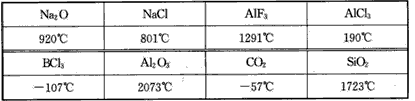
[? ]
A.铝的化合物的晶体中有的是离子晶体
B.表中只有BCl3和干冰是分子晶体
C.同族元素的氧化物可形成不同类型的晶体
D.不同族元素的氧化物可形成相同类型的晶体
参考答案:B
本题解析:
本题难度:一般
5、填空题 (三选一)【选修3:物质结构与性质】
有X、Y、Z三种元素,原子序数依次增大,它们的原子序数之和为43。其中,Y原子的最外层电子数是次外层电子数的三倍。X、Y元素的单质都是构成空气的主要成分。
(1)基态Z原子的价层电子排布式为________;XY3-离子的空间构型为________。
(2)ZO(氧化物)、FeO晶体结构类型均与NaCl的相同,Z2+和Fe2+离子半径分别为69pm和78pm,则熔点ZO______FeO(填“”?);ZO晶体中Z2+的配位数为___________。
(3)化合物A常用于检验Z2+:在稀氨水介质中,A与Z2+ 反应可生成鲜红色沉淀,其结构如图所示:
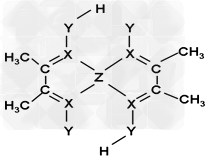
①0.5mol化合物A?中含σ键数为_______;鲜红色沉淀中X与Z2+离子间形成的是配位键,在图上标出配位键的电子给予的方向。
②该结构中,Y原子与氢原子除了形成共价键外,还存在_______作用;该结构中,碳原子的杂化轨道类型有_____。
参考答案:(1)3d84s2;平面三角形
(2)?>;6
(3)①7×6.02×1023?;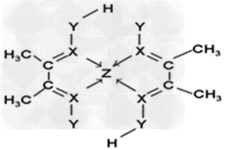 ②氢键;sp2、sp3
②氢键;sp2、sp3
本题解析:
本题难度:一般